Struttura di idrossido di rame (ii), proprietà, nomenclatura, usi

- 1521
- 193
- Dante Morelli
Lui Copper Idrossido (II) O Cupric Idrossido è un solido inorganico cristallino blu o blu verdastro la cui formula chimica è Cu (OH)2. Si ottiene come precipitato voluminoso blu aggiungendo un idrossido alcalino a soluzioni rame (significa che contengono ioni Cu2+). È un composto instabile.
Per aumentare la sua stabilità, è preparato in presenza di ammoniaca (NH3) o fosfati.Se si prepara in presenza di ammoniaca c'è un materiale con buona stabilità e dimensioni di grandi particelle.
 Campione di idrossido cupric, Cu (OH)2. Samzane presso italiano Wikipedia [dominio pubblico] Fonte: Wikipedia Commons
Campione di idrossido cupric, Cu (OH)2. Samzane presso italiano Wikipedia [dominio pubblico] Fonte: Wikipedia Commons Quando si prepara con il fosfato di rame (II), Cu3(Po4)2, Si ottengono una dimensione delle particelle più fine e una superficie più ampia. L'idrossido rastrelloso è ampiamente usato come fungicida e batterica in agricoltura e per curare il legno, estendendo la sua vita utile.
Viene anche usato come integratore di alimenti per animali. È usato come materia prima per ottenere altri sali di rame (II) e in galvanoplastica per coprire le superfici.
Studi vengono condotti per stimare il loro potenziale per combattere le infezioni batteriche e fungine nell'essere umano.
[TOC]
Struttura
L'idrossido di rame (II) contiene ioni di rame infiniti (Cu2+) United per gruppi idrossilici (OH-).
Le catene sono così confezionate che 2 atomi di ossigeno da altre catene sono al di sopra e sotto ogni atomo di rame, quindi adottando una configurazione ottaedrica distorta, che è comune nella maggior parte dei composti di rame (II).
Nella sua struttura, quattro atomi di ossigeno sono a una distanza di 1,93 a; Due atomi di ossigeno sono 2,63 A; E la distanza Cu-Cu è da 2,95 a.
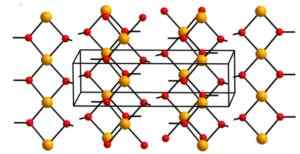 Struttura cristallina di idrossido cupric. Aleksandar Kondinski [CC BY-SA.0 (https: // creativeCommons.Org/licenze/by-sa/4.0)]. Fonte: Wikipedia Commons
Struttura cristallina di idrossido cupric. Aleksandar Kondinski [CC BY-SA.0 (https: // creativeCommons.Org/licenze/by-sa/4.0)]. Fonte: Wikipedia Commons Nomenclatura
- Copper Idrossido (II).
- Idrossido cupric.
- Diidrossido di rame.
Proprietà
Stato fisico
Solido cristallino.
Peso molecolare
99,58 g/mol.
Punto di fusione
Si rompe prima di sciogliersi. Punto di degradazione 229 ºC.
Può servirti: 25 esempi di solubilità nella vita di tutti i giorniDensità
3,37 g/cm3
Solubilità
È praticamente insolubile in acqua: 2,9 microgrammi/L a 25 ºC. Rapidamente solubile in acidi, in soluzioni alcaline concentrate e idrossido di ammonio. Insolubile in solventi organici. In acqua calda decompone generando ossido di rame (II), che è più stabile.
Altre proprietà
È facilmente solubile in acidi forti e anche in soluzioni concentrate alcaline di idrossidi, per dare anioni blu profondi, probabilmente il tipo [CUN(OH)2n+2"2-.
La sua stabilità dipende dal metodo di preparazione.
Può essere scomposto dando ossido di rame (II) nero (CUO) se rimane a riposo qualche giorno o a basso riscaldamento.
In presenza di un eccesso di alcali si rompe oltre 50 ° C.
Applicazioni
In agricoltura
L'idrossido di rame (II) ha un'ampia applicazione come fungicida e antibatterico nelle colture agricole. Ecco alcuni esempi:
- Serve contro le macchie batteriche ( Erwinia) In lattuga, applicando come un trattamento fogliare.
- Contro le macchie batteriche (di Xanthomonas pruni) Nelle pesche, per le quali viene applicato un trattamento latente e fogliare.
- Viene usato contro il foglio e lo stelo dei mirtilli attraverso applicazioni latenti.
- Contro il marciume durante la conservazione dei mirtilli causati da Monilinia oxycocci, per applicazione latente.
Per l'applicazione in agricoltura, viene utilizzato l'idrossido di rame (II) che viene preparato in presenza di fosfati a causa della sua piccola dimensione delle particelle.
 Coltivazione di lattuga. Fonte: Pixabay
Coltivazione di lattuga. Fonte: Pixabay Nella conservazione del legno
Il legno, a causa della natura organica, è sensibile all'attacco di insetti e microrganismi. L'idrossido di rame (II) è usato come biocide per funghi che attaccano il legno.
Di solito viene utilizzato accanto a un composto di ammonio quaternario (NH4+). L'idrossido di rame funge da fungicida e il composto di ammonio quaternario funziona come un insetticida.
In questo modo, il legno trattato sopporta o resiste alle condizioni di servizio, raggiungendo il livello di prestazioni richiesto dall'utente. Tuttavia, il legno trattato con questi composti ha un alto livello di rame ed è molto corrosivo per l'acciaio comune, quindi è richiesto un tipo di acciaio inossidabile che può sopportare la lavorazione del legno trattato.
Può servirti: reazione reversibile: caratteristiche ed esempiNonostante la sua utilità, l'idrossido di rame (II) è considerato un biocide leggermente pericoloso.
Per questo motivo, c'è la preoccupazione che sia rilasciato dal legno trattato all'ambiente in quantità che possono essere dannose per i microrganismi presenti naturalmente nelle acque (fiumi, laghi, zone umide e mare) o il suolo.
Nella produzione di Rayón
Dal diciannovesimo secolo, sono state utilizzate soluzioni ammoniaali di idrossido di rame (II). Questo è uno dei primi passi per ottenere la fibra chiamata Rayón attraverso la tecnologia sviluppata da BEMBERG in Germania.
L'idrossido di rame (II) si dissolve in una soluzione di ammoniaca (NH3), formando un sale complesso.
Fibre di cotone raffinate corti vengono aggiunte alla soluzione ammoniaca di rame contenente idrossido di rame (II) sotto forma di solido precipitato.
La cellulosa di cotone forma un complesso con idrossido di rame tetra-ammonio che si dissolve nella soluzione.
Successivamente, questa soluzione è coagula mentre passa attraverso un dispositivo di estrusione.
A causa del suo alto costo, questa tecnologia è già stata superata da quella della viscosa. La tecnologia di BEMBERG è attualmente utilizzata solo in Giappone.
Nell'industria alimentare degli animali
È usato come tracce di alimentazione animale, poiché è una delle sostanze richieste come micronutrienti per la nutrizione completa degli animali.
 Cibo concentrato per il bestiame. ThamizhpParithi Maari [CC BY-SA 3.0 (https: // creativeCommons.Org/licenze/by-sa/3.0)]. Fonte: Wikipedia Commons
Cibo concentrato per il bestiame. ThamizhpParithi Maari [CC BY-SA 3.0 (https: // creativeCommons.Org/licenze/by-sa/3.0)]. Fonte: Wikipedia Commons Questo perché negli esseri vivi più alti è un elemento essenziale, richiesto per l'attività di una varietà di enzimi contenenti rame.
Ad esempio, è contenuto nell'enzima che partecipa alla produzione di collagene e all'enzima richiesto per la sintesi di melanina, tra gli altri.
Può servirti: ammineÈ un composto generalmente riconosciuto come assicurazione se aggiunto a livelli coerenti con una buona pratica alimentare.
 Vacche latte. Fonte: Pixabay
Vacche latte. Fonte: Pixabay Nella produzione di altri composti di rame (II)
Precursore attivo nella produzione dei seguenti composti di rame (II): rame (II), 2-otilhexanoato di rame (II) e saponi di rame e saponi di rame. In questi casi viene utilizzato l'idrossido di rame (II) che viene sintetizzato in presenza di ammoniaca.
Altri usi
Viene utilizzato nella stabilizzazione del nylon, negli elettrodi a batteria; come fissaggio a colori nelle operazioni di tintura; come pigmento; negli insetticidi; nel trattamento della carta e nella colorazione; nei catalizzatori, come catalizzatore nella vulcanizzazione della gomma polisolfuro; come pigmento anti -sniffing; e in elettrolisi, in galvanoplastica.
Future applicazioni mediche
L'idrossido di rame (II) fa parte di composti di rame che vengono studiati sotto forma di nanoparticelle per l'eliminazione di batteri come E. coli, K. Pneumoniae, p. Aeruginosa, Salmonella spp., Tra gli altri, le cause delle malattie nell'essere umano.
È stato anche scoperto che le nanoparticelle di rame possono essere efficaci contro Candida albicans, Un fungo che è la causa comune delle patologie umane.
Ciò indica che la nanotecnologia del rame può svolgere un ruolo importante contro i batteri e i funghi che causano infezioni umane e l'idrossido di rame (II) potrebbe essere molto utile in questi campi.
Riferimenti
- Cotone, f. Albert e Wilkinson, Geoffrey. (1980). Chimica inorganica avanzata. Quarta edizione. John Wiley & Sons.
- Kirk-Othmer (1994). Enciclopedia della tecnologia chimica. Volume 7. Quarta edizione. John Wiley & Sons.
- L'enciclopedia di chimica industriale di Ullmann. (1990). Quinta edizione. Volume A7. VCH Verlagsgellschaft MBH.
- Dance, j.C.; Emeléus, h.J.; Sir Ronald Nyholm e Trotman-Deckenson, a.F. (1973). Chimica inorganica completa. Volume 3. Pergamon Press.
- Biblioteca nazionale di medicina. (2019). Rame (ii) idrosside. Recuperato da: pubchem.NCBI.Nlm.NIH.Gov
- Schiopu, n. e tiruta-brara, l. (2012). Conservanti in legno. In tossicità dei materiali di lucidatura. Capitolo 6. Recuperato da ScienceDirect.com.
- Mordorski, b. e Friedman, a. (2017). Nanoparticelle metalliche per infezione microbica. In nanomateriali funzionalizzati per la gestione dell'infezione microbica. capitolo 4. Recuperato da ScienceDirect.com.
- Takashi Tsurumi. (1994). Soluzione che gira. In una tecnologia di filatura in fibra avanzata. capitolo 3. Recuperato da ScienceDirect.com.
- « Histochemistry Foundation, elaborazione, colorazione
- CERIO OSDIDE (IV) Struttura, proprietà, usi »

