CERIO OSDIDE (IV) Struttura, proprietà, usi

- 3650
- 264
- Benedetta Rinaldi
Lui Cerio ossido (IV) U l'ossido zagico è un solido inorganico bianco o giallo pallido che è prodotto dall'ossidazione del cerio (CE) dall'ossigeno alla sua Valencia 4+. La formula chimica dell'ossido zagico è CEO2 Ed è l'ossido più stabile della collina.
Cerio (CE) è un elemento della serie Lanthanid, che è incluso nel gruppo dei terreni RAN. La fonte naturale di questo ossido è il minerale di bastastro. Nel concentrato commerciale di questo minerale il CEO2 Può essere trovato in una proporzione approssimativa fino al 30% in peso.
 Un campione di ossido di cerio (IV). Immagine scattata agosto 2005 dall'utente: Walkerma. Pd-se stesso Fonte: Wikipedia Commons
Un campione di ossido di cerio (IV). Immagine scattata agosto 2005 dall'utente: Walkerma. Pd-se stesso Fonte: Wikipedia Commons L'amministratore delegato2 Può essere facilmente ottenuto riscaldando in aria o ossigeno da Hill (III), CE (OH)3, o qualsiasi sale di collina (III), come ossalato, carbonato o nitrato.
L'amministratore delegato2 lo stechiometrico può essere ottenuto mediante reazione ad alta temperatura dell'ossido di collina (III) con ossigeno elementare. L'ossigeno deve essere eccessivamente e abbastanza tempo per completare la conversione delle varie fasi non estochiometriche che si stanno formando deve essere lasciata abbastanza da completare.
Queste fasi comprendono prodotti CEO di formula multicoloreX (dove x varia tra 1,5 e 2,0). Sono anche chiamati CEO2-x, dove x può avere un valore fino a 0,3. L'amministratore delegato2 È la forma CE più utilizzata nel settore. Ha una classificazione a bassa tossicità, soprattutto a causa della sua scarsa solubilità in acqua.
 Campione minerale di bastastro bastardo. Rob Lavinsky, Irocks.Com-CC-BY-SA-3.0 [CC BY-SA 3.0 (https: // creativeCommons.Org/licenze/by-sa/3.0)] Fonte: Wikipedia Commons
Campione minerale di bastastro bastardo. Rob Lavinsky, Irocks.Com-CC-BY-SA-3.0 [CC BY-SA 3.0 (https: // creativeCommons.Org/licenze/by-sa/3.0)] Fonte: Wikipedia Commons [TOC]
Struttura
Cerio Ossido (IV) cristallizzato stechiometrico nella rete cubica di tipo fluorite (caffè2), con 8 ioni o2- In una struttura cubica coordinata con 4 ioni CE4+.
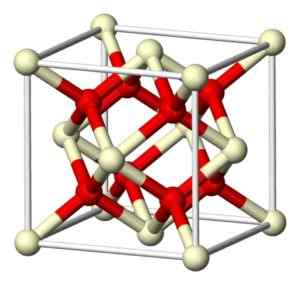 Struttura cristallina dell'ossido di collina (IV). Benjah-bmm27 [dominio pubblico] Fonte: Wikipedia Commons
Struttura cristallina dell'ossido di collina (IV). Benjah-bmm27 [dominio pubblico] Fonte: Wikipedia Commons Nomenclatura
- Cerio ossido (IV).
- Ossido zagico.
- Biossido di cerio.
- Ceria.
- Stoichiometric Hill: materiale formato completamente dal CEO2.
- Ossido di cerio non eco-etico: materiale formato da ossidi misti dal CEO2 al CEO1.5
Proprietà
Stato fisico
Solido giallo pallido. Il colore è sensibile alla stechiometria e alla presenza di altri lantanidi. Gli ossidi non statichiometrici sono spesso blu.
Durezza MOHS
Circa 6-6.1.
Peso molecolare
172,12 g/mol.
Punto di fusione
2600 ºC approssimativamente.
Densità
7.132 g/cm3
Solubilità
Insolubile in acqua fredda e calda. Solubile in acido solforico concentrato concentrato. Insolubile in acidi diluiti.
Indice di rifrazione
2.2.
Altre proprietà
L'amministratore delegato2 È una sostanza inerte, non viene attaccata da acidi forti o alcali. Tuttavia, può essere sciolto dagli acidi in presenza di agenti riducenti, come il perossido di idrogeno (H2O2) o stagno (ii), tra gli altri, generando soluzioni CERIO (iii).
Può servirti: sistema eterogeneoPresenta un'elevata stabilità termica. Non subisce cambiamenti cristallografici durante i soliti intervalli di riscaldamento.
Il suo derivato idratato (CEO2.NH2O) è un precipitato giallo e gelatinoso ottenuto durante il trattamento di soluzioni CERIO (IV) con le basi.
L'amministratore delegato2 È scarsamente assorbito dal tratto gastrointestinale, quindi non ha effetti tossici.
Applicazioni
- Nell'industria metallurgica
L'amministratore delegato2 Viene utilizzato in elettrodi di alcune tecnologie di saldatura, come la saldatura dell'arco di tungsteno con gas inerte.
L'ossido è finemente disperso in tutta la matrice di tungsteno. A basse tensioni queste particelle di CEO2 dare una maggiore affidabilità rispetto al solo tungsteno.
- Nell'industria del vetro
Lucidatura del vetro
CERIO L'ossido è l'agente di lucidatura più efficiente per la maggior parte delle composizioni di vetro commerciali. L'amministratore delegato2 ha quasi completamente sostituito altri ossidi di lucidatura, come la fede2O3, Silice e zro2, A causa della sua maggiore velocità di lucidatura e pulizia, aumentando aumentando il grado di purezza dell'ossido.
Pulimentos commerciali per vetro in base alle polveri di ossido di cerio hanno definito le dimensioni delle particelle e la dispersione controllata nei sistemi acquosi.
Il processo di lucidatura del vetro richiede acqua e ciò che viene rimosso o riforma è uno strato superficiale idratato più morbido. L'agente di lucidatura deve avere una durezza MOHS di circa 6,5, vicino alla durezza della maggior parte del vetro.
L'ossido di cerio in acqua contiene la coppia CE (IV) / EC (III) che con le loro reazioni di riduzione dell'ossido può fornire assistenza chimica durante la rottura della rete di silicato di vetro.
L'amministratore delegato2 Con un alto grado di purezza viene utilizzato per trattare specchi, elettrodomestici, lenti oftalmiche e materiale ottico di precisione.
Scolorimento del vetro
L'amministratore delegato2 può scolorire il vetro di soda-callo per bottiglie, brocche e simili. Il CE (iv) ossida le impurità della fede (ii), che forniscono colore blu verde, alla fede (iii) che conferisce un colore giallo 10 volte più debole.
Vetro resistente alle radiazioni
L'aggiunta dell'1% di CEO2 Al vetro sopprime lo scolorimento o l'oscuramento del vetro causato dal bombardamento di elettroni ad alta energia nel vetro TV. Lo stesso accade nelle finestre usate nelle cellule calde dell'industria nucleare, poiché sopprime la decolorazione indotta dai raggi gamma.
Si ritiene che il meccanismo di soppressione dipenda dalla presenza di ioni CE4+ e ce3+ Nella rete di vetro.
Può servirti: chimica nucleare: storia, campo di studio, aree, applicazioniVetro fotosensibile
Alcune formulazioni di vetro possono sviluppare immagini latenti che possono quindi essere convertite in una struttura o un colore permanenti.
Questo tipo di vetro contiene CEO2 che assorbe le radiazioni UV e rilascia elettroni nella matrice di vetro.
Attraverso il trattamento successivo viene generata la crescita di cristalli di altri composti nel vetro, creando motivi dettagliati per usi elettronici o decorativi.
- In smalti
Per il suo CEO di indice di rifrazione elevato2 È un agente di opacità nelle composizioni di smalto utilizzate come rivestimenti protettivi sui metalli.
La sua elevata stabilità termica e la sua unica forma cristallografica durante l'intero intervallo di temperatura ottenuto durante il processo dello smalto, lo rendono adeguato per l'uso negli smalti per la porcellana.
In questa applicazione il CEO2 fornisce la copertura bianca desiderata durante lo smalto bruciato. È l'ingrediente che fornisce opacità.
- In ceramica di Circonio
La ceramica di cirrium è un isolante termico e viene utilizzata in applicazioni ad alta temperatura. Richiede un additivo per avere elevata resistenza e tenacia. Aggiunta di CEO2 Un materiale di ossido di cirrium Un materiale con tenacia eccezionale e una buona resistenza si verifica.
Ossido di zirch con CEO2 È usato nei rivestimenti per fungere da barriera termica sulle superfici metalliche.
Ad esempio, nelle parti dei motori dell'aeromobile questi rivestimenti proteggono dalle alte temperature a cui sarebbero esposti i metalli.
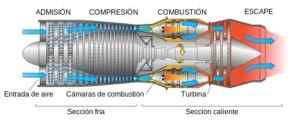 Motore a reazione. Jeff Dahl, traduzione spagnola di Xavigivax [CC BY-SA 4.0 (https: // creativeCommons.Org/licenze/by-sa/4.0)] Fonte: Wikipedia Commons
Motore a reazione. Jeff Dahl, traduzione spagnola di Xavigivax [CC BY-SA 4.0 (https: // creativeCommons.Org/licenze/by-sa/4.0)] Fonte: Wikipedia Commons - Nei catalizzatori per il controllo delle emissioni del veicolo
L'amministratore delegato2 È un componente attivo nella rimozione degli inquinanti dalle emissioni del veicolo. Ciò è in gran parte dovuto alla sua capacità di immagazzinare o rilasciare ossigeno a seconda delle condizioni che lo circondano.
Il convertitore catalitico dei veicoli automobilistici si trova tra il motore e l'uscita dei gas di scarico. Ha un catalizzatore che deve ossidare gli idrocarburi non di non frequenza, convertire co -a co co2, e ridurre gli ossidi di azoto, noX, UN2 IO2.
 Convertitore catalitico dei gas di scarico dal motore a combustione interna di un veicolo auto. Ahanix1989 presso l'inglese Wikipedia [dominio pubblico] Fonte: Wikipedia Commons
Convertitore catalitico dei gas di scarico dal motore a combustione interna di un veicolo auto. Ahanix1989 presso l'inglese Wikipedia [dominio pubblico] Fonte: Wikipedia Commons Oltre al platino e ad altri metalli catalitici, il principale componente attivo di questi sistemi multifunzionali è CEO2.
Ogni convertitore catalitico contiene 50-100 g di CEO2 finemente diviso, che svolge diverse funzioni. I più importanti sono:
Agisce come stabilizzatore di allumina di superficie alta
Alumina di superficie alta tende a sinterare, perdendo la sua superficie alta durante il funzionamento ad alte temperature. Questo è ritardato dalla presenza del CEO2.
Può servirti: dimetilanilina: struttura, proprietà, sintesi, usiSi comporta come un librador di stoccaggio di ossigeno
Per la sua capacità di formare CEO non est perchiometrico2-x, L'ossido di cerio (IV) fornisce ossigeno elementare dalla propria struttura durante il periodo del scarso ciclo di ossigeno/ricco di carburante.
Pertanto, l'ossidazione di idrocarburi non bruciati che provengono dal motore e la conversione di CO può continuare2, anche quando l'ossigeno a gas è insufficiente.
Quindi, nel periodo del ciclo ricco di ossigeno, occupa di nuovo ossigeno e ossidato, recuperando la sua forma stechiometrica del CEO2.
Altri
Funziona come un improprio della capacità catalitica della cavalcata nella riduzione degli ossidi di azoto non lo faX Azoto e ossigeno.
- Sulle reazioni chimiche
Nei processi di cracking catalitico delle raffinerie il CEO2 Agisce come un ossidante catalitico che aiuta nella conversione di così2 Per così3 e promuove la formazione di solfato in trappole di processo specifiche.
L'amministratore delegato2 Migliora l'attività del catalizzatore in base all'ossido di ferro utilizzato per ottenere il tratto a partire dall'etilbenzene. Ciò è probabilmente dovuto all'interazione positiva tra coppie di ossido -riduzione (II) - Fe (III) e CE (III) - CE (IV).
- In applicazioni biologiche e biomediche
È stato scoperto che le nanoparticelle del CEO2 Agiscono eliminando i radicali liberi, come superossido, idrogeno, idrossile e ossido nitrico radicale.
Possono proteggere i tessuti biologici da danni indotti dalle radiazioni, danni alla retina indotti dal laser, aumentare la fascia di vita delle cellule dei fotorecettori, ridurre le lesioni spinali, ridurre l'infiammazione cronica e promuovere l'angiogenesi o la formazione dei vasi sanguigni.
Inoltre, alcune nanofibre contenenti nanoparticelle CEO2 Si sono dimostrati tossici contro i ceppi batterici, essendo candidati promettenti per applicazioni battericide.
- Altri usi
L'amministratore delegato2 È un materiale isolante elettrico grazie alla sua eccellente stabilità chimica, ad alta quota relativa (ha un'alta tendenza a polarizzarsi prima dell'applicazione di un campo elettrico) e una rete cristallina simile al silicio.
Ha trovato l'applicazione nel condensatore e strati di ammortizzazione di materiali superconduttori.
Viene anche utilizzato in sensori di gas, materiali per elettrodi a celle a combustibile a ossido solido, pompe di ossigeno e monitor di ossigeno.
Riferimenti
- Cotone, f. Albert e Wilkinson, Geoffrey. (1980). Chimica inorganica avanzata. Quarta edizione. John Wiley & Sons.
- Dance, j.C.; Emeléus, h.J.; Sir Ronald Nyholm e Trotman-Deckenson, a.F. (1973). Chimica inorganica completa. Volume 4. Pergamon Press.
- Kirk-Othmer (1994). Enciclopedia della tecnologia chimica. Volume 5. Quarta edizione. John Wiley & Sons.
- L'enciclopedia di chimica industriale di Ullmann. (1990). Quinta edizione. Volume A6. VCH Verlagsgellschaft MBH.
- Casals, Eudald et al. (2012). Analisi e rischio di nanomateriali in campioni ambientali e alimentari. Nella comprensione della chimica analitica. Recuperato da ScienceDirect.com.
- MailAdil t. Sebastian. (2008). Aluminia, Titania, Ceria, silicato, Tungstate e altri materiali. In materiali dielettrici per la comunicazione wireless. Recuperato da ScienceDirect.com.
- Afeesh Rajan Unnithan, et al. (2015). Impalcature con proprietà antibatteriche. In nanotecnologie applicazioni per l'ingegneria dei tessuti. Recuperato da ScienceDirect.com.
- Gottardi V., et al. (1979). Lucidare la superficie di un bicchiere studiata con una tecnica nucleare. Bollettino della Ceramica spagnola e della Glass Society, Vol. 18, n. 3. Recuperato dai bollettini.Secv.È.
- « Struttura di idrossido di rame (ii), proprietà, nomenclatura, usi
- Equazione del direttore vettoriale della linea, esercizi risolti »

