Struttura, usi, ottimo, proprietà, proprietà, proprietà, ottimo

- 4371
- 711
- Benedetta Rinaldi
Lui biossido di cloro È un composto inorganico formato dall'elemento di cloro (CL) e ossigeno (O). La sua formula chimica è CLO2. È un gas giallo verdastro a rossastro. Non si trova naturalmente nell'ambiente.
È estremamente reattivo, quindi è comune essere preparato nel luogo in cui verrà utilizzato. Uno dei suoi usi più importanti è come microbicida, antisettico e deodorante perché elimina i batteri, i virus e i funghi molto facilmente e in concentrazioni molto basse.
 Alcuni alimenti venduti nei supermercati potrebbero essere stati disinfettati con il biossido di cloro CLO2. Autore: ElasticComputefarm. Fonte: Pixabay.
Alcuni alimenti venduti nei supermercati potrebbero essere stati disinfettati con il biossido di cloro CLO2. Autore: ElasticComputefarm. Fonte: Pixabay. Permette di disinfettare cibi come verdure, frutta, carni, uccelli e frutti di mare. Serve per ignitire superfici, pavimenti, bagni, sistemi di ventilazione, piscine, attrezzature da laboratorio, attrezzature per dentista, ecc.
Pertanto, viene utilizzato nella lavorazione degli alimenti, negli ospedali e nelle cliniche, nei settori e nei negozi. Viene utilizzato per purificare l'acqua usata per bere e anche le acque reflue municipali.
È molto efficace come agente ossidante, quindi viene utilizzato per sbiancare la polpa di carta, gli oli, la farina, la pelle, le fibre tessili, tra gli altri.
Quando è sotto forma di gas è molto pericoloso, in quanto è molto esplosivo ed è utilizzato principalmente in soluzioni acquose. È tossico se è inalante.
[TOC]
Struttura
Il biossido di cloro è formato dall'unione di un atomo di cloro (CL) con due atomi di ossigeno (O). I collegamenti di cloro con ogni ossigeno sono covalenti e doppi. Il cloro in questo composto ha una valenza di +4.
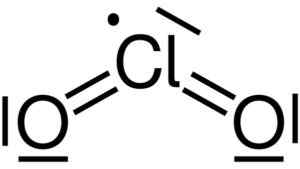 Struttura di lewis di biossido di cloro2. Yikrazuul [dominio pubblico]. Fonte: Wikimedia Commons.
Struttura di lewis di biossido di cloro2. Yikrazuul [dominio pubblico]. Fonte: Wikimedia Commons. Ha una struttura simmetrica e ad angolo, perché ha elettroni liberi. Cioè, non formano un collegamento con nessun altro atomo.
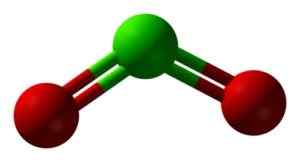 Struttura CLO2 in tre dimensioni. Verde = cloro; Rosso = ossigeno. Ben Mills e Jynto [dominio pubblico]. Fonte: Wikimedia Commons.
Struttura CLO2 in tre dimensioni. Verde = cloro; Rosso = ossigeno. Ben Mills e Jynto [dominio pubblico]. Fonte: Wikimedia Commons. Nomenclatura
- Biossido di cloro
- Ossido di cloro (IV)
Proprietà
Stato fisico
Giallo verdastro a giallo rossastro.
Peso molecolare
67,45 g/mol.
Punto di fusione
-59 ºC.
Punto di ebollizione
11 ºC.
Densità
Liquido a 0 ° C = 1.642 g/cm3
Gas = 2,33 (densità relativa dell'aria, aria = 1).
Può servirti: alcol isoamilico: struttura, proprietà, usi e rischiSolubilità
Solubile in acqua: 2000 cm3 del CLO2 gas a 100 cm3 di acqua fredda o 0,8 g/100 ml di acqua a 20 ° C. Solubile in soluzione alcalina e nella soluzione di acido solforico h2SW4.
Proprietà chimiche
Il clo2 È estremamente reattivo e può sfruttare violentemente. È un agente ossidante molto efficace.
Il clo2 Si rompe violentemente se viene a contatto con materiali organici. Se sei in aria ad una concentrazione superiore al 10%, può esplodere a causa della luce solare o del calore.
Puoi anche far esplodere in presenza di mercurio (Hg) o monossido di carbonio (CO).
Sotto l'azione di ultravioletto (UV) o ozono il CLO2 Diventa esossido di cloro2O6, composto molto instabile.
Proprietà delle soluzioni acquose
Le sue soluzioni acquose sono gialle o rossastre. Sono stabili se rimangono freddi, ben sigillati e protetti dalla luce solare. In presenza di luce queste soluzioni vengono lentamente scomposte per dare acido cloridrico HCl e acido clorico HCLO3.
 Soluzione d'acqua di CLO2 dove si osserva che viene rilasciato un gas giallo che è il CLO2. Autore: Materialscient. Fonte: Wikimedia Commons.
Soluzione d'acqua di CLO2 dove si osserva che viene rilasciato un gas giallo che è il CLO2. Autore: Materialscient. Fonte: Wikimedia Commons. Nelle soluzioni alcaline il clo2 È suddiviso in ioni clorito clo2- e clorato3-. In soluzioni acide, l'acido cloro forma HCLO2 E poi questo è suddiviso in acido cloridrico HCl e acido clorico HCLO3.
Altre proprietà
I vapori concentrati di CLO2 Sono potenzialmente esplosivi, quindi non è stato possibile comprimere né mescolato solo con altri gas. Per questo motivo si preferisce prepararlo nel sito dove verrà utilizzato.
Quando sono temperature molto basse nella sua forma idratata, che è il modo in cui viene talvolta trasferito, è solido sotto forma di un blocco di ghiaccio e arancione.
Ha un odore simile al cloro. È tossico per inalazione.
Ottenimento
Può essere ottenuto in diversi modi. Ad esempio, in alcuni casi le soluzioni CLO2 Si preparano a passare una miscela di gas di cloro (CL2) e aria (o cloro e gas azoto2) attraverso una colonna che contiene granuli di clorito di sodio (Naclo2).
Può servirti: layer Valencia2 Naclo2 + Cl2 → 2 NaCl + 2 CLO2
Il prodotto generato contiene circa il 90% di CLO2, Tra gli altri composti di cloro.
È anche ottenuto dal clorato di potassio (KCLO3) e acido solforico (H2SW4) In presenza di acido ossalico come riduttore. In questo caso, si forma anche l'anidride carbonica (CO2) che serve a diluire il CLO2.
Può essere preparato nel sito di utilizzo in base al clorato di sodio (NaClo3), acido solforico (H2SW4) e metanolo (scegli3OH).
Nel settore è ottenuto dal clorato di sodio (Naclo3) e biossido di zolfo (SO2) In presenza di acido solforico.
2 Naclo3 + SW2 + H2SW4 → 2 CLO2 + 2 Nahso4
Usa come disinfettante
Può essere usato come potente agente antimicrobico. È stato scoperto che è altamente efficace contro diversi microrganismi, come Escherichia coli e il Staphylococcus aureus.
Con quest'ultimo, una concentrazione di soli 5 ppm di CLO2 per eliminarne il 100%. È battericida, antisettico e deodorante. È efficace su un ampio intervallo di pH.
Nel cibo
Viene usato come agente antimicrobico in acqua per fumigare frutta e verdura, nella lavorazione di uccelli di uccelli, carni rosse, sia pezzi di carne e organi e prodotti marini e frutti di mare.
 La carne rossa dei supermercati potrebbe essere stata trattata con biossido di cloro per disinfettarli. Autore: Karamo. Fonte: Pixabay.
La carne rossa dei supermercati potrebbe essere stata trattata con biossido di cloro per disinfettarli. Autore: Karamo. Fonte: Pixabay. Le soluzioni di biossido di cloro devono essere utilizzate in una concentrazione che non supera i 3 ppm (parti per milione) di CLO2 residuo, in modo che non abbia un effetto sul cibo.
Dopo il trattamento con CLO2 Tutti gli alimenti devono essere governati completamente con acqua potabile o devono essere usati come scottati, cucina o in scatola.
Nel caso dei prodotti marini la soluzione fognaria2 Dovrebbe essere usato nell'acqua e nel ghiaccio che vengono utilizzati nel risciacquo, nel lavaggio, nello scongelamento, nel trasporto o nello stoccaggio. I frutti di mare grezzi devono quindi essere lavati molto bene con acqua potabile prima del consumo.
 Acqua fredda e ghiaccio con cui i frutti marini contengono piccole quantità di CLO2. Autore: partecipazioni di dominio pubblico. Fonte: Pixabay.
Acqua fredda e ghiaccio con cui i frutti marini contengono piccole quantità di CLO2. Autore: partecipazioni di dominio pubblico. Fonte: Pixabay. Su carta e cartone che verranno a contatto con il cibo
Soluzioni CLO2 Sono usati per eliminare i microrganismi che causano slim (come alghe, batteri e funghi) nell'acqua di processo utilizzata nella produzione di carta e cartone che entreranno in contatto con alimenti.
Può servirti: molecole apolariIn acqua potabile
Serve a purificare l'acqua e renderla bevibile (sicuro da bere). È usato nel pretrattamento dell'acqua che verrà quindi imbottigliato per bere o acqua che verrà utilizzato come ingrediente nella produzione di bevande o bevande analcoliche.
 Alcune bevande analcoliche trasformate possono contenere acqua trattata con CLO2. Susan Slater [CC BY-SA (https: // creativeCommons.Org/licenze/by-sa/4.0)]. Fonte: Wikimedia Commons.
Alcune bevande analcoliche trasformate possono contenere acqua trattata con CLO2. Susan Slater [CC BY-SA (https: // creativeCommons.Org/licenze/by-sa/4.0)]. Fonte: Wikimedia Commons. In odontoiatria
È usato negli strumenti utilizzati dal dentista o dal dentista per disinfettarli e distruggere gli organismi patogeni in essi.
In applicazioni mediche
Le soluzioni acquose di clo2 Sono stati usati per trattare la candidosi orale (infezione da bocca). La candidosi è un'infezione da funghi Candida albicans.
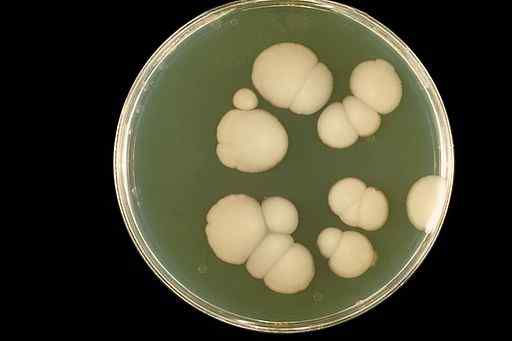 Candida albicans Fungo Apparenza in un raccolto di laboratorio. CDC/DR. William Kaplan [dominio pubblico]. Fonte: Wikimedia Commons.
Candida albicans Fungo Apparenza in un raccolto di laboratorio. CDC/DR. William Kaplan [dominio pubblico]. Fonte: Wikimedia Commons. Il biossido di cloro elimina la bocca dalla bocca e migliora significativamente la comparsa di tessuti orali senza effetti collaterali.
Alcuni ricercatori medici indicano che le soluzioni CLO2 Applicati alle ferite delle operazioni chirurgiche, possono ridurre o sopprimere la formazione di accessioni senza influire sulla cura della stessa, con il vantaggio aggiuntivo delle sue proprietà antisettiche.
Altri usi
Per le sue proprietà ossidanti e microbicide il CLO2 è usato per:
- Sbiancare la cellulosa del legno nella produzione di polpa e carta, fornendo una lucentezza stabile.
- Decorare grassi e oli, pelle, farina sbiancante e tessuti.
- Applicazioni agricole come la disinfezione di superfici dure, attrezzature, sistemi idrici e serre di funghi.
- Applicazioni in settori, negozi e ospedali come la disinfezione di superfici dure (pareti, pavimenti, bagni), sistemi di ventilazione, attrezzature di laboratorio.
- Disinfettare appartamenti e bagni di famiglie, sistemi di aria condizionata, sistemi di circolazione delle acque del nuoto.
- Il trattamento delle acque reflue municipali e industriali.
- Pulizia dell'inquinamento di giacimenti petroliferi.
- Produzione di sali di cloruro (CL-).
Rischi
- I vapori concentrati di CLO2 Sono potenzialmente esplosivi.
- È tossico per inalazione e ingestione. È irritante occhio, naso e gola, può causare edema polmonare e bronchite cronica.
- Secondo le fonti hanno consultato il CLO2 non causa mutazioni del DNA né causa il cancro nell'uomo.
Riferimenti
- O.S. Biblioteca nazionale di medicina. (2019). Biossido di cloro. Recuperato da Pubchem.NCBI.Nlm.NIH.Gov.
- Dean, J.A. (editore). (1973). Lange's Handbook of Chemistry (undicesimo edizione). McGraw-Hill Book Company.
- L'enciclopedia di chimica industriale di Ullmann. (1990). Quinta edizione. VCH Verlagsgellschaft MBH.
- Cotone, f. Albert e Wilkinson, Geoffrey. (1980). Chimica inorganica avanzata. Quarta edizione. John Wiley & Sons.
- Bajpai, p. (2012). Bleaching di biossido di cloro. Effetto del biossido di cloro sbiancante sulla qualità della polpa. In approcci ecologici benigni per la candelazione polpa (seconda edizione). Recuperato da ScienceDirect.com.
- Moran, s. (2018). Chimica dell'acqua. Biossido di cloro. In una guida applicata all'acqua e alla progettazione dell'impianto di trattamento dell'effluente. Recuperato da ScienceDirect.com.
- McKen, l. (2012). Introduzione a FoodRadition and Medical Sterilization. Chorine gassoso Diexide. Nell'effetto della sterilizzazione su materie plastiche ed elastomeri (terza edizione). Recuperato da ScienceDirect.com.
- « Caratteristiche paleolitiche superiori, arte, organizzazione sociale
- Struttura dell'acido solfonico, nomenclatura, proprietà, usi »

