Reazione di spostamento

- 2146
- 354
- Silvano Montanari
Spieghiamo quali sono le reazioni di spostamento, i tipi che esistono e danno diversi esempi
 La reazione tra rame metallico e soluzione di nitrato d'argento è una reazione di spostamento che produce nitrato di rame (II) (che dà alla soluzione una colorazione blu verdastra) e argento metallico che cresce sotto forma di un grigio argento di fluff di colore
La reazione tra rame metallico e soluzione di nitrato d'argento è una reazione di spostamento che produce nitrato di rame (II) (che dà alla soluzione una colorazione blu verdastra) e argento metallico che cresce sotto forma di un grigio argento di fluff di colore Cos'è una reazione di spostamento?
IL Reazione di spostamento o La reazione di sostituzione è un tipo di reazione chimica in cui un atomo o un piccolo gruppo di atomi in una molecola viene sostituito o spostato da un altro atomo o gruppo di atomi.
Le reazioni di spostamento possono essere semplici o doppie e sono molto comuni in natura. Molte delle reazioni chimiche che vediamo quotidianamente sono reazioni di spostamento, come la solfatazione dei terminali nelle batterie per auto.
Tipi di reazioni di spostamento
Esistono due tipi di reazioni di spostamento, semplici e doppie, che sono descritte di seguito insieme ad alcuni esempi specifici:
Reazione di spostamento semplice
Queste sono reazioni di spostamento in cui un elemento sostituisce un altro in un composto chimico. Sono riconosciuti perché sia nei reagenti che nei prodotti ci sono solo due sostanze coinvolte, e in ogni caso una di esse è un elemento puro mentre l'altro è un composto.
Queste reazioni possono avere una delle seguenti equazioni generali:
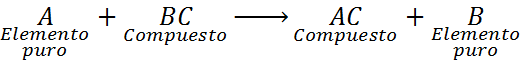
Come si può vedere, in questa reazione l'elemento A reagisce con il composto BC e sposta o sostituisce l'elemento B per formare il composto CA.
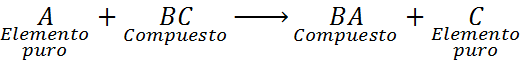
In questo caso, l'elemento A reagisce anche con il composto BC, ma sposta o sostituisce l'elemento C per formare il composto BA, rilasciando C sotto forma di un elemento puro.
Una delle caratteristiche più importanti per riconoscere una semplice reazione di spostamento è che l'elemento in arrivo deve finire per occupare lo stesso posto che occupava l'elemento in uscita (B o C, a seconda dei casi) e questo deve terminare come un elemento puro.
Può servirti: Arseniuro di gallio: struttura, proprietà, usi, rischioVa notato che, in molti casi, la parte C della molecola non è necessariamente un elemento individuale, ma che può essere un gruppo di atomi come ioni nitrati (no3-) o solfato (così4-).
Esempi di semplici reazioni di spostamento
- Spostamento d'argento di rame
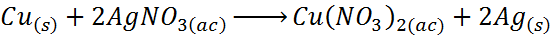
In questo caso, il rame (Cu) agisce per l'elemento A, argento (Ag) corrisponde agli ioni dell'elemento B e ai nitrati (NO3-) Rappresenta c.
Come puoi vedere, in questa reazione, il rame sostituisce l'argento in nitrato d'argento, rilasciando l'argento in modo elementare.
- Solfazione dei terminali della batteria

Questa semplice reazione di spostamento è ciò che accade nei terminali o nei contatti elettrici di molti accumulatori di piombo, ovvero le batterie presenti nella maggior parte delle auto a benzina.
La reazione è evidenziata dalla formazione di un solido bianco che copre i contatti di piombo di queste batterie. Come si può vedere nell'equazione, questa è una reazione in cui il piombo sposta l'idrogeno nell'acido solforico.
- Spostamento del bromo per fluoro

In questo caso, il fluoro, che è un elemento molto reattivo, sostituisce il bromo nel bromuro di sodio (NABR) per formare il fluoro di sodio (NAF). Si noti che qui l'elemento che viene sostituito non è quello che appare per primo nella formula composta, ma che è la seconda, come nella seconda forma della reazione generale precedentemente mostrata.
Può servirti: distillazione frazionaria: processo, attrezzatura, applicazioni, esempiReazione a doppia spostamento
Le reazioni a doppia spostamento, chiamate anche doppie reazioni di sostituzione o doppia decomposizione, possono essere viste come uno scambio di coppie. Queste sono reazioni in cui due diversi composti chimici si scambiano elementi per formare due diversi nuovi composti. Queste reazioni hanno la seguente equazione generale:
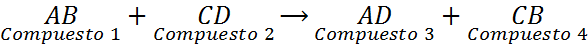
Come si può vedere in questa reazione generale, l'elemento A del composto 1 (AB) sostituisce l'elemento composto 2 (CD) per formare il composto 3 (AD). Allo stesso tempo, l'elemento C del composto 2 (CD) sostituisce l'elemento A del composto 1 (AB) per formare il composto 4 (CB).
Nei doppi spostamenti è essenziale che gli elementi che vengono sostituiti tra loro occupano posizioni equivalenti nei nuovi composti. Ciò significa che, nella reazione generale, a, che è a sinistra e quindi è probabilmente un catione, può sostituire solo C nel composto CD, ma non può sostituire D.
Questo è simile a uno scambio di coppie di danza. Se tutte le coppie sono formate da un uomo e una donna, le nuove coppie si sono formate dopo la reazione devono essere formate anche da un uomo e da una donna.
Esempi di reazioni a doppia spostamento
- Reazione tra cloruro di sodio e nitrato d'argento

Questo è un chiaro esempio di reazione a doppia spostamento. Qui, il sodio sostituisce l'argento in nitrato d'argento per formare nitrato di sodio (nano3), Allo stesso tempo che l'argento sostituisce il sodio nel cloruro di sodio per formare cloruro d'argento (AGCL).
Può servirti: epide- Reazione tra solfato di calcio e cloruro di sodio

In questa reazione a doppia spostamento, il calcio sostituisce il sodio nel cloruro di sodio per formare il cloruro di calcio mentre il sodio sostituisce il calcio nel solfato di calcio per formare solfato di sodio così.
Un altro modo per vedere questa reazione ugualmente valida è che il solfato sta sostituendo il cloruro nel cloruro di sodio per formare solfato di sodio mentre il cloruro sta sostituendo il solfato.
Sebbene entrambe le forme siano ugualmente accettabili, il primo è più comune del secondo.
- Reazione tra acido solforico e idrossido di potassio
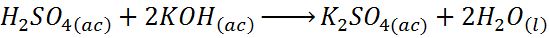
La reazione tra acido solforico e idrossido di potassio è una reazione di neutralizzazione basata sull'acido di base, ma è anche una reazione a doppia spostamento.
In questo caso, l'idrogeno sta sostituendo il potassio nell'idrossido di potassio per formare acqua, mentre il potassio sostituisce l'idrogeno nell'acido solforico per formare solfato di potassio.

