Modello atomico Dalton

- 1949
- 565
- Silvano Montanari
Spieghiamo il modello atomico di Dalton, i suoi postulati e le sue limitazioni
 Il modello atomico di Dalton è stato il primo a essere basato sulla ricerca scientifica. Fonte: f. Zapata.
Il modello atomico di Dalton è stato il primo a essere basato sulla ricerca scientifica. Fonte: f. Zapata. Qual è il modello atomico di Dalton?
Lui Modello atomico Dalton Propone che tutta la materia sia composta da piccole e indivisibili unità, chiamate atomi, recuperando così le idee che gli ex pensatori greci avevano formulato duemila anni fa.
È il primo modello atomico emerso da un'attenta sperimentazione in laboratorio, perché sebbene l'umanità abbia sempre cercato di capire qual è la materia, fino all'inizio del diciannovesimo secolo, le possibilità di verificare sperimentalmente le teorie erano ancora limitate.
Tuttavia, oltre ad essere un buon osservatore della natura, anche l'insegnante di inglese John Dalton (1766-1844), si distingueva anche nel campo della strumentazione, perché ha creato diversi dispositivi di misurazione, che in seguito avrebbe usato nel suo laboratorio per lo studio dello studio del gas.
Pertanto, Dalton si rese conto che le sostanze sono combinate seguendo determinate regole e, per spiegarlo, ha postulato che tutta la materia era composta da atomi, piccole sfere omogenee e prive di struttura interna. Gli atomi, ha detto, formano composti seguendo alcune proporzioni e durante una reazione chimica, si separano e si combinano di nuovo, creando nuovi composti.
Dalton non solo ha sviluppato il primo modello atomico basato sulla sperimentazione rigorosa. Ha anche creato un sistema di nomenclatura per gli elementi, li ha ordinati per il loro peso atomico, ha stabilito la legge di molteplici proporzioni, la legge delle pressioni parziali e ha descritto la cecità a determinati colori, una condizione che lui stesso ha sofferto, chiamata lui stesso daltonismo.
Il suo ampio contributo alla scienza ha guadagnato numerose distinzioni durante la sua carriera scientifica, ma Dalton ha sempre vissuto in modo modesto e semplice, dedicato alla scienza fino alla fine dei suoi giorni.
Breve storia
Sin dai tempi remoti, l'umanità ha cercato una spiegazione sulla natura della materia. Pensatori greci del V secolo.C, e prima loro, alcuni filosofi indù, postulavano che la questione fosse costituita da unità elementari chiamate atomi. Tuttavia, mancavano del necessario supporto sperimentale per verificare le loro teorie.
Può servirti: quali sono le proprietà termiche e cosa sono? (Con esempi)Il primo modello atomico è attribuito a Leucipo e al suo discepolo di Abdera (460. C. - 370 a. C.). Dal primo poco è noto, ma Democrito era un saggio di grande famoso, paragonabile a Platone e Aristotele, sebbene alcuni frammenti del suo lavoro siano appena conservati.
Democrito ha concepito l'atomo come l'ultima particella che forma la questione, indivisibile e indistruttibile. Secondo le loro teorie, tutta la materia era composta da queste particelle, troppo piccola per essere vista. E secondo il modo di combinare, gli atomi hanno fornito al soggetto le loro proprietà caratteristiche.
Contrariamente a questo, dopo aver commentato. Le idee continue di Aristotele hanno finalmente prevalso fino all'inizio del XIX secolo.
Le opere di Dalton
Nel 1793, John Dalton era interessato alla meteorologia e continuò a lavorare nello studio dei gas atmosferici e delle loro proprietà. Grazie ai suoi esperimenti, si rese conto che elementi come l'ossigeno, sempre combinati in una certa proporzione, dati da un numero intero.
Nel 1803, Dalton spiegò che queste proporzioni sono dovute al fatto che la questione è composta da particelle di base, chiamate atomi, come ha detto Democrit molto tempo fa. Ha presentato la sua proposta nel lavoro "Nuovo sistema di filosofia chimica", in cui ha descritto i risultati dei suoi esperimenti.
Inoltre, in quel lavoro includeva anche simboli speciali per rappresentare i singoli atomi di ciascun elemento, gettando così le basi della chimica moderna.
Può servirti: suoni acuti: caratteristiche ed esempiSpiegazione del modello atomico Dalton
Durante il periodo in cui Dalton sviluppò il suo lavoro, altri scienziati avevano già scoperto alcune delle leggi che governano l'argomento e le combinazioni tra gli elementi: Antoine Lavoisier affermava che, durante una reazione chimica, la massa non viene creata o distrutta, ma che diventa.
Questa legge è stata seguita dalla legge di Proust sulle proporzioni definite, stabilendo che, quando sono combinati due elementi, lo fanno sempre in proporzioni fisse.
Ora, una parte degli esperimenti di Dalton consisteva nello studio dell'assorbimento dell'acqua in acqua. Lì osservò che un certo volume d'acqua poteva assorbire solo una certa quantità di gas e che tale quantità variava in base al gas. Inoltre, il gas potrebbe essere recuperato dall'acqua, mantenendo intatte le sue proprietà.
Aveva anche scoperto che quando due elementi possono essere combinati per avere origine più di un composto, la quantità di ciascuno rimane fissa e mantenendo una semplice relazione numerica, ad esempio 1: 1, 1: 2; 2: 3 e così via. Questa è la chiamata Legge di molteplici proporzioni.
Per spiegare questi fatti, Dalton ha sostenuto che il gas, l'acqua e in generale, tutta la materia, è costituita da pezzi di base che, se combinati, danno origine a diversi composti. Ogni elemento è costituito da particelle distintive (Dalton non li chiamava atomi all'inizio), ma anche in combinazione, tali particelle mantengono le loro qualità inalterate.
Il modello atomico di Dalton postula
Il modello atomico di Dalton è riassunto nelle seguenti affermazioni:
1. La materia è costituita da piccole particelle indivisibili chiamate atomi.
2. Ogni elemento è costituito da atomi identici tra loro e con proprietà uguali. Gli atomi di un elemento differiscono da quelli degli altri.
3. Unendo due o più atomi di diversi elementi, lo fanno in determinate e semplici proporzioni, creando così i composti, formati da molecole. Le molecole di un determinato composto sono identiche tra loro.
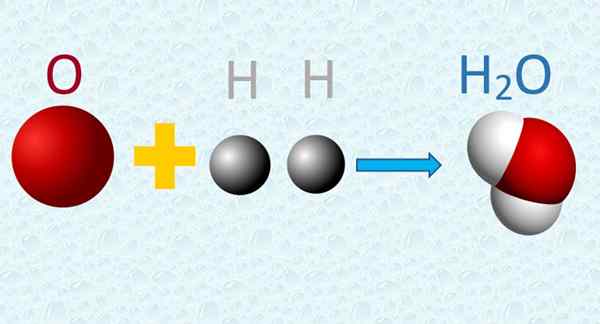 In una molecola d'acqua, gli atomi di ossigeno e idrogeno sono combinati in proporzioni semplici. Fonte: f. Zapata.
In una molecola d'acqua, gli atomi di ossigeno e idrogeno sono combinati in proporzioni semplici. Fonte: f. Zapata. 4. Durante una reazione chimica gli atomi di reazione vengono scambiati, ma non subiscono alcuna trasformazione, né sono creati o distrutti nel processo.
Fallimenti del modello Dalton
La ricerca scientifica ha sperimentato un boom notevole durante il diciannovesimo secolo, promosso dalla rivoluzione industriale. E i principali fallimenti del modello atomico di Dalton non sono stati rivelati:
Può servirti: tensione interfacciale: definizione, equazione, unità e misurazione1. L'atomo non è indivisibile
Questo è uno dei fallimenti più importanti del modello atomico di Dalton. Gli esperimenti condotti durante il diciannovesimo e il ventesimo secolo hanno mostrato che l'atomo è costituito da una moltitudine di particelle subatomiche.
I primi a conoscersi furono l'elettrone e il protone, e in seguito fu appreso sull'esistenza del neutrone. Quindi, sia il protone che il neutrone hanno rivelato la sua struttura interna.
2. Gli atomi dello stesso elemento potrebbero non essere identici
Gli elementi hanno isotopi che, sebbene abbiano le stesse proprietà chimiche, differiscono nel numero di neutroni, quindi il loro peso atomico è diverso. Ad esempio, gli isotopi di idrogeno sono Protio, Deuterio e Trizio.
3. Gli atomi non sono invariabili
Ci sono sostanze radioattive che emettono particelle ed energia, trasformandosi in altri elementi.
4. Gli atomi non sempre si combinano in intere proporzioni
È dimostrato che ci sono composti organici e più complessi, che non seguono esattamente la legge di Dalton di più proporzioni.
Articoli di interesse
Modello atomico di Schrödinger.
Broglie Atomic Model.
Modello atomico di Chadwick.
Modello atomico Heisenberg.
Modello atomico Perrin.
Modello atomico Thomson.
Modello atomico di Dirac Jordan.
Modello atomico di Democrito.
Modello atomico Leucipo.
Modello atomico Bohr.
Modello atomico Rutherford.
Modello atomico attuale.

