Linfociti T citotossici, struttura, funzioni
- 3369
- 427
- Brigitta Ferrari
IL Linfociti T citotossici, Linfociti T citolitici, cellule T citotossiche o cellule T omicidi (CTL, inglese Linfociti T citotossici), sono uno dei gruppi di cellule che partecipano alle risposte cellulari specifiche nell'uomo e in altri organismi multicellulari.
Queste cellule, descritte in base alla loro capacità di mediare l'immunità cellulare, sono state descritte dai Govaerts nel 1960 e, anni dopo, diversi gruppi di ricercatori hanno approfondito la conoscenza dei loro meccanismi di azione e le loro caratteristiche più distintive.
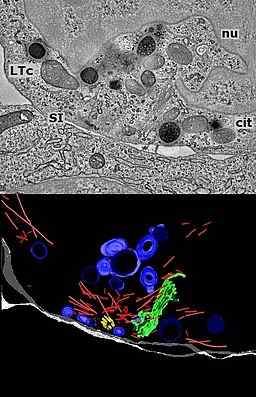
 Sinapsi immunitaria tra un linfocita T citotossico (LTC) e il suo cellulare bianco (Stephen Fuller Source, Endre Marovits, Gillian Griffiths, Jane Stinchcombe, Giovanna Bossi [CC da 3.0 (https: // creativeCommons.Org/licenze/di/3.0)] via Wikimedia Commons)
Sinapsi immunitaria tra un linfocita T citotossico (LTC) e il suo cellulare bianco (Stephen Fuller Source, Endre Marovits, Gillian Griffiths, Jane Stinchcombe, Giovanna Bossi [CC da 3.0 (https: // creativeCommons.Org/licenze/di/3.0)] via Wikimedia Commons) L'immunità cellulare, in generale, è mediata da linfociti T e fagociti, che lavorano insieme per l'eliminazione o il controllo di strani microrganismi invasori intracellulari, come virus e alcuni batteri e parassiti, inducendo la morte di cellule infette.
Come è vero per i meccanismi di risposta immunitaria umorale (mediati dai linfociti B), la risposta immunitaria cellulare può essere divisa in tre fasi note come fase di riconoscimento, fase di attivazione e fase effettrice.
La fase di riconoscimento consiste nell'unione di strani antigeni a specifici linfociti T differenziati che esprimono recettori in grado di riconoscere piccoli sequenze di peptidi in strani antigeni di origine proteica, presentati nel contesto delle proteine del maggiore complesso di istocompatibilità.
Quando si verifica il contatto con antigene-linfociti, i linfociti T si moltiplicano (proliferati) e possono successivamente differenziarsi in un altro tipo di cellula in grado di attivare i fagociti che uccidono i microrganismi intracellulari o possono lisar le cellule prodotte prodotte da strani antigeni.
Questa è la fase di attivazione e di solito merita la partecipazione di cellule collaborative o accessori. Infine, la fase effettore implica lo sviluppo delle funzioni specifiche dei linfociti attivati che si terminano con l'eliminazione degli antigeni e, a questo punto, i linfociti sono noti come "cellule effettrici".
[TOC]
Caratteristiche e struttura
I due tipi di linfociti esistenti hanno un diametro approssimativo di 8-10 μm e un nucleo di grandi dimensioni che contiene eterocromatina densamente confezionata. Nella sottile porzione di citosol che possiedono sono mitocondri, ribosomi e lisosomi.
I linfociti mancano di organelli specializzati all'interno e, così come il resto delle cellule del sangue, hanno la loro origine nel midollo osseo.
Una volta prodotti, i linfociti T migrano e vanno verso il timo (da cui l'origine del loro nome), dove vengono successivamente attivati e completano la loro differenziazione (maturi).
Può servirti: eccitabilità cellulareQueste cellule non producono anticorpi o riconoscono antigeni solubili, ma si specializzano nel riconoscimento degli antigeni peptidici attaccati alle proteine codificate dai geni del principale complesso di istocompatibilità (MHC, inglese Complesso maggiore di istocompatibilità) che sono espressi sulla superficie di altre cellule.
Queste cellule sono conosciute come antigeni o cellule che presentano APC (inglese Cellule di presentazione dell'antigene).
I linfociti T sono divisi in due tipi: collaboratori di linfociti T e linfociti citotossici o citolitici.
Collaboratori di linfociti T
I linfociti T collaboranti secernono citochine, ormoni peptidici in grado di promuovere la proliferazione e la differenziazione di altre cellule e nuovi linfociti (T e B) e per attirare e attivare leucociti infiammatori come i macrofagi e i granofagi.
Differiscono dai linfociti T citotossici per l'espressione di una specifica glicoproteina di superficie chiamata "gruppo di differenziazione 4" o CD4 (dall'inglese Cluster di differenziazione 4).
Linfociti T citotossici
I linfociti T titossici sono in grado di lisar le cellule che si esprimono sulla loro superficie strane antigeni a causa della presenza di microrganismi o di patogeni intracellulari invasori.
Sono identificati dall'espressione del marcatore di superficie della glicoproteina CD8 (dall'inglese Cluster di differenziazione 8).
Funzioni
I linfociti T citoletici partecipano al recupero dopo infezioni di origine virale, parassita e batterica. Sono anche responsabili delle risposte al rifiuto degli innesti da altri pazienti e hanno un ruolo importante nello sviluppo dell'immunità contro i tumori.
La sua funzione principale, come menzionato in precedenza, è la regolazione delle risposte immunitarie contro gli antigeni proteici, oltre a servire come cellule collaborative nell'eliminazione dei microrganismi intracellulari.
Meccanismo di azione
I linfociti T esercitano le loro funzioni grazie al fatto che alcuni agenti patogeni invasori valgono il macchinario cellulare delle cellule che infettano per moltiplicare o sopravvivere. Questi, una volta raggiunti l'interno cellulare, non sono accessibili agli anticorpi umorali, quindi l'unico modo per eliminarli è eliminare la cellula che li ospita.
I linfociti T civilitici svolgono tre funzioni che consentono loro di "uccidere" o eliminare le cellule maligne o infette che sono i loro bianchi:
1- citochine segrete come TNF-α (fattore di necrosi tumorale) e IFN-γ (interferone gamma), che hanno effetti antitumorali, antivirali e antimicrobici, poiché inibiscono la loro replicazione.
2- produrre e rilasciare granuli citotossici (lisosomi modificati) ricchi di ruote e fattorie performanti.
Le perforini sono proteine a forma di pori che sono responsabili di "perforare" la membrana plasmatica delle cellule infette, mentre i granzimi sono proteasi che fanno strada verso le cellule attraverso i pori formati dalle perforine e degradano le proteine intracellulari.
Può servirti: membrana basale: caratteristiche, struttura e funzioniL'azione combinata di perforine e granzimi termina con la cura della produzione di proteine virali, batteriche o parassita.
3- dirigono i meccanismi di morte apopototici sulle cellule infette attraverso interazioni FAS/FASL (proteina FAS e il loro ligando, che partecipano alla regolazione della morte cellulare).
Questo processo si verifica grazie all'espressione del ligando FASL sulla superficie delle cellule T attivate. L'unione proteica FAS (prodotta anche dai linfociti T citotossici) e il suo ricevitore innesca le cascate di attivazione della cisteina di proteasi note come caspari, che mediano direttamente i processi apapatotici cellulari.
Le cellule infette che vengono "elaborate" dai linfociti T citotossici vengono "pulite" da altre cellule come i fagociti, che partecipano anche alla "guarigione" di porzioni di tessuto morto o necrotico.
Attivazione
Le cellule T citolitiche sono attivate da cellule dendritiche che esprimono molecole di classe I MHC caricate o marcate con antigeni. Le cellule dendritiche possono esprimere questi antigeni a causa dell'ingestione di cellule intatte diretta o dell'ingestione di antigeni liberi.
Una volta che le cellule dendritiche processano cellule o antigeni infetti, questi antigeni presenti nel contesto delle molecole di classe I o di classe II del maggiore complesso di istocompatibilità (MHC).
Sono necessari almeno tre segnali specifici per attivare e promuovere la moltiplicazione delle cellule T citotossiche:
- La prima cosa che dovrebbe accadere è l'interazione tra il recettore della membrana TCR del linfocita T e l'MHC attaccato all'antigene presentato dalle cellule dendritiche.
- Quindi, un altro tipo di linfocita, una cellula con marcatori di superficie CD28, interagisce con il suo ligando (B7-1) sulle cellule che presentano l'antigene e fornisce il secondo segnale di attivazione.
- L'ultimo segnale, in grado di iniziare la proliferazione di cellule attivate, corrisponde alla produzione di interleucina 12 (IL-12) da parte delle cellule dendritiche.
Questo processo, inoltre, implica la mobilizzazione del calcio, la trascrizione genica, il rilascio di recettori pre-elaborati, l'internalizzazione dei recettori della superficie, tra gli altri.
È importante aggiungere che i linfociti che lasciano il timo non sono completamente differenziati, perché devono attivare e maturare per esercitare le loro funzioni. I linfiti citotossici "ingenui" o "vergini" possono riconoscere gli antigeni, ma non sono in grado di lisar le loro cellule bersaglio.
Può servirti: cella fiammeggiante: cosa è, struttura, operazioneMaturazione
La maturazione dei linfociti T inizia nel timo, dove si sviluppano da quelli che alcuni autori hanno chiamato T-Linfociti citotossici, che sono cellule impegnate nel lignaggio cellulare in questione, specifiche per uno strano antigene in particolare in particolare in particolare in particolare.
Queste cellule pre-linfociti esprimono i tipici recettori marker CD8 dei linfociti citolitici, ma non hanno ancora funzioni citolitiche. I pre-linfociti non sono abbondanti nel sangue, ma piuttosto all'interno di tessuti infetti o tessuti "strani".
La maturazione o la differenziazione dei linfociti T si verifica dopo la loro attivazione (che dipende dai segnali e dagli eventi descritti nella sezione precedente) e implica ottenere tutti i macchinari necessari per acquisire funzioni citolitiche.
La prima cosa che accade è la formazione di specifici granuli citotossici, attaccati alla regione interna della membrana plasmatica e ricca di perforine e granzimi.
Quindi l'espressione superficiale della proteina dell'Unione Fas (FASL) viene innescata e infine acquisisce la capacità di esprimere citochine e altre proteine che svolgeranno funzioni negli eventi di lisi cellulare.
Si dice che la maturazione delle cellule T, dopo la loro attivazione, termina con la differenziazione della "cellula effettrice", in grado di esercitare le funzioni del linfocita citolitico per la distruzione o l'eliminazione delle cellule ospiti infettate.
Inoltre, parte della popolazione di linfociti T che si è moltiplicata durante la differenziazione soddisfa funzioni come "cellule di memoria", ma questi hanno diversi schemi di espressione dei recettori della membrana che li distinguono dalle cellule "ingenui" e "effettore".
Riferimenti
- Abbas, a., Lichtman, a., E povero, j. (1999). Immunologia cellulare e molecolare (3a ed.). Madrid: McGraw-Hill.
- Andersen, m., Schrama, d., Straten, p., & Becker, J. (2006). Cellule T citotossiche. Journal of Investigative Dermatology, 126, 32-41.
- Barry, m., & Bleackley, R. C. (2002). Linfociti T citotossici: tutte le strade conducono alla morte. Immunologia delle recensioni della natura, 2(Giugno), 401-409.
- Cellule T citotossiche. (2012). In Immunologia per la farmacia (pp. 162-168). Estratto da ScienceDirect.com
- Ito, h., & Sixhima, M. (2010). Regolazione dell'induzione e della funzione dei linfociti T citotossici da parte delle cellule T killer naturali. Journal of Biomedicine and Biotechnology, 1-8.
- Janeway CA JR, Travers P, Walport M, et al. Immunobiologia: il sistema immunitario nella salute e nelle malattie. 5a edizione. New York: Garland Science; 2001. Citotossicità mediata dalle cellule T. Disponibile da: NCBI.Nlm.NIH.Gov
- Lam Braciale, V. (1998). Linfociti T citotossici. In Enciclopedia dell'immunologia (P. 725). Elsevier Ltd.
- Russell, J. H., & Law, t. J. (2002). Citotossicità mediata dai linfociti. Annu. Rev. Immunol., venti, 323-370.
- Wissinger, e. (N.D.). Società britannica per l'immunologia. Estratto il 25 settembre 2019 da Immunology.org
- « Caratteristiche, habitat, proprietà, coltivazione
- Caratteristiche dei capelli León, proprietà, coltivazione »

