Struttura isopreno, proprietà, applicazioni
- 3848
- 400
- Rosolino Santoro
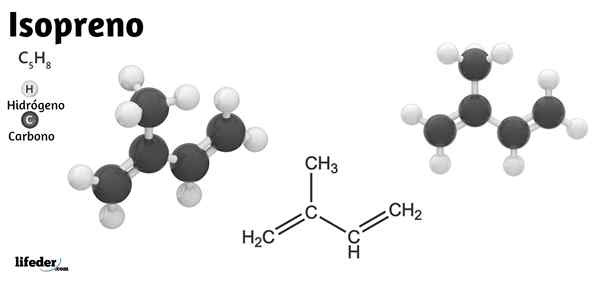
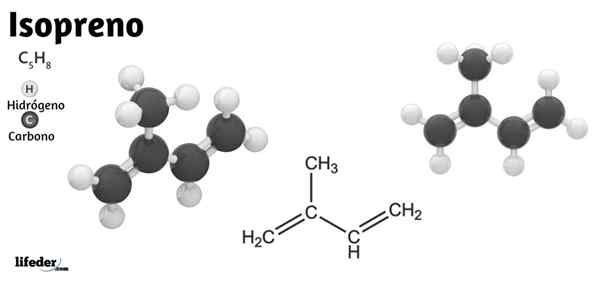
Lui Isoprene o 2-metil-1,3-butadiene, è un composto organico che consiste in un idrocarburo la cui formula molecolare è c5H8. Nonostante la sua apparente semplicità, rappresenta le basi strutturali della gomma naturale e, ancora più importante, lo scheletro delle unità biologiche con cui gli isoprenoidi o i terpeni sono sintetizzati enzimaticamente.
Pertanto, l'isoprene mantiene importanza non solo nella chimica organica ma anche nella biochimica. Nell'immagine inferiore si può vedere la sua formula strutturale, che può essere scomposta linearmente come Cho2= C (CH3) −ch = Cho2. Da questa formula si capisce perché il suo nome Iupac è 2-metil-1,3-butadiene, poiché i due doppi legami si trovano nei carboni 1 e 3.
L'isoprene è un idrocarburo considerevolmente comune nell'ambiente. Piante, alghe, batteri e animali sono in grado di sintetizzarlo ed emetterlo, persino formando la parte più abbondante delle nostre espirazioni. Le masse vegetali sono i principali produttori e emettitori di isoprene, usandolo in meccanismi per resistere al calore esterno.
Biochimicamente, l'isoprene nella sua unità biologica viene utilizzato dagli organismi per sintetizzare vari tipi di terpeni, tra cui il Laundhen e i componenti degli oli essenziali si distinguono. Organicamente, serve per la sintesi di gomme sintetiche e altri polimeri correlati.
[TOC]
Struttura isoprene
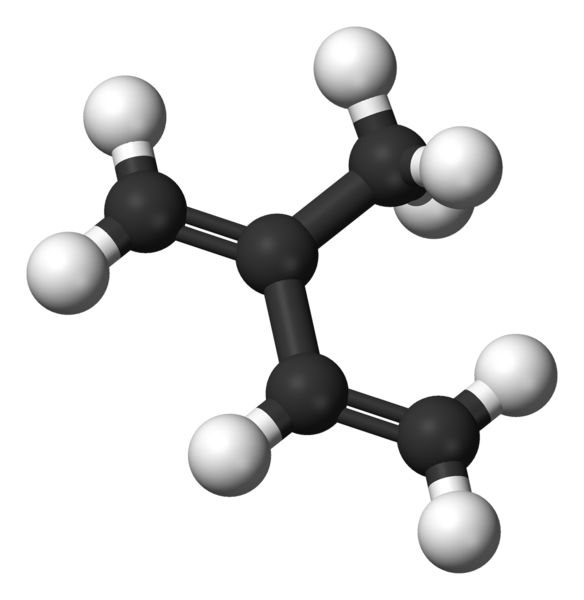 Molecola di isoprene rappresentato da un modello di sfere e barre
Molecola di isoprene rappresentato da un modello di sfere e barre Nell'immagine superiore abbiamo la struttura molecolare dell'isoprene. Come visto, le sfere nere corrispondono agli atomi di carbonio, mentre i bianchi sono atomi di idrogeno.
La molecola presenta una geometria piatta, cioè tutti i suoi atomi sono disposti sullo stesso piano, tranne gli idrogeni del gruppo -CH3 Carbon collegato 2. Questa geometria è dovuta al fatto che gli atomi di carbonio dello scheletro 1.3-butadiene hanno l'ibrazione SP2, mentre il carbonio di -ch3 Ha sp3.
Può servirti: bromo: storia, struttura, configurazione elettronica, proprietà, usiLe molecole di isoprene interagiscono tra loro attraverso forze dispersive di Londra, che sono considerevolmente deboli a causa delle loro masse molecolari basse. Tuttavia, esercitano una coesione sufficiente in modo che l'isoprene esista come liquido volatile in condizioni normali.
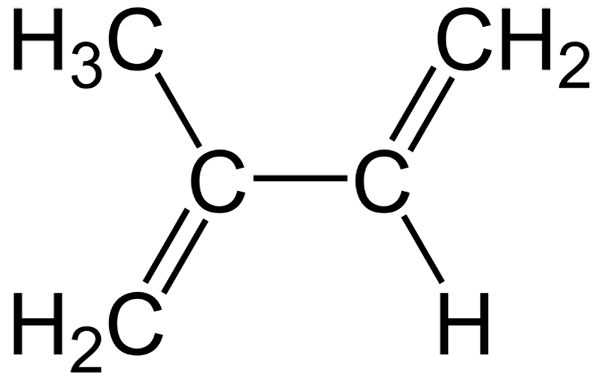 Formula strutturale dell'isoprene
Formula strutturale dell'isoprene Il fatto che le loro molecole siano piatte facilita il loro inserimento tra le membrane cellulari, contribuendo ai loro rinforzi nel meccanismo che le piante usano per cuscinare improvvisi cambiamenti di temperatura (40 ° C o più).
Le molecole di isoprene sono in grado di formare cristalli. Ma non accade allo stesso modo con i loro polimeri, il poliaprene, che tendono a raggrupparsi in solidi amorfi, le cui masse molecolari medie sono molto più grandi, cessando di essere una sostanza volatile.
Proprietà isoprene
Le proprietà qui menzionate corrispondono a quelle dell'isoprene e non a quelle della gomma naturale, che consiste nel polimero CIS-1,4-polisoprene. Alcune fonti bibliografiche possono persino usare le proprietà del lattice appena estratte dagli alberi per caratterizzare l'isoprene, essendo un grave errore per confonderli.
Aspetto
Fluido incolore e volatile con un odore simile all'olio.
Massa molare
68.12 g/mol
Punto di fusione
-143.95 ºC
Punto di ebollizione
3. 4.067 ºC. Pertanto, è un liquido abbastanza volatile.
punto d'infiammabilità
-54 ºC (tazza chiusa)
Temperatura di autorezione
395 ºC
Densità
0.681 g/cm3
Densità del vapore
2.35 in relazione all'aria.
Pressione del vapore
550 mmHg a 25 ° C, che è conforme alla sua grande volatilità.
Solubilità
Essere un idrocarburo è impossibile con l'acqua, situata nelle sue miscele sopra questo perché è meno denso. Tuttavia, è miscibile con acetone, benzene, etere petrolifero, disolfuro di carbonio, diclorometano e praticamente con qualsiasi altro solvente aromatico o clorato.
Può servirti: tipo di collegamento di 02Tensione superficiale
16.9 DINS/CM.
Reattività
L'isoprene può reagire nucleofile (attaccato da specie di elettroni) attraverso i loro carboni 1 e 4. Pertanto, alle estremità del suo scheletro di carbonio può essere polimero, il che dà origine al poliaprene. Questa reazione di polimerizzazione è esotermica, a tal punto che a contatto con alcune sostanze può diventare esplosivo.
Unità biologiche
L'isoprene, sebbene intrinsecamente presente nelle strutture dei terpeni, non è il materiale di partenza utilizzato dagli enzimi per sintetizzarli. Invece, usano prodotti metabolici chiamati prodotti isopentenil (IPP, blu) e dimetilalil pirofosfato (dmapp, rosso) prodotti pirofosfato come substrati (dmapp, rosso).
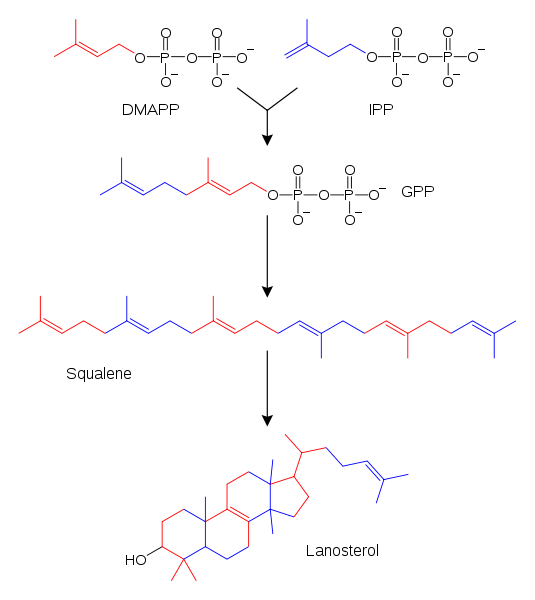 Sintesi di loostilo dalle unità biologiche dell'isoprene. Fonte: Fvasconcellos, originale di Tim Vickers / Public Domain
Sintesi di loostilo dalle unità biologiche dell'isoprene. Fonte: Fvasconcellos, originale di Tim Vickers / Public Domain Nell'immagine superiore un esempio del suddetto sopra. Sia, sia l'IPP che il DMAPP, reagiscono tra loro grazie all'intervento enzimatico per causare Geranilo pirofosfato (GPP).
Quest'ultimo, a sua volta, incorpora altri frammenti molecolari di IPP o DMApp (vedi colori), fino a quando non diventa l'esclane, un precursore prezioso per la sintesi della lana.
Quindi, l'isoprene nella sua unità biologica (IPP o DMAPP) partecipa alla biosintesi di steroli e altri lipidi. Abbiamo anche terpeni, come il limonene (di oli di limone e arancioni) e mirceno (olio di arrayán), che costituiscono oli essenziali e che sono sintetizzati da processi chimici e strutturalmente simili.
In questo senso, l'unità isoprene, a volte chiaramente riconoscibile nei terpeni o isoprenoidi, è essenziale per la sintesi di sinfine dei prodotti naturali.
Può servirti: legaApplicazioni isoprene
 Una delle principali applicazioni di gomma isoprene è la produzione di pneumatici per auto
Una delle principali applicazioni di gomma isoprene è la produzione di pneumatici per auto L'isoprene è polimerizzato in gomma naturale, quindi tutte le sue applicazioni possono essere attribuite a questo composto in modo indiretto. Fa parte del gutapercha, materiale elastico realizzato con una miscela di cis e polimeri trans 1.4-poliisopren, che una volta utilizzata per la produzione di palline da golf.
La gomma serve per l'elaborazione di sfere, tubi, guanti, preservativi, stivali, accessori di strumenti elettrici, adesivi, tute da immersione, bottiglie per bottiglie, rivestimenti che neutralizzano le vibrazioni; E soprattutto viene utilizzato, insieme alla sua versione sintetica, la gomma isoprene, per la produzione di massa di pneumatici.
L'isoprene, come il poligre, può essere miscelato con altri polimeri, come le gomme da sfregamento elasticizzate o butodiene, per produrre materiali ancora più resistenti e durevoli. Cioè, viene utilizzato per la sintesi di diversi copolimeri elastici.
Al di fuori dell'industria della gomma, l'isoprene è destinato come materiale di partenza per la sintesi di vitamine, aromi, steroidi, fragranze e qualsiasi altra sostanza isopreneide che è più praticabile per sintetizzarlo che per ottenerlo da fonti naturali da fonti.
Riferimenti
- Graham Solomons t.W., Craig b. Frigorifero. (2011). Chimica organica. (10th Edizione.). Wiley Plus.
- Carey f. (2008). Chimica organica. (Sesta edizione). Mc Graw Hill.
- Morrison e Boyd. (1987). Chimica organica. (Quinta edizione). Addison-Wesley Iberoamericana.
- Wikipedia. (2020). Isoprene. Recuperato da: in.Wikipedia.org
- Centro nazionale per le informazioni sulla biotecnologia. (2020). Isoprene. Pubchem Comunund Sommario per CID 6557. Recuperato da: pubchem.NCBI.Nlm.NIH.Gov
- Elsevier b.V. (2020). Isoprene. Scienceirect. Estratto da: ScienceDirect.com
- Database delle proprietà polimeriche. (2020). Gomma isoprene: proprietà e applicazioni. Recuperato da: polimerdatabase.com
- « Unità forza ionica, come calcolarla, esempi
- Struttura di diidroxiacetone, proprietà, ottenimento, usi »

