Struttura idrossido di ferro (ii), proprietà, usi
- 3152
- 248
- Rosolino Santoro
Lui Irondido di ferro (II), Chiamato anche idrossido ferroso, è un composto inorganico di formula chimica di fede (OH)2. Se la sua purezza è alta, il suo solido è composto solo da ioni di fede2+ e oh- In una relazione 2: 1; Tuttavia, possono contenere molecole d'acqua e diverse specie ioniche, cambiando la posizione.
Rappresenta la forma "ridotta" della famosa ruggine e superficie rossastra composta da ioni di fede3+; Mentre era in ruggine verdastra, la fede predomina2+, Accanto a Oh- e un altro importo di anioni: co32-, SW42-, NO3- e Haluros (F-, Cl-,… ), Per esempio. Il risultato, sebbene la base di questa ruggine verde è fede (oh)2, è che si ottengono vari solidi.
 Ossido verde sulla superficie del ferro: materiale di origine di questo tipo di idrossido. Fonte: Pixabay.
Ossido verde sulla superficie del ferro: materiale di origine di questo tipo di idrossido. Fonte: Pixabay. Nella vita quotidiana questo idrossido può essere contemplato in luoghi comuni. Ad esempio, la nave dell'immagine superiore ha la sua superficie coperta di ruggine verde (non patina). C'è la fede (oh)2, ma accompagnato da numerosi ioni dalle onde del mare.
Chimicamente parlando, le proprietà e gli usi di questo materiale dipendono dalla fede catione2+ e della sua tendenza a ossidarsi a trasformarsi in fede3+. È un agente riducente, che reagisce rapidamente con ossigeno in condizioni di base. Pertanto dovrebbe essere usato in atmosfere inerte e soluzioni acide.
[TOC]
Struttura di idrossido di ferro (II)
Link
Considerando solo fede (oh)2 Pure, non c'è niente di più ioni di fede2+ e oh-.
Le interazioni tra loro devono essere, in teoria, della natura ionica; Ogni fede fede2+ attira due anioni oh-, le cui attrazioni non direzionali finiscono per stabilire un ordine strutturale e ripetitivo che definisce un cristallo; che a sua volta, dà origine alla polvere di ruggine verde.
Può servirti: idrossido di zinco (Zn (OH) 2)Il problema è che esiste un certo carattere covalente tra i due ioni, e quindi un collegamento Fe-OH ionico non può essere ignorato. Considerando un collegamento Fe-OH parzialmente ionico, si può capire che sono raggruppati in una sorta di strato polimerico.
Doppi strati di idrossido
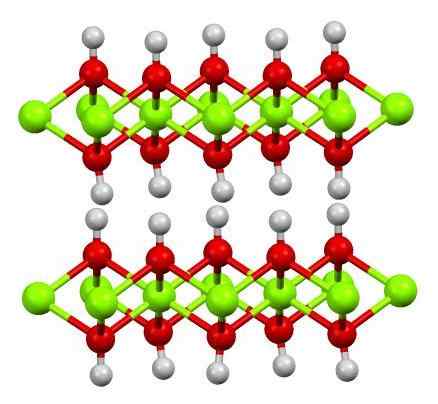
 Faith Structure (Oh) 2. Fonte: Smokefoot [CC BY-SA 4.0 (https: // creativeCommons.Org/licenze/by-sa/4.0)]
Faith Structure (Oh) 2. Fonte: Smokefoot [CC BY-SA 4.0 (https: // creativeCommons.Org/licenze/by-sa/4.0)] La struttura dell'idrossido ferroso puro con un modello di sfere e barre è mostrata sopra. Fe cations2+ Sono rappresentati dalle sfere verdi chillón, mentre oh anioni- Per le sfere rosse e bianche. Nota come gli ioni di fede sono allineati2+ Grazie alle interazioni (ionico-covalente) con l'OH-.
Perché questa struttura sono doppi strati di idrossidi? L'immagine stessa offre la risposta: ci sono due righe o strati di oh- Per ogni fede2+; Cioè, viene mantenuta la proporzione 2: 1 di fede (OH)2 menzionato all'inizio.
Unità strutturali per fede (oh)2 Sono quindi questi panini, dove gli strati di oh- Venerebbero a rappresentare i pani; pane caricato negativamente e che, quindi, non riesce a correggere un cristallo marrone sorprendente.
Ma, d'altra parte, anche gli atomi di H si allineano ed eclissi tra loro. Ricordando il concetto di polarità e elettronegatività, questi idrogeni hanno un leggero carico parziale positivo, Δ+; che, sebbene debole, può avere un'area positiva in cui sono alloggiati altri anioni o molecole.
Idrato
When Faith (Oh)2 Si dissolve nell'acqua, le sue molecole si coordinano con il Metal Center of Faith2+ Per formare una ACU complessa: [Faith (H2O)4(OH)2". Questo complesso ha una geometria ottaedrica per avere sei ligandi: quattro molecole d'acqua e due OH-. Tuttavia, nell'idrossido ferroso il panorama è un po 'diverso.
Può servirti: legge sulla conservazione della materiaIn idrata, la formula ipotetica Fe (OH)2· NH2Oppure, le molecole d'acqua sono alloggiate esattamente tra i due strati di idrossido; Cioè, interagiscono attraverso le forze degli ioni di dipolo con idrogeni o sfere bianche. È come se due partite di Ohfeoh fossero afferrate e l'acqua fosse intervallata per raggrupparle: Ohfeoh (H2O) Ohfeah.
Le molecole d'acqua sono molto dinamiche, impedendo alle particelle idrato di acquisire dimensioni considerevoli e, di conseguenza, formano un colloidale solido o una gelatina.
Ruggine verde e rossa
In idrato gli strati di idrossido hanno molecole d'acqua intervallate; Tuttavia, possono avere altri anioni (già menzionati), causando un'ampia varietà di armi verdi. Possono anche "catturare" molecole grandi come il DNA o i farmaci.
Non solo possono essere presenti gli ioni di fede2+, ma anche fede3+, Prodotto dell'ossidazione interna causata dall'ossigeno intervallato. Visibilmente si osserva che la ruggine verde (ossido u) inizia a diventare rossastro all'aumentare della concentrazione di fede3+.
Proprietà
 Provetta con idrossido ferroso in acqua. Fonte: ChemicalIrrest [dominio pubblico]
Provetta con idrossido ferroso in acqua. Fonte: ChemicalIrrest [dominio pubblico] Faith (Oh) è mostrata sopra2 precipitato in una provetta. Essendo in acqua abbondante, la complessa ACU deve predominare al di sopra della nuova struttura. Si noti che la superficie sembra un colore arancione, a seguito dell'ossidazione della fede2+ alla fede3+ per l'ossigeno dell'aria; Cioè, questo idrossido è un agente riducente:
Fede2+ Fede3+ + E-
L'aspetto fisico di questo composto nel suo stato più puro è quello di un solido marrone:
 Puro idrossido ferroso. Fonte: Ondřej Mangl [dominio pubblico]
Puro idrossido ferroso. Fonte: Ondřej Mangl [dominio pubblico] Che, a seconda del suo livello di umidità, può essere presentato come un solido gelatina. È abbastanza insolubile in acqua (ksp= 8 · 10-16 e solubilità = 0,72 g/100 ml a 25 ° C) e ha una massa molare di 89,86 g/mol e una densità di 3,4 g/ml.
Può servirti: i 20 tipi di chimica e la loro denificazioneNon sono riportati alcun punto di ebollizione o fusione per questo composto; Probabilmente a causa del fatto che, prima di una fonte di calore, diventa disidratato e si converte in ossido ferroso, brutto:
Faith (Oh)2 => Ugly + H2O
Applicazioni
Analisi qualitativa organica
La sua potenza riducente viene utilizzata per determinare la presenza di composti nitro, RNO2. La reazione per la quale si ottiene un test positivo è rappresentata con la seguente equazione chimica:
Rno2 + 6fe (OH)2 + 4h2O => rnh2 + 6fe (OH)3
La fede (oh)3 precipita come un solido marrone -redizo, che certifica la presenza del gruppo nitro, -No2.
Riduttore di selenio oxoanions
Il potere riducente della fede (Oh)2 Ha anche usato per ridurre gli anioni SEO32- (Selenito) e SEO42- (Selenate) al selenio elementare,. Praticamente, consente la rimozione di tali anioni, dannosi per la salute, sotto forma di un selenio insolubile e facilmente rimovibile.
Materiali a doppio strato
La sua struttura pura e la ruggine verde, è una fonte di ispirazione per la progettazione di nuovi materiali di caratteristiche mineralogiche.
Si stima che la funzione di questi sia consentire il trasporto di una specie specifica tra i suoi strati, in modo tale che la sua liberazione possa essere controllata o ridotta al sito attivo (terreni, cellule, superficie metallica, ecc.).
Riferimenti
- SHIVER & ATKINS. (2008). Chimica inorganica. (Quarta edizione). Mc Graw Hill.
- Wikipedia. (2019). Ferro (ii) idrossido. Recuperato da: in.Wikipedia.org
- Centro nazionale per le informazioni sulla biotecnologia. (2019). Idrossido ferroso. Database PubChem. CID = 10129897. Recuperato da: pubchem.NCBI.Nlm.NIH.Gov
- Nick Doe. (S.F.). Test per fenoli e gruppi nitro. Chimica 211. Estratto da: accademici.Wellesley.Edu
- Clark Jim. (27 aprile 2019). Chimica del ferro. Chimica librettexts. Recuperato da: Chem.Librettexts.org
- Software tecnico Kingston. (2019). Chimica della ruggine. Medici di corrosione. Recuperato da: corrosione-dotatori.org
- Zingaro, Ralph a. et al. (1997). Riduzione degli anioni di ossoselenio mediante idrossido di ferro (II). Environment International. 23 (3): 299-304. Doi: 10.1016/S0160-4120 (97) 00032-9
- « Proprietà di ossido di cloro (v), struttura, usi
- Proprietà di ossido di cloro (iii), struttura, usi »

