Equazione di Henderson-Haselbalch Spiegazione, esempi, esercizio fisico
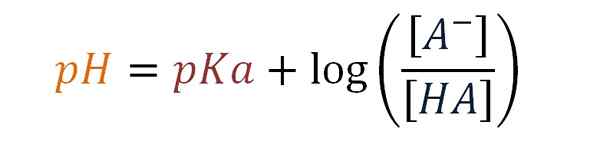
- 4943
- 1290
- Benedetta Rinaldi
IL Equazione di Henderson-Haselbalch È un'espressione matematica che consente il calcolo del pH di un ammortizzatore o una soluzione di smorzamento. Si basa sulla PKA di acido e sulla relazione tra coniugati o concentrazioni di sale e acido, presenti nella soluzione di smorzamento.
L'equazione fu inizialmente sviluppata da Lawrence Joseph Henderson (1878-1942) nel 1907. Questo chimico ha stabilito i componenti della sua equazione in base all'acido carbonico come soluzione tampone o tampone.
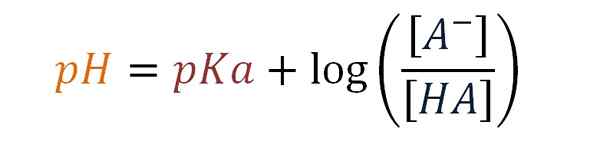 Equazione di Henderson-Haselbalch. Fonte: Gabriel Bolívar.
Equazione di Henderson-Haselbalch. Fonte: Gabriel Bolívar. Successivamente, Karl Albert Hasselbalch (1874-1962) introduce nel 1917 l'uso di logaritmi per integrare l'equazione di Henderson. Il chimico danese ha studiato reazioni di sangue con ossigeno e l'effetto sul suo pH.
Una soluzione tampone è in grado di ridurre al minimo le variazioni del pH che subiscono una soluzione aggiungendo un forte volume di acido o base. È formato da un acido debole e dalla sua forte base coniugata che viene rapidamente dissociata.
[TOC]
Spiegazione
Sviluppo matematico
Un acido debole in una soluzione acquosa si dissocia secondo la legge sull'azione di massa, secondo il seguente schema:
Ha +h2O ⇌ h+ + A-
HA è acido debole e- La tua base coniugata.
Questa reazione è reversibile e ha una costante di equilibrio (KA):
Ka = [h+] ·[A-] / [Ha]
Prendendo logaritmi:
log ka = log [h+] +Log [a-] -log [ha]
Se ogni termine dell'equazione viene moltiplicato per (-1), è espresso nel modo seguente:
- log ka = - log [h+] -log [a] +log [ha]
Il - log ka è definito come pka e il log [h+] è definito come pH. Dopo aver effettuato la dovuta sostituzione, l'espressione matematica è ridotta a:
pka = ph -log [a-] +Log [ha]
Cancella i termini di pH e raggruppamento, l'equazione è espressa nel modo seguente:
Può servirti: link triplo covalenteph = pka +log [a-] / [Ha]
Questa è l'equazione di Henderson-Haselbalch per un ammortizzatore formato da un acido debole.
Equazione per una base debole
Allo stesso modo, una base debole può formare una soluzione tampone e l'equazione di Henderson-Haselbalch per essa è la seguente:
Poh = pkb +log [hb] / [b-"
Tuttavia, la maggior parte delle soluzioni di smorzamento sono originate, comprese quelle di importanza fisiologica, dalla dissociazione di un acido debole. Pertanto, l'espressione più usata per l'equazione di Henderson-Haselbalch è:
ph = pka +log [a-] / [Ha]
Come agisce una soluzione buffer?
Azione per ammortizzatore
L'equazione di Henderson-Haselbalch indica che questa soluzione è formata da un acido debole e una forte base coniugata espressa come sale. Questa composizione consente alla soluzione di smorzamento di rimanere con un pH stabile sebbene vengano aggiunti acidi o basi forti.
Aggiungendo un forte acido all'ammortizzatore, reagisce con la base coniugata per formare sale e acqua. Ciò neutralizza l'acido e consente alla variazione del pH di essere minima.
Ora, se una base forte viene aggiunta all'ammortizzatore, reagisce con acido debole e forma dell'acqua e sale, neutralizzando l'azione della base aggiunta sul pH. Pertanto, la variazione del pH è minima.
Il pH di una soluzione tampone dipende dalla relazione tra concentrazioni di base coniugate e acido debole, e non dal valore assoluto delle concentrazioni di questi componenti. Una soluzione di smorzamento con acqua può essere diluita e il pH non varia praticamente.
Capacità di ammortizzatore
La capacità di smorzamento dipende anche dalla PKA di acido debole, nonché dalle concentrazioni di acido debole e base coniugata. Più vicino all'acido PKA è il pH della soluzione di smorzamento, maggiore è la sua capacità di smorzamento.
Può servirti: principio di Le ChâtelierInoltre, maggiore è la concentrazione dei componenti della soluzione tampone, maggiore sarà la sua capacità di smorzamento.
Esempi di equazioni di Henderson
Tampone acetato
ph = pka +log [Cho3COO-] / [Cho3COOH]
PKA = 4.75
Acido carbonico Amortide
ph = pka +log [HCO3-] / [H2Co3"
PKA = 6.11
Tuttavia, il processo globale che porta alla formazione dello ione bicarbonato in un organismo vivente è il seguente:
Co2 + H2O ⇌ HCO3- + H+
Essere co2 Un gas, la sua concentrazione in soluzione è espressa in base alla sua pressione parziale.
ph = pka +log [HCO3-] / α · PCO2
α = 0,03 (mmol/l)/mmHg
PCO2 è la pressione parziale del CO2
E poi l'equazione sarebbe come:
ph = pka +log [HCO3-] / 0,03 · PCO2
Shock lattato
ph = pka +log [lattato ione] / [acido lattico]
PKA = 3.86
Assorbitore di ammorti di fosfato
ph = pka +log [fosfato dibasico] / [fosfato monobasico]
ph = pka +log [HPO42-] / [H2Po4-"
PKA = 6.8
Oxihemoglobin
ph = pka +log [HBO2-] / [HHBO2"
PKA = 6.62
DeSossiemoglobina
ph = pka +log [hb-] / Hbh
PKA = 8.18
Esercizi risolti
Esercizio 1
L'assorbitore di shock fosfato è importante nella regolazione del pH del corpo, poiché il suo PKA (6,8) è vicino al pH nel corpo (7,4). Quale sarà il valore della relazione [na2HPO42-] / [Nah2Po4-] dell'equazione di Henderson-Haselbalch per un valore di pH = 7,35 e un PKA = 6,8?
La reazione di dissociazione di Nah2Po4- È:
Nah2Po4- (acido) ⇌ nahpo42- (Base) +H+
ph = pka +log [Na2HPO42-] / [Nah2Po4-"
Clearendo la relazione [coniugata / acida] per la soluzione di smorzamento del fosfato, abbiamo:
7.35 - 6.8 = log [NA2HPO42-] / [Nah2Po4-"
0,535 = log [Na2HPO42-] / [Nah2Po4-"
100,535 = 10Log [Na2HPO4] / [NAH2PO4]
Può servirti: difenilammina3.43 = [NA2HPO42-] / [Nah2Po4-"
Esercizio 2
Una soluzione tampone acetata ha una concentrazione di acido acetico di 0,0135 m e una concentrazione di acetato di sodio 0,0260 M. Calcola il pH della soluzione di ammortizzatore, sapendo che il PKA per l'assorbitore di ammorti di acetato è 4,75.
L'equilibrio di dissociazione per l'acido acetico è:
Cap3COOH ⇌ CH3COO- + H+
ph = pka +log [Cho3COO-] / [Cho3COOH]
Sostituire i valori che abbiamo:
[Ch3COO-] / [Cho3COOH] = 0,0260 m / 0,0135 m
[Ch3COO-] / [Cho3COOH] = 1.884
Log 1.884 = 0,275
pH = 4.75 +0.275
pH = 5.025
Esercizio 3
Un ammortizzatore di acetato contiene 0,1 m di acido acetico e acetato di sodio 0,1 M. Calcola il pH della soluzione di smorzamento dopo aver aggiunto 5 ml di 0,05 m con acido cloridrico da 10 ml.
Il primo passo è calcolare la concentrazione finale dell'HCL durante la miscelazione con la soluzione tampone:
Vi · ci = vf · cf
CF = VI · (CI / VF)
= 5 ml · (0,05 m / 15 ml)
= 0,017 m
L'acido cloridrico reagisce con acetato di sodio per formare acido acetico. Pertanto, la concentrazione di acetato di sodio diminuisce di 0,017 m e la concentrazione di acido acetico aumenta della stessa quantità:
pH = pka +log (0,1 m - 0,017 m) /(0,1 m +0,017 m)
ph = pka +log 0,083 / 0,017
= 4.75 -0.149
= 4.601
Riferimenti
- Whitten, Davis, Peck e Stanley. (2008). Chimica. (8 ° ed.). Apprendimento del Cengage.
- Jimenez Vargas e J. Mª Macarulla. (1984). Fisiologico fisico. 6a edizione. Editoriale interamericano.
- Wikipedia. (2020). Equazione di Henderson-Hasselbalch. Recuperato da: in.Wikipedia.org
- Gurinder Khaira e Alexander Kot. (5 giugno 2019). Approssimazione di Henderson-Hasselbalch. Chimica librettexts. Recuperato da: Chem.Librettexts.org
- Helmestine, Anne Marie, PH.D. (29 gennaio 2020). Definizione dell'equazione di Henderson Hasselbalch. Recuperato da: Thoughtco.com
- I redattori di Enyclopedia Britannica. (6 febbraio 2020). Lawrence Joseph Henderson. Encyclopædia Britannica. Recuperato da: Britannica.com
- « Caratteristiche, funzioni, esempi e parti di prefazione
- Refrattometria di fondazione, tipi di refrattari, applicazioni »

