Acido propanoico
- 3734
- 354
- Silvano Montanari
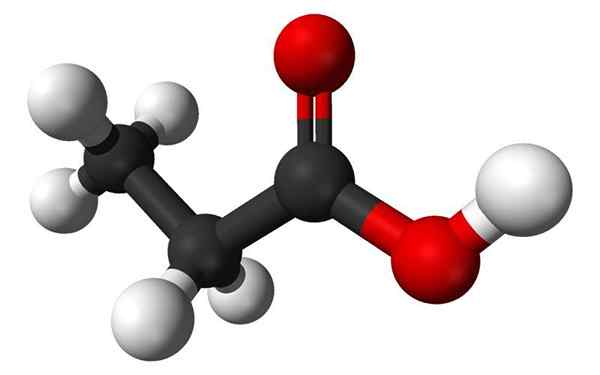
 Molecola di acido propanoico in un modello a barre e sfere. Fonte: Benjah-BMM27, Wikimedia Commons
Molecola di acido propanoico in un modello a barre e sfere. Fonte: Benjah-BMM27, Wikimedia Commons Cos'è l'acido propano?
Lui Acido propanoico, Chiamato anche propionico, è un acido grasso a catena corta satura che include etano attaccato in carbonio da un gruppo carbossilico. La sua formula è Cho3-Cap2-COOH.
L'anione CH3CH2Coo, così come i sali e gli esteri dell'acido propanico, sono noti come proporzioni (o propanoa).
Può essere ottenuto dai residui di polpa di legno mediante processo di fermentazione, usando i batteri di genere Propionibacterium. È anche ottenuto da etanolo e monossido di carbonio, usando un catalizzatore di trifluoruro di boro.
Un altro modo per ottenere acido propano è dovuto all'ossidazione di una proporzione in presenza di ioni di cobalto o manganese. Questa reazione si sviluppa rapidamente a temperature fino a 40-50 ° C:
2ch3Cap2CHO + O2 → 2ch3Cap2COOH
Il composto è naturalmente presente a bassi livelli nei prodotti lattiero -caseari e si verifica in modo generale, insieme ad altri acidi grassi a catena corta, nel tratto gastrointestinale di esseri umani e altri mammiferi come prodotto finale della digestione microbica dei carboidrati.
Proprietà fisiche e chimiche
- L'acido propanoico è un liquido incolore e oleoso, con odore di acro, spiacevole e rancido.
- Ha un peso molecolare di 74,08 g/mol e una densità di 0,992 g/ml.
- Il suo punto di congelamento e di ebollizione è rispettivamente -20,5 ° C e 141,1 ° C.
- L'acido propanoico è un acido debole, il cui PKA è 4,88.
- Il composto è molto solubile in acqua, essendo in grado di dissolvere 34,97 grammi composti da ogni 100 ml di solvente. È anche solubile in etanolo, etere e cloroformio.
Può servirti: composti organici: caratteristiche, classificazione, esempi- Ha proprietà fisiche intermedie tra quelle di acidi carbossilici più piccoli, acidi formici e acetici e acidi grassi più grandi.
- Mostra le proprietà generali degli acidi carbossilici e può formare derivati da ammide, estere, anidride e cloruro.
- Puoi subire un'alogenazione alfa con Bromo in presenza di PBR3 come catalizzatore (la reazione HVZ) per formare CH3CHRCOOH.
Reattività e pericoli
L'acido propanoico è un materiale infiammabile e di carburante. Può essere illuminato da calore, scintille o fiamme. I vapori possono formare miscele esplosive con l'aria, essendo in grado di viaggiare alla fonte di accensione e di sfruttare.
la maggior parte dei vapori è più pesante dell'aria. Saranno estesi lungo il terreno e saranno raccolti in aree basse o confinate (fognature, scantinati, serbatoi). Pericolo di esplosione o fogne interni, esterni o fognari.
Le sostanze designate con A (P) possono essere polimeriche esplicamente. I contenitori possono esplodere quando riscaldati.
Il composto deve essere tenuto lontano dal calore o dalle fonti di accensione. Se riscaldato alla decomposizione emette fumo acro e fumi irritanti.
L'acido propanoico è irritante per la pelle, gli occhi, il naso e la gola, ma non produce effetti sistemici acuti e non ha un potenziale genotossico dimostrabile. In caso di contatto devi lavarti con molta acqua.
Biochimica
La base coniugata dell'acido propanico, il propionato, è formata come il frammento terminale a tre carbonio (attivato con coenzima a come propionil-CoA) nell'ossidazione degli acidi grassi del numero impar e l'ossidazione della catena laterale della laterale della laterale la laterale della laterale della laterale della laterale della laterale della laterale della laterale della laterale della laterale catena della catena laterale del colesterolo.
Può servirti: costante di ionizzazioneEsperimenti con isotopi radioattivi di propionato iniettati nei ratti a digiuno indicano che può apparire in glicogeno, glucosio, intermedi del ciclo di acido citrico, aminoacidi e proteine.
La via del metabolismo dell'acido propanoico implica l'interazione con il coenzima A, la carbossilazione per formare metilmalonil-coenzima A e conversione in acido succinico, che entra nel ciclo dell'acido citrico.
L'acido propanoico può ossidarsi senza formare corpi chetonici e, a differenza dell'acido acetico, è incorporato in un carboidrato, nonché un lipide.
L'acido propionico è uno degli acidi organici più frequenti, una malattia che include molti disturbi diversi.
Il risultato di pazienti nati con acido propionico è scarso nei modelli di sviluppo intellettuale, con il 60% che hanno un coefficiente intellettuale inferiore a 75 e che richiedono un'istruzione speciale.
Trapianti renali epatici e/o di successo in pochi pazienti hanno portato a una migliore qualità della vita, ma non hanno necessariamente impedito complicanze neurologiche e visceri.
Questi risultati sottolineano la necessità di un monitoraggio metabolico permanente, indipendentemente dalla strategia terapeutica.
Applicazioni
- L'acido propanoico inibisce la crescita batterica e della muffa a livelli tra lo 0,1 e l'1% in peso. Di conseguenza, la maggior parte dell'acido propano prodotto viene consumata come conservante sia per alimenti per mangimi e consumi umani, come cereali e cereali.
- Circa il 51% del consumo mondiale di acido propanoico è destinato all'alimentazione degli animali e alla conservazione del grano, mentre quasi il 29% viene utilizzato nella produzione di propionatos di calcio e sodio, che sono anche utilizzati nell'industria alimentare e alimentare.
Può servirti: idruro di litio: struttura, proprietà, ottenimento, usi- Altri mercati importanti per l'acido propano sono la produzione di erbicidi e quello di Cetona dietil. Le applicazioni di volume inferiore includono propionato acetato di cellulosa, prodotti farmaceutici, solventi, aromatizzante e fragranza, plastificazione, coloranti e assistenti tessili, in pelle e gomma.
- La domanda di acido propanoico dipende in gran parte dalla produzione di mangimi e cereali, seguita da alimenti confezionati e prodotti da forno.
- Altri mercati in rapida crescita includono esteri propionati per solventi, come n-butilo e pentilo propionato. Questi esteri sono sempre più usati come sostituti dei solventi elencati come inquinanti atmosferici pericolosi.
Riferimenti
- Acido propionico. Recuperato da EBI.AC.UK.
- Acido propionico. HMDB è stato recuperato.AC.
- Manuale di economia chimica acido propionico. Estratto da IHS IHS.com.

