Tipi di corpi chetogenesi, sintesi e degradazione
- 4763
- 277
- Silvano Montanari
IL chetogenesi È il processo attraverso il quale si ottengono acetoacetato, β-idrossibutirato e acetone, che insieme sono chiamati corpi chetonici. Questo meccanismo complesso e finemente regolato viene effettuato nei mitocondri, dal catabolismo degli acidi grassi.
Ottenere i corpi chetonici avviene quando il corpo è soggetto a periodi di digiuno esaustivi. Sebbene questi metaboliti siano per lo più sintetizzati nelle cellule epatiche, si trovano come un'importante fonte di energia nei tessuti vari, come il muscolo scheletrico e nel cuore e nei tessuti cerebrali.
 Fonte: SAV VAS [CC0]
Fonte: SAV VAS [CC0] Β-idrossibutirato e acetoacetato sono metaboliti usati come substrati nel muscolo cardiaco e nella corteccia renale. Nel cervello, i corpi chetonici diventano importanti fonti di energia quando il corpo ha esaurito la sua riserva di glucosio.
[TOC]
Caratteristiche generali
La chetogenesi è considerata una via fisiologica o metabolica molto importante. Generalmente, questo meccanismo viene eseguito nel fegato, sebbene sia stato dimostrato che può essere eseguito in altri tessuti in grado di metabolizzare gli acidi grassi.
La formazione di corpi chetonici è la principale derivazione metabolica di acetil-CoA. Questo metabolita è ottenuto dalla via metabolica nota come β-ossidazione, che è la degradazione degli acidi grassi.
La disponibilità di glucosio nei tessuti in cui si verifica β-ossidazione determina la destinazione metabolica di acetil-CoA. In particolari situazioni, gli acidi grassi ossidati sono diretti quasi interamente alla sintesi di corpi chetonici.
Tipi e proprietà dei corpi chetonici
Il corpo chetonico principale è l'acetoacetato o l'acido acetoacetico, che è per lo più sintetizzato nelle cellule epatiche. Dall'acetoacetato, sono derivate le altre molecole che compongono i corpi chetonici.
La riduzione dell'acido acetoacetico dà origine a D-β-idrossibutirato, il secondo corpo chetonico. L'acetone è un composto difficile da degradare ed è prodotto da una reazione di decarbossilazione spontanea dell'acetoacetato (quindi non richiede un intervento di alcun enzima), quando è presente in alte concentrazioni nel sangue.
La denominazione dei corpi chetonici è stata disposta per convenzione, dal momento che il β-idrossibutirato a rigor di termini non ha una funzione chetone. Queste tre molecole sono solubili in acqua, il che facilita il trasporto del sangue. La sua funzione principale è quella di fornire energia a determinati tessuti come muscolo scheletrico e cardiaco.
Gli enzimi coinvolti nella formazione di corpi chetonici sono principalmente nel fegato e nei reni, il che spiega che queste due posizioni sono i principali produttori di questi metaboliti. La sua sintesi si verifica solo ed esclusivamente nella matrice mitocondriale delle cellule.
Può servirti: sporulazione: nelle piante, nei funghi e nei batteriUna volta che queste molecole sono state sintetizzate, vanno al flusso sanguigno affrontando i tessuti che li richiedono, dove si degradano fino a acetil-CoA.
Sintesi di corpi chetonici
Condizioni per la chetogenesi
La destinazione metabolica dell'acetil-CoA dall'ossidazione β dipende dai requisiti metabolici dell'organismo. Questo è ossidato a CO2 e h2O attraverso il ciclo dell'acido citrico o la sintesi di acidi grassi, se il metabolismo di lipidi e carboidrati è stabile nel corpo.
Quando il corpo ha bisogno di carboidrati, l'ossalacetato viene utilizzato per la produzione di glucosio (gluconeogenesi) invece di iniziare il ciclo dell'acido citrico. Ciò accade, come detto, quando il corpo ha una certa incapacità di ottenere glucosio, in casi come il digiuno prolungato o la presenza di diabete.
Per questo motivo, l'acetil-CoA risultante dall'ossidazione degli acidi grassi viene utilizzato per la produzione di corpi chetonici.
Meccanismo
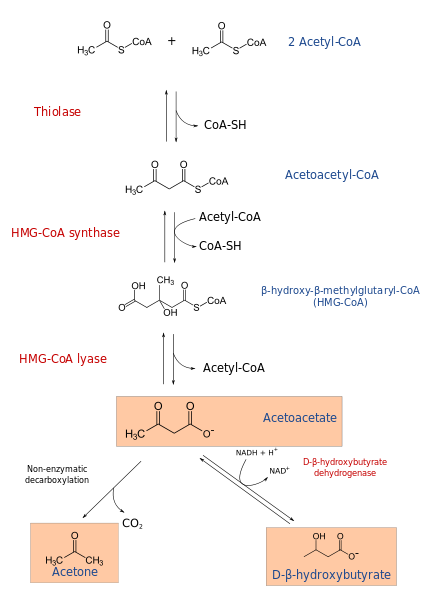
Il processo di chetogenesi inizia dai prodotti dell'ossidazione β: acetacetil-CoA o acetil-CoA. Quando il substrato è acetil-CoA, il primo passo consiste nella condensazione di due molecole, reazione acetil-COA transferasi, per produrre acetacetil-CoA.
L'acetacetil-CoA è condensato con un terzo acetil-CoA dall'azione dell'HMG-CoA sintasi, per produrre HMG-CoA (β-idrossi-β-metilglutaril-CoA). L'HMG-CoA è degradato in acetoacetato e acetil-CoA mediante azione HMG-CoA LIASA. In questo modo si ottiene il primo corpo chetonico.
L'acetoacetato è ridotto a β-idrossibutirato dall'intervento di β-idrossibutirato deidrogenasi. Questa reazione dipende da NADH.
Il principale corpo di acetoacetato chetonico è un β-cetoacido, che sperimenta decarbossilazione non enzimatica. Questo processo è semplice e produce acetone e co2.
Questa serie di reazioni provoca quindi i corpi chetonici. Questi essere solubili in acqua possono essere trasportati in modo semplice attraverso la circolazione sanguigna, senza la necessità di ancorare a una struttura di albumina, come nel caso degli acidi grassi che sono insolubili in mezzo acquoso.
Β-ossidazione e chetogenesi sono correlati
Il metabolismo degli acidi grassi produce substrati per la chetogenesi, quindi questi due modi sono funzionalmente correlati.
L'acetoacetil-CoA è un inibitore del metabolismo degli acidi grassi, poiché interrompe l'attività dell'acil-CoA deidrogenasi che è il primo enzima di β-ossidazione. Inoltre, esercita anche l'inibizione sul trasferimento di acetil-CoA e HMG-CoA sintasi.
L'enzima HMG-CoA sintasi, soggetto al CPT-I (enzima coinvolto nella produzione di acil carnitina nell'ossidazione β), rappresenta un importante ruolo regolatorio nella formazione di acidi grassi.
Può servirti: flora e fauna di Zacatecas: specie più rappresentativeRegolazione dell'ossidazione β e il suo effetto sulla chetogenesi
L'alimentazione dell'organismo regola un insieme complesso di segnali ormonali. Carboidrati, aminoacidi e lipidi consumati nella dieta sono depositati sotto forma di triacilgliceroli nel tessuto adiposo. L'insulina, un ormone anabolico, interviene nella sintesi dei lipidi e nella formazione di triacilgliceroli.
A livello mitocondriale, l'ossidazione β è controllata dall'ingresso e dalla partecipazione di alcuni substrati nei mitocondri. L'enzima cpt I sintetizza l'acile carnitina da Acil citosolic acil.
Quando il corpo viene alimentato, l'acetil-CoA carbossilasi e il citrato aumentano i livelli di CPT I, mentre diminuisce la sua fosforilazione (reazione dipendente dall'AMP ciclica).
Ciò provoca un accumulo di Malonil COA, che stimola la sintesi di acidi grassi e ne blocca l'ossidazione, prevenendo un ciclo inutile da generare.
Nel caso del digiuno, l'attività della carbossilasi è molto bassa perché i livelli dell'enzima CPT I sono stati ridotti e si sono anche fosforilati, attivando e promuovendo l'ossidazione dei lipidi, il che consentirà successivamente la formazione dei corpi di chetone attraverso l'acetilico -Coa.
Degradazione
I corpi chetonici si diffondono al di fuori delle cellule in cui erano sintetizzati e vengono trasportati ai tessuti periferici dal flusso sanguigno. In questi tessuti possono essere ossidati attraverso il ciclo di acidi tricarbossilici.
Nei tessuti periferici β-idrossibutirato viene ossidato in acetoacetato. Successivamente l'attuale acetoacetato viene attivato dall'azione dell'enzima transferasi 3-zoa.
Succinil-CoA agisce come un donatore di COA che diventa succinato. L'attivazione dell'acetoacetato si verifica per prevenire il succinil-CoA.
L'aceoacetil-CoA risultante subisce una rottura tiolitica che produce due molecole di acetil-CoA che sono incorporate nel ciclo di acidi tricarbossilici, meglio conosciuta come ciclo di Krebs.
Le cellule epatiche mancano del trasferimento di 3 cotoacil-CoA, impedendo l'attivazione di questo metabolita in queste cellule. In questo modo è garantito che i corpi chetonici non si ossidano nelle cellule in cui sono stati prodotti, ma che possono essere trasferiti nei tessuti in cui è richiesta la loro attività.
Rilevanza medica dei corpi chetonici
Nel corpo umano, alte concentrazioni di corpi chetonici nel sangue possono causare condizioni speciali chiamate acidosi e chetonemia.
Può servirti: sfingomyeline: cosa è, struttura, funzioni, sintesiLa produzione di questi metaboliti corrisponde al catabolismo di acidi grassi e carboidrati. Una delle cause più comuni di una condizione di chetogenesi patologica è l'alta concentrazione di frammenti di dicarbonati acetici che non si degradano sulla via di ossidazione degli acidi tricarbossilici.
Di conseguenza, vi è un aumento dei livelli di corpi chetonici nel sangue superiori a 2-4 mg/100 N e la loro presenza nelle urine. Ciò si traduce nel disturbo del metabolismo intermedio di questi metaboliti.
Alcuni difetti nei fattori neuroglandolari ipofisari che regolano la degradazione e la sintesi dei corpi chetonici, insieme ai disturbi nel metabolismo dell'idrocarburo, sono la causa della condizione dell'ipercetonemia.
Diabete mellito e accumulo di corpi chetonici
Il diabete mellito (tipo 1) è una malattia endocrina che provoca un aumento della produzione di corpi chetonici. La produzione inadeguata dell'insulina disabilita il glucosio per i muscoli, il fegato e il tessuto adiposo, accumulando così nel sangue.
Le cellule in assenza di glucosio iniziano il processo di gluconeogenesi e degradazione di grassi e proteine per ripristinare il loro metabolismo. Di conseguenza, le concentrazioni di ossalacetato diminuiscono e aumentano l'ossidazione dei lipidi.
Si verifica un accumulo di acetil-CoA, che in assenza di ossalacetato non può seguire il percorso dell'acido citrico.
L'accumulo di acetone è rilevato dalla sua presenza nelle urine e nel respiro delle persone che presentano questa condizione, ed è in realtà uno dei sintomi che indicano la manifestazione di questa malattia.
Riferimenti
- Blázquez Ortiz, c. (2004). Chetogenesi negli astrociti: caratterizzazione, regolazione e possibile documento citoprotettivo (Dottorato di tesi, Università Complutse di Madrid, Servizio delle pubblicazioni).
- Devlin, t. M. (1992). Libro di testo di biochimica: con correlazioni cliniche.
- Garrett, r. H., & Grisham, C. M. (2008). Biochimica. Thomson Brooks/Cole.
- McGry, J. D., Mannaerts, g. P., & Foster, D. W. (1977). Un possibile ruolo per malonil-CoA nella regolazione dell'ossidazione e della chetogenesi degli acidi grassi epatici. The Journal of Clinical Investigation, 60(1), 265-270.
- Melo, v., Ruiz, v. M., & Cuamatzi, o. (2007). Biochimica dei processi metabolici. Reverte.
- Nelson, d. L., Lechinger, a. L., & Cox, m. M. (2008). Principi di biochimica Lechinger. Macmillan.
- Pertierra, a. G., Gutiérrez, c. V., E altri, c. M. (2000). Fondamenti di biochimica metabolica. Tébar editoriale.
- Voet, d., & Voet, J. G. (2006). Biochimica. Ed. Pan -American Medical.
- « Colazione continentale cosa è e quali cibi include?
- Proprietà, rischi e usi del perossido di calcio (CaO2) »

