Benzil idrogeno Bencil, carbocazioni, radicali benzilici

- 2506
- 378
- Benedetta Rinaldi
Lui Benchilo o benzil È un gruppo sostitutivo comune in chimica organica la cui formula è c6H5Cap2- o bn-. Strutturalmente è semplicemente costituito dall'unione di un gruppo di metilene, Cho2, Con un gruppo fenilico, C6H5; Cioè un SP3 Collegato direttamente a un anello di benzene.
Pertanto, il gruppo Benchilo può essere visto come un anello aromatico attaccato a una piccola catena. In alcuni testi è preferito l'uso dell'abbreviazione BN invece di C6H5Cap2-, Riconoscerlo facilmente in qualsiasi composto; Soprattutto quando è collegato a un atomo di ossigeno o azoto, O-BN o NBN2, rispettivamente.
 Gruppo Bencilo. Fonte: Ingraralhaosului [dominio pubblico]
Gruppo Bencilo. Fonte: Ingraralhaosului [dominio pubblico] Questo gruppo è anche implicitamente in una serie di composti ampiamente noti. Ad esempio, in acido benzoico, C6H5COOH, potrebbe essere considerato come un benchilo la cui auto carbone3 ha subito un'ossidazione esaustiva; o benzaldeide, c6H5Cho, di ossidazione parziale; e alcool benzilico, c6H5Cap2Oh, ancora meno ossidato.
Un altro esempio in qualche modo ovvio di questo gruppo è a Tolueno, c6H5Cap3, che può subire un certo numero di reazioni a seguito dell'insolita stabilità derivante da radicali o carbocazioni benziliche. Tuttavia, il gruppo Bencilo serve a proteggere i gruppi OH o NH2 di reazioni che modificano indesamente il prodotto per sintetizzare.
[TOC]
Esempi di composti con Grupo Benchilo
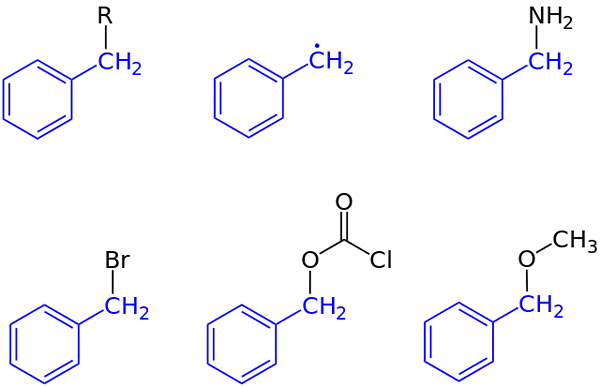 Composti del gruppo Bencilo. Fonte: Jü [dominio pubblico]
Composti del gruppo Bencilo. Fonte: Jü [dominio pubblico] Nella prima immagine, è stata mostrata la rappresentazione generale di un composto con un gruppo Bencil: C6H5Cap2-R, dove r può essere qualsiasi altro frammento molecolare o atomo. Pertanto, la R variabile può ottenere un numero elevato di esempi; Alcuni semplici, altri solo per una regione specifica di una struttura o un set maggiore.
L'alcool benzilico, ad esempio, deriva dalla sostituzione di R con OH: C6H5Cap2-OH. Se invece di oh è il gruppo NH2, Quindi sorge il composto di Bencelamina: C6H5Cap2-NH2.
Può servirti: boroidride di sodio (NABH4): struttura, proprietà, usiSe l'atomo che sostituisce R è BR, il composto ha avuto origine il bromuro di banco: c6H5Cap2-BR; R di co2CL ha origine un estere, clorocarbonato da banco (o carrobenzoxil cloruro); e Och3 Origina l'etere metilico benzil, c6H5Cap2-Och3.
Anche (sebbene non correttamente), R può essere assunto da un elettrone solitario: il radicale benzilico, c6H5Cap2·, Prodotto del rilascio del radicale R ·. Un altro esempio, sebbene non sia incluso nell'immagine, è il fenilacetonitrile o il cianuro di Benchilo, C6H5Cap2-Cn.
Ci sono composti in cui il gruppo Benchilo rappresenta a malapena una regione specifica. Quando è così, l'abbreviazione di BN viene solitamente utilizzata per semplificare la struttura e le sue illustrazioni.
Benzil idrogeni
I composti di cui sopra hanno in comune non solo l'anello aromatico o fenilico, ma anche i benzil idrogeni; Questi sono quelli che appartengono al carbonio spo3.
Tali idrogeni possono essere rappresentati come: bn-ch3, Bn-ch2R o bn-chr2. Il composto BN-CR3 Manca di benzil idrogeno e quindi la sua reattività è inferiore a quella degli altri.
Questi idrogeni sono diversi da quelli che sono generalmente collegati a una SP a carbonio3.
Ad esempio, considera metano, Cho4, che può anche essere scritto come Cho3-H. Per rompere il collegamento CHO3-H In una rottura eterolitica (formazione radicale), una certa quantità di energia (104kj/mol) deve essere fornita.
Tuttavia, energia per la stessa rottura vincolante C6H5Cap2-H è inferiore rispetto a quello del metano (85 kJ/mol). Essendo meno energia, implica che il radicale c6H5Cap2· È più stabile di Cho3·. Lo stesso accade in misura maggiore o minore con altri benzil idrogeni.
Di conseguenza, gli idrogeni benzilici sono più reattivi quando generano radicali o carbocazioni più stabili di quelle causate da altri idrogeni. Perché? La domanda viene data risposta nella sezione seguente.
Può servirti: acido benzoico (C6H5COOH)Carbocazioni e radicali benzyici
Il radicale C era già considerato6H5Cap2·, Carbocalizzazione benzilico mancante: C6H5Cap2+. Nel primo c'è un elettrone scomparso e solitario, e nel secondo una carenza elettronica. Le due specie sono molto reattive e rappresentano composti transitori da cui hanno origine i prodotti finali della reazione.
Carbon sp3, Dopo aver perso uno o due elettroni per formare rispettivamente il radicale o il carbocalizzazione, è possibile adottare l'ibridazione SP2 (piano trigonale), in modo che esiste la minimo possibile repulsione tra i suoi gruppi elettronici. Ma se diventa SP2, Come i carboni dell'anello aromatico, può verificarsi una coniugazione? La risposta è si.
Risonanza nel gruppo Bencilo
Questa coniugazione o risonanza è il fattore chiave per spiegare la stabilità di queste specie benziliche o Bencil. Nell'immagine seguente è illustrato un tale fenomeno:
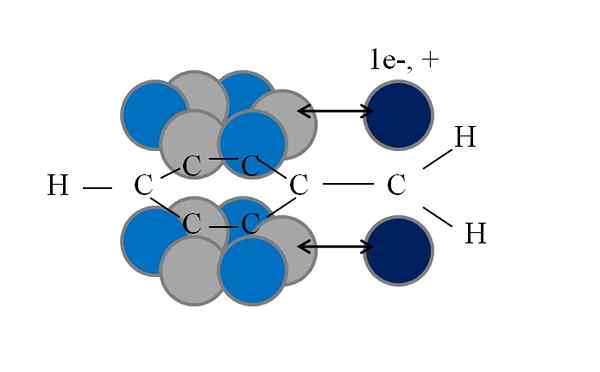 Coniugazione o risonanza nel gruppo Benchilo. Gli altri idrogeni sono stati omessi per semplificare l'immagine. Fonte: Gabriel Bolívar.
Coniugazione o risonanza nel gruppo Benchilo. Gli altri idrogeni sono stati omessi per semplificare l'immagine. Fonte: Gabriel Bolívar. Si noti che dove uno dei benzil idrogeni era un orbitale P Con un elettrone scomparso (radicale, 1e-) o vuoto (carbocalizzazione, +). Come si può vedere, questo orbitale P È parallelo al sistema aromatico (cerchi grigi e blu), con la doppia freccia che indica l'inizio della coniugazione.
Pertanto, sia l'elettrone scomparso che il carico positivo possono essere trasferiti o dispersi dall'anello aromatico, poiché il parallelismo dei suoi orbitali lo favorisce geometricamente. Tuttavia, questi non si trovano in nessun orbitale P dell'anello aromatico; Solo in coloro che appartengono ai carboni in posizioni orto e per il CH2.
Può servirti: analisi quantitativa in chimica: misurazioni, preparazioneQuesto è il motivo per cui i cerchi blu chiari si distinguono sopra i grigi: in essi la densità negativa o positiva del radicale o del carbocalizzazione è concentrata, rispettivamente.
Altri radicali
Vale la pena ricordare che questa coniugazione o risonanza non può verificarsi nei carboni SP3 più distante dall'anello aromatico.
Ad esempio, radicale C6H5Cap2Cap2· È molto più instabile perché l'elettrone scomparso non può essere coniugato con l'anello quando il gruppo è archiviato2 Nel mezzo e con l'ibridazione SP3. Lo stesso vale per C6H5Cap2Cap2+.
Reazioni
In sintesi: i benzil idrogeni sono soggetti a reagire, generando un radicale o un carbocalizzazione, che termina a sua volta causando il prodotto finale della reazione. Pertanto, reagiscono attraverso un meccanismo SN1.
Un esempio è costituito da bromazione di toluene sotto radiazione ultravioletta:
C6H5Cap3 + 1/2br2 => C6H5Cap2Br
C6H5Cap2BR + 1/2BR2 => C6H5Chbr2
C6H5Chbr2 + 1/2br2 => C6H5Cbr3
In effetti, in questa reazione ci sono Br · Radicals.
D'altra parte, il gruppo Benchilo stesso reagisce per proteggere i gruppi OH o NH2 In una semplice reazione di sostituzione. Pertanto, un alcool ROH può essere "benzilad" usando bromuro di benchilo e altri reagenti (koh o nah):
Roh + bnbr => robn + hbr
Robn è un benzil etere, a cui il suo gruppo OH iniziale può essere restituito se è sottoposto a un mezzo riduttivo. Questo etere deve rimanere invariato mentre altre reazioni vengono eseguite nel composto.
Riferimenti
- Morrison, r.T. E boyd, r. N. (1987). Chimica organica. (5a edizione). Addison-Wesley Iberoamericana.
- Carey, f. A. (2008). Chimica organica. (6a edizione). McGraw-Hill, Intermerica, Editor S.A.
- Graham Solomons t.W., Craig b. Frigorifero. (2011). Chimica organica. Ammine. (10a edizione.). Wiley Plus.
- Wikipedia. (2019). Gruppo benzilico. Recuperato da: in.Wikipedia.org
- Dottore. Donald L. Robertson. (5 dicembre 2010). Fenil o benzil? Recuperato da: casa.Miracosta.Edu
- Gamini Gunawardena. (12 ottobre 2015). Carbocalizzazione benzilica. Chimica librettexts. Recuperato da: Chem.Librettexts.org
- « Spiegazione della proporzionalità composita, tre regole composte, esercizi
- Funzioni del sistema ematopoyetico, tessuti, istologia, organi »

