Caratteristiche, preparazione e applicazioni di Timolphhalein
- 2178
- 589
- Rufo Longo
IL Timolphthalein È un indicatore di pH il cui nome scientifico è: 3,3-bis [4-idrossi-2-metil-5- (1-metil) fenil] -1 (3H) -isobenzofuranone e la sua formula chimica è c è c è c è c28H30O4. È sintetizzato dall'anidride ftalica e dalla timol.
Questo indicatore di pH ha proprietà molto peculiari, perché a pH estremamente basso è rosso intenso (pH < 0). Posteriormente hay un amplio rango de pH en donde es completamente incoloro (pH 1 - 9,2), con un rango de viraje entre 9,3 a 10,5 donde puede cambiar a azul, mientras que por encima de 10,5 es azul intenso.
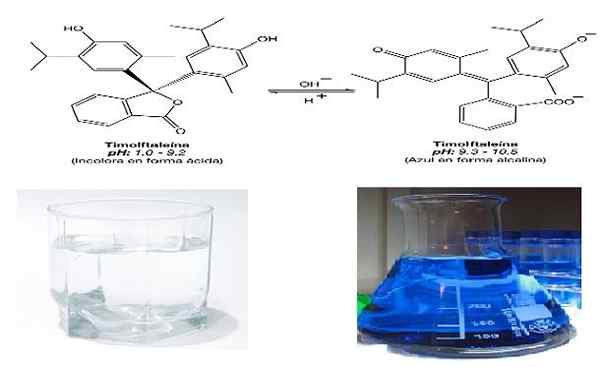
 Struttura chimica della timolphthalein in pH acido (incolore) e pH alcalino (blu intenso). Fonte: DannyBalita [CC BY-SA 4.0 (https: // creativeCommons.Org/licenze/by-sa/4.0)]/pxhere.com
Struttura chimica della timolphthalein in pH acido (incolore) e pH alcalino (blu intenso). Fonte: DannyBalita [CC BY-SA 4.0 (https: // creativeCommons.Org/licenze/by-sa/4.0)]/pxhere.com Tra le sue applicazioni è fungere da indicatore di base acido in alcune reazioni chimiche. Viene anche usato come cromogeno in alcune reazioni colorimetriche in cui viene valutata l'attività enzimatica. Ad esempio, nella determinazione della fosfatasi alcalina.
Per quanto riguarda la tossicità, è meno dannoso di altri indicatori di pH, classificati dalla National Fire Protection Association (NFPA) come livello 1 in relazione alla sua influenza sulla salute; Ciò significa che non è cancerogeno o mutagenico.
Né ha una tossicità specifica nei confronti di qualsiasi organo target; cioè, rappresenta un basso rischio di aggressività sanitaria. Tuttavia, il contatto diretto con la pelle e le mucose può produrre una leggera irritazione.
D'altra parte, in termini di infiammabilità è classificato come 1 e in termini di reattività come zero.
[TOC]
Caratteristiche
L'indicatore di pH di Timolphthalein nella sua forma solida è una polvere bianca, nel suo stato liquido è un rosso intenso a pH inferiore a zero, incolore a pH 1-9,2 e blu sopra 10,5. La sua massa molare è di 430,54 g/mol, con un punto di fusione di (258 ° C), mentre il punto di ebollizione varia da 248-252 ° C. La densità è 0.92 g/ml a 25 ° C
Può servirti: striscio batterico: cosa è, caratteristiche e preparazioneÈ insolubile in freddo e solubile in etanolo. Non è una sostanza esplosiva.
La cura della cautela, durante il trasporto, lo stoccaggio e la manipolazione devono essere tenute lontane dai forti ossidanti.
Preparazione
L'indicatore di pH della timolphhalein viene generalmente utilizzato per una concentrazione dello 0,1% per analisi volumetriche. Per fare ciò, dobbiamo procedere come segue:
- Pesare 100 mg di timolphthalein e dissolversi a 100 ml di alcol etilico al 95%.
Può anche essere preparato come segue:
- Pesare 100 mg di timolphthalein e dissolversi in 60 ml di alcool assoluto e aggiungere 40 ml di acqua distillata.
- Conservare a temperatura ambiente (15 - 25 ° C). È importante che il luogo di stoccaggio sia fresco, ventilato e senza umidità.
Applicazioni
Determinazione della fosfatasi alcalina
Nel determinare questo test esiste una tecnica basata sull'azione idrolitica che la fosfatasi alcalina sulla timolphthalein monofosfato. Se è presente la fosfatasi alcalina, idrolizza la timolftaleina monofosfato, liberando la timoltaleina.
Questo produce una colorazione blu alcalina pH. L'attività enzimatica della fosfatasi alcalina è direttamente proporzionale all'intensità del colore formato. L'assorbanza viene letta a 590 nm.
Determinazione dell'antigene prostatico (PSA)
In questo senso, Shao F e collaboratori nel 2018 hanno sviluppato una tecnica colorimetrica in cui usano nanoparticelle di silice mesoporosa che catturano le molecole di timolftaleina, che sono fortemente unite dalla presenza di feniltimetiloxisilaan.
A loro volta, queste nanoparticelle sono state coperte di polietilemina (PEI), favorendo l'unione dell'anticorpo anti-PSA secondario.
D'altra parte, il campione del paziente è stato immobilizzato su una targa; E quando contatti le nanoparticelle presenti al PSA, si unirà agli anticorpi. Le nanoparticelle che non sono unannali saranno eliminate.
Può servirti: flora e fauna della Sierra ecuadoriana: specie rappresentativeSuccessivamente, la timolphthalein verrà facilmente rilasciata aggiungendo una soluzione alcalina, che genera una colorazione blu. Il grado di colore è direttamente proporzionale alla concentrazione di PSA.
Determinazione dell'attività dell'enzima arginina chinasi o fosfoquinasi
Usando l'indicatore di pH della timolphhalein, è possibile determinare l'attività enzimatica della chinasi arginina. Il test si basa su quanto segue:
L'enzima di arginina chinasi è la fosfotransferasi che partecipa alla formazione di fosfoarginina., Come rivelato nella seguente reazione chimica:
 Fonte: “Arginina chinasi."Wikipedia, enciclopedia gratuita. 10 lug 2018, 13:49 UTC. 20 maggio 2019, 03:58 Wikipedia.org/
Fonte: “Arginina chinasi."Wikipedia, enciclopedia gratuita. 10 lug 2018, 13:49 UTC. 20 maggio 2019, 03:58 Wikipedia.org/ Se questa reazione viene eseguita davanti all'indicatore di pH della timolphhalein, è possibile misurare l'attività enzimatica. Ciò è possibile in base alla seguente spiegazione: la reazione si verifica in un pH alcalino, in cui la timolphhalein mostrerà il suo colore blu.
L'attività enzimatica è misurata dallo sbiadimento del colore riflesso dalla diminuzione dell'assorbanza a 575 nm, perché man mano che l'enzima agisce vengono rilasciati protoni (H+), che acidifica il mezzo.
Questo fa perdere il colore a Timolphthalein una volta che si avvicina all'area di svolta. Se il pH raggiunge i valori inferiori a 9.2, diventa completamente incolore.
Pertanto, l'intensità del colore blu è inversamente proporzionale all'attività enzimatica.
Tossicità
Nell'umano
Questo composto è meno tossico della maggior parte degli indicatori di pH, poiché finora gli effetti cancerogeni non sono attribuiti o mutageni. Tuttavia, non è totalmente innocuo: a contatto con la pelle e le mucose possono produrre arrossamento delle aree menzionate.
Può anche produrre reazioni indesiderate se viene ingerito o per inalazione accidentalmente.
Può servirti: flora e fauna di Santiago Del Estero: specie principaliNel caso in cui vi sia un contatto diretto con la pelle e le mucose, l'area interessata deve essere lavata con molta acqua per almeno 15 minuti. E se osservano segni di irritazione, devi andare al centro sanitario più vicino.
Ecco perché l'uso di strumenti di sicurezza come abiti, guanti e lenti di sicurezza durante la manipolazione si consiglia.
Nonostante abbia un basso rischio di infiammabilità, si raccomanda che per prudenza rimanga lontano dagli accendini.
Impatto sull'ambiente
Nonostante sia meno tossico per la salute umana, è tossico per gli ambienti acquatici, influenzando gli organismi che si trovano lì. Inoltre, ha un'alta potenza di bioacumulazione e a lungo termine è possibile che si possano formare prodotti di degradazione dannosi.
Pertanto, si dovrebbe evitare che questo prodotto raggiunga le acque superficiali o sotterranee, poiché influirebbe sull'acqua potabile.
In questo senso, i laboratori che usano questo indicatore devono eliminare i loro rifiuti in conformità con i regolamenti in vigore in ciascun paese.
Riferimenti
- Pizzani P, Godoy S, León M, Rueda E, Castañeda M, Arias A. Effetto dell'aumento delle concentrazioni di fosforo sull'attività degli enzimi fosfatasi di fitasi e alcalina nell'epitelio intestinale di giovani pecore. Rev. Scienziato. (Maracaibo). 2008,18 (1): 59-64. Disponibile su: scielo.org.
- “Timolphthalein." Wikipedia, Enciclopedia gratuita. 22 febbraio 2019, 04:40 UTC. Il 19 maggio 2019, 22:20, è.Wikipedia.org.
- Shao F, Zhang L, Jiao L, Wang X, Miao L, Li H, Zhou F. Saggio immunosornge privo di enzimi di antigene specifico della prostata amplificato rilasciando molecole indicatore di pH entroptate in nanoparticelle di silice mesoporosa. Chem. 2018; 17; 90 (14): 8673-8679.
- Yu Z, Pan J, Zhou HM. Un test diretto a pH continuo-spettrofotometrico per l'attività dell'arginina chinasi. PEPT Lett Protein. 2002; 9 (6): 545-52.
- Scharlau. Scheda di sicurezza di Timolphthalein. 2013. Disponibile su: Javeriana.Edu.co
- Scheda di sicurezza di Timolphthalein. MSDS. National University of Heredia, Costa Rica. Disponibile su: Timolphthalein%20 (3).
- “Arginina chinasi." Wikipedia, Enciclopedia gratuita. 10 lug 2018, 13:49 UTC. 20 maggio 2019, 03:58 è.Wikipedia.org.
- « Caratteristiche del rosso metile, preparazione e applicazioni
- Caratteristiche, esempi ed esercizi di vettori simultanei »

