Soluzione insatura
- 4285
- 1094
- Brigitta Ferrari
 Nella soluzione insatura, la metà solvente è ancora in grado di dissolvere più soluto
Nella soluzione insatura, la metà solvente è ancora in grado di dissolvere più soluto Cos'è una soluzione insaturata?
UN soluzione insatura È tutta quella soluzione in cui il mezzo solvente è ancora in grado di dissolvere più soluto. Questo mezzo è generalmente liquido, sebbene può anche essere gassoso. Per quanto riguarda il soluto, è un conglomerato di particelle solide o gassose.
E per quanto riguarda i soluti liquidi? In tal caso, la soluzione è omogenea fintanto che entrambi i liquidi sono miscibili. Un esempio di ciò è l'aggiunta di alcol etilico all'acqua; I due liquidi con le loro molecole, Cho3Cap2Oh e h2Oppure, sono miscibili perché formano ponti idrogeno (scegli3Cap2OH, OH2).
Tuttavia, se il diclorometano si mescola (scegli2Cl2) e acqua, questi formeranno una soluzione con due fasi: una acquosa e l'altra organica. Questo perché Choles di CH2Cl2 e h2O interagire in modo molto debolmente, quindi alcuni scivoli sugli altri, risultando in due liquidi impossibili.
Una goccia minima di Cho2Cl2 (soluto) abbastanza per saturare l'acqua (solvente). Se, al contrario, potessero formare una soluzione insatura, sarebbe vista una soluzione completamente omogenea.
Per questo motivo, solo i soluti solidi e gassosi possono generare soluzioni insature.
Cos'è una soluzione insaturata?
In una soluzione insatura, le molecole di solvente interagiscono con l'efficacia in modo tale che le molecole di soluto non possano formare un'altra fase.
Ciò significa che le interazioni con soluto solvente superano, date le condizioni di pressione e temperatura, interazioni con soluzione soluto.
Una volta che le interazioni del soluto aumentano, "orchestrano" la formazione di una seconda fase. Ad esempio, se il mezzo di solvente è un liquido e il soluto è solido, il secondo si dissolverà nel primo a formare una soluzione omogenea, fino a quando non appare una fase solida, che non è altro che il soluto precipitato.
Può servirti: polimetilmetacrilatoQuesto precipitato è dovuto al fatto che le molecole di soluto riescono a essere raggruppate dalla loro natura chimica, intrinseca alla loro struttura o collegamenti. Quando ciò accade, si dice che la soluzione sia satura di soluto.
Pertanto, una soluzione di soluto insaturi è costituita da una fase liquida senza precipitato. Mentre se il soluto è gassoso, una soluzione insatura deve essere libera dalla presenza di bolle (che non sono altro che gruppi di bevande analcoliche).
Effetto di temperatura
La temperatura influenza direttamente il grado di insaturazione di una soluzione rispetto a un soluto.
Ciò può essere principalmente dovuto a due ragioni: l'indebolimento delle interazioni del soluto di soluto a causa dell'effetto termico e l'aumento delle vibrazioni molecolari che aiutano a disperdere le molecole del soluto.
Se un mezzo di solvente è considerato come uno spazio compatto nei cui fori sono alloggiate le molecole di soluto, la temperatura aumenta le molecole vibrate aumentando la dimensione di questi fori; in modo tale che il soluto possa farsi strada in altre direzioni.
Solidi insolubili
Tuttavia, alcuni soluti hanno interazioni così forti, che le molecole di solvente sono appena in grado di separarli.
Quando è così, una concentrazione minima di detto soluto disciolto è sufficiente per far sì che si precipitasse, e quindi è un solido insolubile.
I solidi insolubili, formando una seconda fase solida che differisce dalla fase liquida, generano poche soluzioni insature.
Ad esempio, se 1L del liquido A può dissolvere solo 1 g di b senza precipitare, allora quando si mescola 1L di A con 0.5 g di B genereranno una soluzione insatura.
Può servirti: idrocolideAllo stesso modo, un grado di concentrazioni comprese tra 0 e 1 g di B formano anche soluzioni insature. Ma dopo 1g, B precipiterà. Quando ciò si verifica, la soluzione passa da insatura a satura da B.
Se una soluzione satura con 1 viene presentata al riscaldamento.5 g di b, il calore aiuterà lo scioglimento del precipitato. Tuttavia, se c'è molto B precipitato, il calore non può dissolverlo.
In tal caso, un aumento della temperatura evaporrebbe semplicemente il solvente o il liquido.
Esempi di soluzione insatura
Gli esempi di soluzioni insature sono numerosi, poiché dipendono dal solvente e dal soluto. Ad esempio, per lo stesso liquido A e altri soluti C, D, E ... Z, le loro soluzioni saranno insature fintanto che non precipitano o formaranno una bolla (se sono soluti gassosi).
-Il mare può contribuire con due esempi. L'acqua di mare è un'enorme soluzione di salvataggio. Se metti a bollire un po 'di quest'acqua, si noterà che è insatura in assenza di sale precipitato. Tuttavia, man mano che l'acqua evapora, gli ioni disciolti iniziano a essere raggruppati, lasciando il salino attaccato alla pentola.
-Un altro esempio è lo scioglimento dell'ossigeno nell'acqua dei mari. La molecola di O2 Frank le profondità del mare abbastanza da respirare la fauna marina, anche se è poco solubile.
Per questo motivo è comune osservare le bolle di ossigeno che emergono in superficie; di cui, alcune molecole riescono a dissolversi.
Una situazione simile si verifica con la molecola di anidride carbonica, CO2. A differenza di O2, Il co2 È leggermente più solubile perché reagisce con l'acqua per formare acido carbonico, h2Co3.
Può servirti: sistemi di materialiDifferenza con soluzione satura
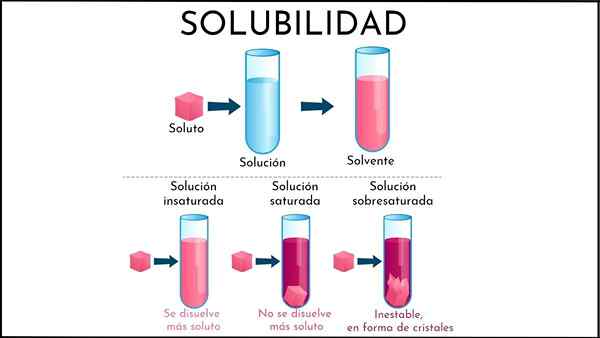
Riassumendo i nuovi spiegati, quali sono le differenze tra una soluzione insatura e satura? Innanzitutto, l'aspetto visivo: una soluzione insatura è costituita da una singola fase. Pertanto, non ci dovrebbe essere presenza di solido (fase solida) o bolla (fase di soda).
Inoltre, le concentrazioni di soluto in una soluzione insatura possono variare fino a formare un precipitato o una bolla. Mentre sono in soluzioni sature e bifasiche (liquido-solido o liquido-gassoso), la concentrazione di soluto disciolto è costante.
Perché? Poiché le particelle (molecole o ioni) che compongono il precipitato, stabiliscono un equilibrio con quelle che si trovano sciolte nel solvente:
Particelle di particelle disciolte precipitate
Molecole di bolle disciolte
Questo scenario non è contemplato in soluzioni insature. Quando si tenta di dissolvere più soluto in una soluzione satura, l'equilibrio si sposta a sinistra; alla formazione di più precipitati o bolle.
Perché in soluzioni insature questo equilibrio (saturazione) non è stato ancora stabilito (saturazione) può "conservare" più solido o gas.
Intorno a un alghe nel fondo del mare c'è ossigeno disciolto, ma quando le bolle di ossigeno nascono dalle sue foglie, significa che si verifica la saturazione del gas; Altrimenti, le bolle non verrebbero osservate.
Riferimenti
- Chimica generale. materiale per l'insegnamento. Lima: Pontificale Catholic University of Peru. Recuperato da: Corinth.Pucp.Edu.PE
- Helmestine, Anne Marie, PH.D. (2018). Definizione della soluzione insatura. Recuperato da: Thoughtco.com
- TutorVista (s.F.). Soluzione insatura. Tratto da: chimica.TutorVista.com
- Chimica librettext (s.F.). Tipi di saturazione. Recuperato da: Chem.Librettexts.org
- Nadine James. (2018). Soluzione insatura: definizione ed esempio. Recuperato da: studio.com

