Caratteristiche di safranina, uso, tecniche, tossicità
- 3458
- 1029
- Kayla Serr
IL Safranina È un colorante meriqinoide, chiamato per possesso nella sua struttura chimica di 2 anelli di benzene e 2 anelli quinoidi, quest'ultimo è quello che fornisce il colore rosso.
È anche chiamato safranina o dimetil rosso di base nella sua forma sommaria, poiché il suo nome scientifico è 3.7-diamino-2,8-dimetil-5- fenil-fenil-fenillventiH19N4 Cl.
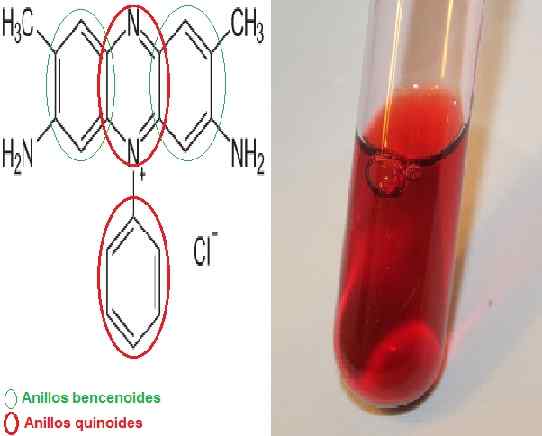
 Struttura chimica della safranina che indica gli anelli di benzene e chinoide/ soluzione acquosa di safranina. Fonte: Neurotoger [dominio pubblico] a cura di MSC. Marielsa Gil/Lhchem [CC BY-SA 3.0 (https: // creativeCommons.Org/licenze/by-sa/3.0)]
Struttura chimica della safranina che indica gli anelli di benzene e chinoide/ soluzione acquosa di safranina. Fonte: Neurotoger [dominio pubblico] a cura di MSC. Marielsa Gil/Lhchem [CC BY-SA 3.0 (https: // creativeCommons.Org/licenze/by-sa/3.0)] C'è una variante chiamata trimetile-safraina ma non c'è differenza significativa tra le due sostanze.
La safranina è un colorante monocromatico e, secondo le caratteristiche della formula chimica, è una sostanza di carica positiva. Pertanto, ha affinità con strutture caricate negativamente. Queste strutture saranno tinte di rosso.
Questa proprietà fornisce applicabilità in molte tecniche istologiche per tingere varie strutture cellulari, sia da organismi eucariotici che procariotici.
La safranina viene utilizzata come colorante a contrasto in tecniche di uso di routine importanti e ben note in batteriologia. Queste tecniche sono: colorazione di Gram-Hucker, colorazione Schaeffer Fulton per spore o capsule batteriche colorate, tra gli altri.
[TOC]
Caratteristiche
Il colore dello zafferano (spezie ottenute dagli stigmi del fiore di Crocus sativ) è stata l'ispirazione per posizionare il nome di questa tintura. Dal termine zafferano arriva il nome di safranina. Ciò è dovuto alla grande somiglianza tra il colore dello zafferano e la colorazione che questo colorante fornisce.
La safranina si ottiene come cristalli o polvere, entrambe le presentazioni sono solubili in acqua. La tintura di safranina non ha un odore. Colorare le strutture rosse. Le strutture che attirano il colorante safranino sono chiamate safranofili.
Strutturalmente, la safranina è complessa, ha due anelli di benzene alle estremità e al centro si trovano gli anelli di due quinoidi dove si trova il catione n+. Il centro della struttura è il sistema responsabile della fornitura di colore. Con questa caratteristica questo colorante è classificato nella categoria II.
Utilizzo
La safranina viene utilizzata per tingere varie strutture. Soprattutto evidenzia le cellule di Kulchitsky presenti nel tratto gastrointestinale, chiamate anche cellule di Enterocromofines.
È in grado di tingere i microrganismi appartenenti alla famiglia Rickettsiaceae. Allo stesso modo, è usato in varie tecniche, come il metodo di Koster, una modificata utilizzata per la colorazione dei batteri di genere Brucella.
D'altra parte, la safranina viene utilizzata nella tecnica di colorazione delle spore di Schaeffer Fulton e nella colorazione di Gram-Hucker. In entrambe le tecniche, Safranine funziona come un colorante a contrasto.
Può servirti: indianoNel primo le spore prendono il colore del verde della malachite e il resto delle strutture sono rossi dalla safranina. Nel secondo, i batteri gram negativi perdono il colore del vetro viola nella fase di scolorimento, quindi la safranina è colui che colora i batteri gram negativi di rosso.
Inoltre, la safranina viene utilizzata in batteriologia per preparare l'agar Brucella con una diluizione di safranina 1: 5000. Questo mezzo serve a differenziare la specie Brucella Suis del resto della specie. Brucella melitensis E Brucella abortus crescere in questo mezzo ma B. Suis È inibito.
Nel campo agroindustriale, la safranina è stata utilizzata al 2,25% e diluito 1:10 per tingere i campioni di stelo dalla pianta di canna da zucchero.
Questa pianta è comunemente influenzata dai batteri Leifsonia Xyli sottotitoli. XILI, chi danneggia lo xilema della pianta. Gli steli tinti vengono valutati per determinare la funzione dei vasi di xilema.
Tecniche nell'area della batteriologia
Colorazione castañeda per colorazione rIckettsias
Uno striscio di sangue o tessuto viene posizionato in una soluzione tampone (smorzamento del fosfato pH 7,6). È consentito asciugare spontaneamente e quindi coperto di blu di metilene per 3 minuti e contratto con safranina. Rickettsias colorato blu, in contrasto con lo sfondo rosso.
Colorazione koster modificata per Brucella
Viene eseguito uno striscio e la flamea in più per la fissazione. Successivamente, è coperto da una miscela di 2 parti di saturi saturi di safranina con 3 parti di soluzione KOH 1 mol/L, per 1 minuto. Viene eseguito un lavaggio con acqua distillata e 1% di blu di metilene Fenado.
Se il campione contiene batteri di genere Brucella Questi saranno osservati arancione in uno sfondo blu.
Colorazione delle capsule batteriche
Viene eseguita una miscela di sospensione batterica con inchiostro cinese e safranina. Un alone rossastro sarà osservato al microscopio attorno a ciascuna capsula batterica con uno sfondo nero.
Può servirti: sostanze pureColorazione di spore Schaeffer Fulton
Viene eseguita una sospensione batterica estesa. Quindi è fissato per riscaldare. È coperto di verde malachite al 5%, spesso si infila fino all'emissione di vapori. Il processo viene ripetuto per 6-10 minuti. Infine, viene lavato con acqua e assunto con safranina allo 0,5% per 30 secondi. I bacilli sono tinti di rosso e le spore verdi.
Colorazione Gram-Hucker
Viene eseguita una sospensione batterica estesa e fissata al calore. La lamina con vetro viola di 1 minuto è coperta. Quindi Lugol viene posizionato come una soluzione mordant per 1 minuto. Successivamente, è scolorito con alcol di acetone e infine assunto con safranina per 30 secondi.
I batteri gram positivi sono tinti blu viola e batteri gram negativi di rosso.
Alcuni laboratori hanno smesso di usare la tecnica Gram-Hucker per adottare la tecnica Gram-Kopeloff modificata. In quest'ultimo caso, la safranina viene sostituita da Fuchsin di base. Questo perché la safranina macchia debolmente le specie di generi Legionella, Campylobacter E Brucella.
Tecniche nell'area istologica
Colorazione cellulare Kulchitsky (EnterocromoFines)
I tagli tissutali del tratto gastrointestinale con cloruro d'argento sono tinti. Quindi è scolorito con tiosolfato di sodio e infine assunto con safranina.
Le cellule di Kulchitsky si distinguono perché vengono presentate con granuli marroni nerastri.
Colorazione per il rilevamento dell'osteoartrosi
Safranina perché ha un carico positivo, i gruppi di carbossi e solfato di glicosaminoglicani si legano molto bene. Questi fanno parte dei proteoglicani che costituiscono la cartilagine articolare. In questo senso, quando si tinge con safranina o, può essere identificato se c'è o meno una perdita di cartilagine.
La perdita di tessuto cartilagineo può essere misurata attraverso la scala di mankin o anche chiamata scala di osteoartrosi.
La tecnica viene quindi spiegata: il taglio istologico è immerso in un vassoio con la soluzione di ematossilina ferrica di Weigert, quindi viene passata attraverso l'alcool acido e lavato con acqua.
Continua il processo di colorazione immergendo il foglio in verde veloce, lava con acido acetico e ora immerge in safranina o. Per finire il processo, è disidratato usando alcoli a diverse concentrazioni in ordine crescente. L'ultimo passaggio richiede xileno o xilol per il campione per chiarire.
Può servirti: metalloidiI fogli sono condizionati con balsamo del Canada o simili per essere osservati al microscopio.
Con questa tecnica, i nuclei sono tinti di nero, l'osso verde e la cartilagine in cui si trovano i proteoglicani rossi.
TINCION per l'identificazione dei macroalgas
Pérez et al. Nel 2003 hanno proposto una tecnica semplice ed economica per tingere i macroalgas. I campioni sono preparati in tagli istologici con paraffina. I tagli sono fissati con glicerina all'1%, lasciandosi completamente asciutti. Quindi viene posizionato in xilolo per eliminare la paraffina.
Il taglio viene reidratato, facendolo passare attraverso una serie di vassoi che contengono etanolo in diversi gradi di concentrazione (ordine discendente), per 2 minuti in ciascuno.
Successivamente, viene tinto per 5 minuti con una miscela 3: 1 di safranina all'1% con blu di toluidina all'1%, entrambi preparati con etanolo al 50%. La miscela viene aggiunta tre gocce di acido picric che agiscono come mordente.
Quindi diventa di nuovo disidratato attraverso i vassoi di alcol, ma questa volta sale. Infine, viene chiarito con Xilol e il campione viene preparato con il balsamo del Canada da osservare.
Tossicità
Fortunatamente, Safranine è una tintura che non rappresenta un pericolo per coloro che lo manipolano. È un colorante innocuo, non è cancerogeno e non è neanche infiammabile.
In contatto diretto con la pelle o le mucose possono causare un leggero arrossamento dell'area, senza gravi complicanze. Per questo si consiglia di lavare l'area interessata con molta acqua.
Riferimenti
- Garcia h. Colorante di safranina o. Tecnica di salute, 2012; 1 (2): 83-85. Disponibile su: Medicigraphic.com
- Gil m. Colorazione Gram: base, materiali, tecnica e usi. 2019. Disponibile su: Lofede.com
- Gil m. Colorazione delle spore: base, tecniche e usi. 2019. Disponibile su: Lofede.com
- Safranina." Wikipedia, Enciclopedia gratuita. 7 marzo 2017, 10:39 UTC. AGO 2019, 20:49 è.Wikipedia.org
- Pérez-Cortéz S, Vera B, Sánchez C. Tecnica di colorazione utile nell'interpretazione anatomica di Tenuifrons graciliasi E Gracilaria chilensis (Rhodophyta). Bot Act. Venez. 2003; 26 (2): 237-244. Disponibile su: scielo.org.
- Chiesa Aleika, Peralta Esther Lilia, Alvarez Elba, Milián J, Matos Madyu. Rapporto tra la funzionalità dei vasi di xilema e la presenza di Leifsonia Xyli Subp. XILI. Rev. Protezione verdure. 2007; 22 (1): 65-65. Disponibile su: scielo.SLD

