Struttura della piperidina, sintesi, derivati, reazioni
- 1672
- 180
- Lidia Valentini
IL Piperidina È un composto organico la cui formula condensata è (CH2)5NH. È costituito da un'ammina secondaria ciclica, in cui il gruppo amminico, NH, fa parte di un anello esagonale, che è eterociclico, a causa della presenza dell'atomo di azoto.
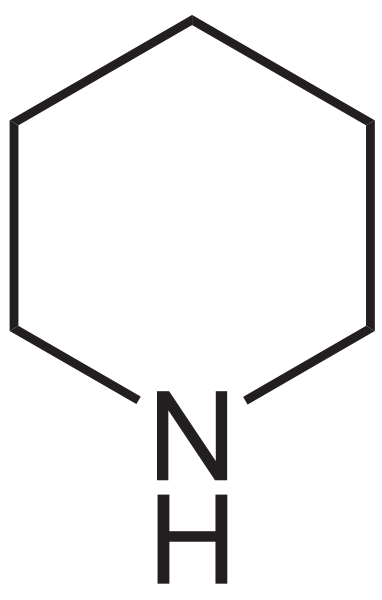
La piperidina diventa la versione azotata del cicloesano. Ad esempio, nota nell'immagine inferiore la formula strutturale di piperidina: è molto simile a quella del cicloesano, con l'unica differenza che uno dei gruppi di metilene, Cho2, è stato sostituito da un NH.
 Formula strutturale di piperidina. Fonte: neurotoger / dominio pubblico
Formula strutturale di piperidina. Fonte: neurotoger / dominio pubblico Il nome curioso di questa ammina deriva dalla parola latina "piper", che significa pepe, perché era nel pepe nero dove per la prima volta è stato trovato e sintetizzato. In effetti, l'aroma della piperidina è confuso da quello di una miscela di pepe e pesce.
Il suo anello esagonale ed eterociclico è anche presentato in molti alcaloidi e farmaci, quindi la piperidina è destinata alla sintesi organica di tali prodotti; come morfina, miniaxidil e simpatia.
[TOC]
Struttura
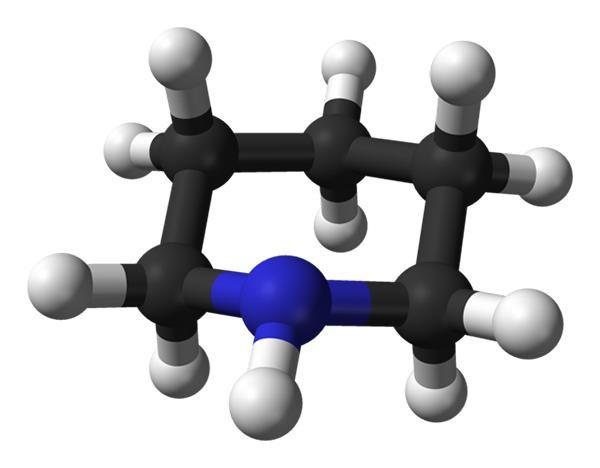 Struttura molecolare della piperidina. Fonte: Benjah-BMM27 / Dominio pubblico
Struttura molecolare della piperidina. Fonte: Benjah-BMM27 / Dominio pubblico Nell'immagine superiore abbiamo la struttura molecolare della piperidina, rappresentata da un modello di sfere e barre. Le sfere nere, corrispondenti agli atomi di carbonio, costituiscono lo scheletro che sarebbe lo stesso del cicloesano se non è per l'atomo di azoto, quello della sfera bluastra.
Qui puoi vedere le cinque unità di metilene, CH2, e il modo in cui sono disposti i loro atomi di idrogeno. Allo stesso modo, il gruppo amminico secondario è chiaramente osservato, il cui azoto elettrico contribuisce alla polarità alla molecola.
Può servirti: benefici della chimica per la societàPertanto, la piperidina ha un momento di dipolo permanente, in cui la densità di carico negativa è concentrata attorno a NH.
Avendo la piperidina un momento di dipolo, le sue forze o interazioni intermolecolari sono prevalentemente di tipo dipolo-dipolo.
Tra le interazioni dipolo-dipolo, sono presenti i ponti idrogeno stabiliti dai gruppi NH-NH di molecole di piperidina vicine. Di conseguenza, la coesione di molecole di piperidina in un liquido che bolle a una temperatura di 106 ºC.
Conformazioni
L'anello esagonale della piperidina, così come quello del cicloesano, non è piatto: i suoi atomi di idrogeno si alternano in posizioni assiali (sopra o sotto) ed equatoriale (diretto verso i lati). Pertanto, la piperidina adotta diverse conformazioni spaziali, la sedia è la più importante e stabile.
L'immagine precedente mostra uno dei quattro possibili confFiglieomer in cui l'atomo di idrogeno del gruppo NH si trova nella posizione equatoriale; Mentre la coppia di elettroni non condivise di azoto non si trova in posizione assiale (su, in questo caso).
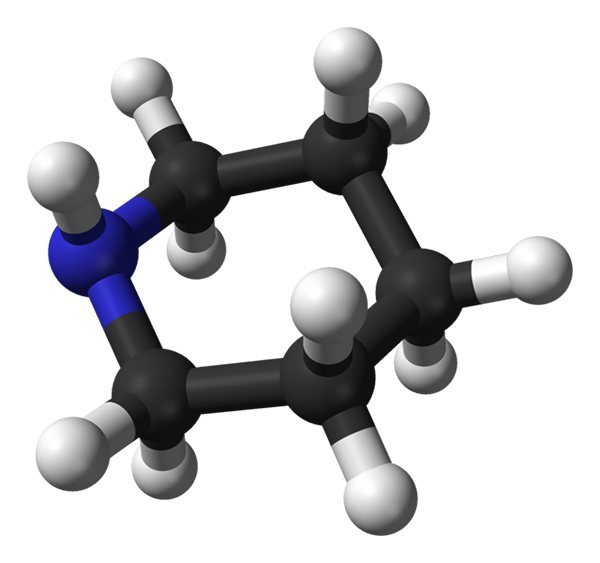 Conformazione assiale di piperidina. L'atomo di idrogeno in posizione assiale aumenta la tensione gemella sull'anello per essere troppo vicino ad altri idrogeni assiali e adiacenti. Fonte: Benjah-BMM27 / Dominio pubblico
Conformazione assiale di piperidina. L'atomo di idrogeno in posizione assiale aumenta la tensione gemella sull'anello per essere troppo vicino ad altri idrogeni assiali e adiacenti. Fonte: Benjah-BMM27 / Dominio pubblico Ora viene mostrato un altro confruero (immagine superiore), in cui questa volta l'atomo di idrogeno del gruppo NH è in posizione assiale (UP); e la coppia di elettroni condivisi né azoto, in posizione equatoriale (a sinistra).
In modo che in totale ci siano quattro conformatori: due con l'idrogeno di NH in posizioni assiali ed equatoriali e altri due in cui le posizioni relative degli elettroni azotati sono variate rispetto alla sedia.
Può servirti: acido seleenidrico (H2SE): cosa è, struttura, proprietà, usiI conformatori in cui l'idrogeno NH è in posizione equatoriale sono i più stabili, perché soffrono di tensioni steriche più basse.
Sintesi
La prima sintesi di piperidina. La piperina sta reagendo con acido nitrico, staccando l'unità eterociclica la cui struttura era già stata rivista.
Tuttavia, alle scale industriali la sintesi della piperidina è preferita dall'idrogenazione catalitica della piridina:
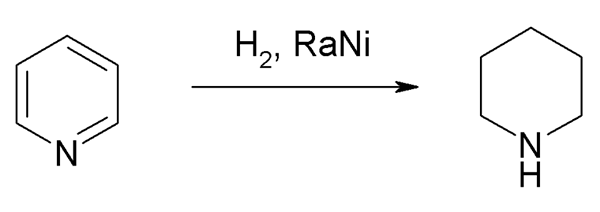 Idrogenazione della piridina per ottenere piperidina. Fonte: Steffen 962 via Wikipedia.
Idrogenazione della piridina per ottenere piperidina. Fonte: Steffen 962 via Wikipedia. Hydogens, h2, Si uniscono all'anello di piridina che rompe il loro sistema aromatico, per il quale è necessario l'aiuto di catalizzatori metallici.
Derivati
Piperina
Molto più importante della stessa piperidina, è la sua unità strutturale, riconoscibile in innumerevoli alcaloidi e sostanze di origine vegetale. Ad esempio, di seguito hai la struttura molecolare della piperina:
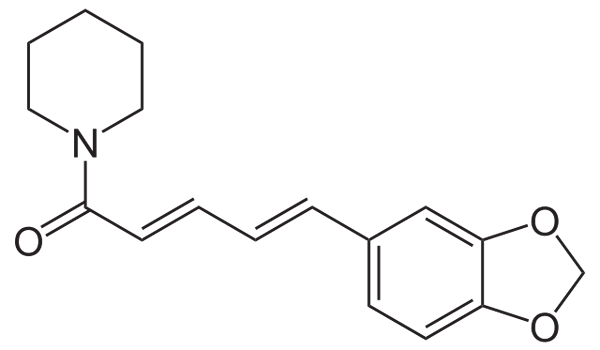 Formula strutturale della piperina. Fonte: Neurotoger via Wikipedia.
Formula strutturale della piperina. Fonte: Neurotoger via Wikipedia. Piperina ha una struttura altamente coniugata; Cioè, ha diversi doppi collegamenti coordinati tra loro che assorbono le radiazioni elettromagnetiche e che in un modo o nell'altro lo rendono un composto non tossico per il consumo umano. In tal caso, il pepe nero sarebbe velenoso.
Coniína
L'anello eterociclico ed esagonale della piperidina si trova anche nel Coní, una neurotossina estratta dalla guarigione, responsabile del suo odore spiacevole e che è stato anche usato per avvelenare. La sua struttura è:
Può servirti: Amonides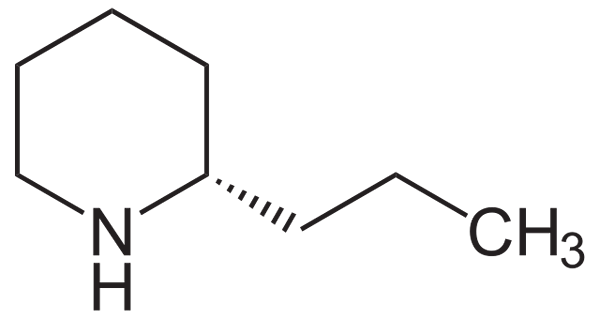 Formula strutturale di coniína. Fonte: neurotoger / dominio pubblico
Formula strutturale di coniína. Fonte: neurotoger / dominio pubblico Si noti che il coniína non è quasi diverso dalla piperidina dalla presenza di un sostituente propil nel carbonio adiacente al gruppo NH.
Pertanto, i derivati della piperidina sono ottenuti sostituendo gli idrogeni dell'anello o l'idrogeno dello stesso gruppo NH, da altri gruppi molecolari o frammenti.
Morfina
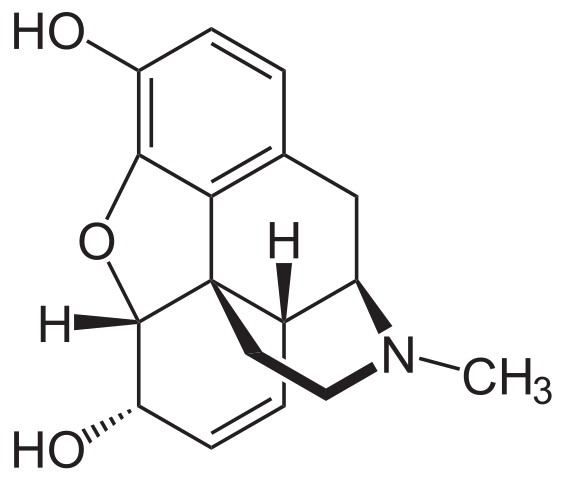 Formula strutturale di morfina. Fonte: neurotoger / dominio pubblico
Formula strutturale di morfina. Fonte: neurotoger / dominio pubblico La morfina è un altro derivato naturale della piperidina. Questa volta l'anello di Piperidina viene fuso con altri anelli e punta fuori dall'aereo, nella direzione dell'osservatore. È identificato perché forma un collegamento con il gruppo CHO3.
Droghe
La piperidina e i suoi derivati sono utilizzati per la progettazione e la sintesi di diversi tipi di farmaci. Pertanto, sono derivati sintetici della piperidina. Tre di loro sono quindi elencati insieme alle rispettive formule strutturali:
 Risperidone, un antipsicotico atipico prescritto per il trattamento di più disturbi mentali. Fonte: fvasconcellos (talk • contributi) / dominio pubblico
Risperidone, un antipsicotico atipico prescritto per il trattamento di più disturbi mentali. Fonte: fvasconcellos (talk • contributi) / dominio pubblico 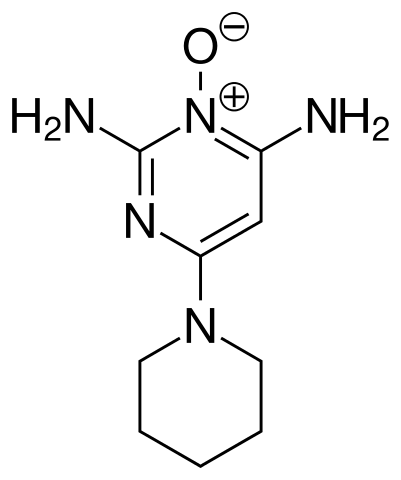 Minoxidil, un vasodilatatore solitamente usato per affrontare l'alopecia. Fonte: vaccinato / dominio pubblico
Minoxidil, un vasodilatatore solitamente usato per affrontare l'alopecia. Fonte: vaccinato / dominio pubblico  Icaridina o picaridina, un repellente per insetti che compone la formulazione delle offerte. Fonte: ArrowsMaster/CC BY-S (https: // creativeCommons.Org/licenze/by-sa/4.0)
Icaridina o picaridina, un repellente per insetti che compone la formulazione delle offerte. Fonte: ArrowsMaster/CC BY-S (https: // creativeCommons.Org/licenze/by-sa/4.0) Riferimenti
- Graham Solomons t.W., Craig b. Frigorifero. (2011). Chimica organica. (10th Edizione.). Wiley Plus.
- Carey f. (2008). Chimica organica. (Sesta edizione). Mc Graw Hill.
- Morrison e Boyd. (1987). Chimica organica. (Quinta edizione). Addison-Wesley Iberoamericana.
- Wikipedia. (2020). Piperidina. Recuperato da: in.Wikipedia.org
- Centro nazionale per le informazioni sulla biotecnologia. (2020). Piperidina. Database PubChem., CID = 8082. Recuperato da: pubchem.NCBI.Nlm.NIH.Gov
- Elsevier b.V. (2020). Piperidina. Scienceirect. Estratto da: ScienceDirect.com
- Harold d. Banche. (1992). Sintesi di piperidina. [PDF]. Recuperato da: app.DICT.mille
- « Struttura del polivinylpirrolidone, proprietà, usi, effetti collaterali
- Struttura di nitrato d'argento (AGNO3), proprietà, usi, tossicità »

