Struttura del pepsinogeno, funzioni, tipi, sintesi
- 3199
- 455
- Lidia Valentini
Lui Pepsinogeno È lo zimogano della pepsina, uno dei principali enzimi idrolitici incaricati di eseguire la digestione delle proteine nello stomaco dei mammiferi. Zimogeni o proenzimi sono precursori enzimatici inattivi, ovvero non sono in grado di catalizzare le reazioni condotte dalle loro forme attive.
La sua attivazione dipende dai cambiamenti nella struttura tridimensionale della proteina che danno origine alla formazione di un sito attivo funzionale. Questi cambiamenti, nella maggior parte dei casi, coincidono con la rottura proteolitica di un segmento proteico.
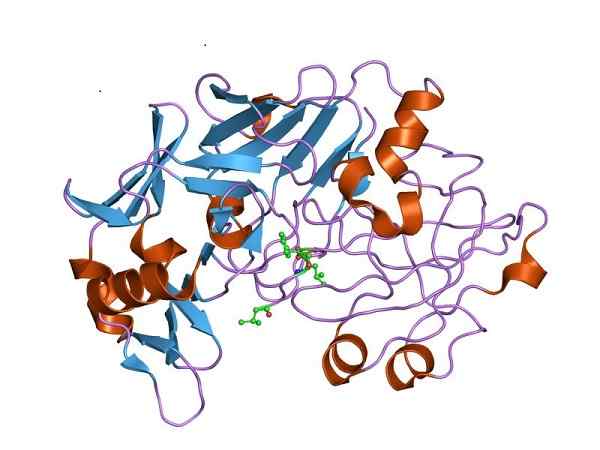
 Struttura tridimensionale della pepsina, la forma cataliticamente attiva di pepsinogeno. Di Jawahar Swaminathan e personale MSD presso l'European Bioinformatics Institute [Public Domain (https: // creativeCommons.Org/licenze/by-sa/4.0)], da Wikimedia Commons
Struttura tridimensionale della pepsina, la forma cataliticamente attiva di pepsinogeno. Di Jawahar Swaminathan e personale MSD presso l'European Bioinformatics Institute [Public Domain (https: // creativeCommons.Org/licenze/by-sa/4.0)], da Wikimedia Commons Pertanto, il pepsinogeno deve sperimentare cambiamenti strutturali per acquisire l'attività della peptidasi richiesta e favorire la digestione delle proteine nello stomaco, dopo l'assunzione di cibo.
[TOC]
Struttura
Il pepsinogeno è una proteina aminoacida 371 appartenente alla grande famiglia di proteinasi aspartiche, caratterizzata dalla presentazione di residui di acido aspartico nel suo centro attivo.
La sua struttura quaternaria è stata determinata per la prima volta per la proteina espressa nei suini attraverso la tecnica di cristallografia a raggi X. Il risultato era simile a quello mostrato dalla forma matura o attiva della proteina, la pepsina.
Pertanto, l'unica differenza trovata è la presenza nel pepsinogeno di un peptide di aminoacidi 44 che si piega sulla fessura del sito attivo. In questa posizione, ostacola l'interazione di questa proteasi con le proteine da degradare.
Questo peptide che verrà clipato per dare origine all'enzima attivo, si trova all'estremità terminale amminica della proteina.
Poiché funziona solo come un limite, l'incapacità del pepsinogeno proteico degradato non è dovuta alle deformazioni strutturali del centro attivo. Al contrario, questo rimane con la stessa conformazione in entrambe le forme dell'enzima.
Può servirti: glucani: struttura, caratteristiche e funzioniIn questo senso, vale la pena notare che la struttura cristallina del pepsinogeno costituisce un modello approssimativo della struttura di altri zimogeni appartenenti alla grande famiglia di proteine aspartiche.
Funzioni
All'inizio della vita, la pepsina (forma attiva di pepsinogeno) è importante per la digestione del latte. Successivamente, la sua funzione è quella di degradare le proteine dietetiche nei loro componenti (aminoacidi) al fine di facilitare il loro facile assorbimento.
Sintesi e secrezione
Il pepsinogeno è sintetizzato dalle cellule principali e dalle cellule fondamentali della mucosa gastrica. Successivamente, è conservato in vescicole secretorie che rimangono nel citoplasma di queste cellule fino al momento in cui è richiesto il loro rilascio.
Pertanto, la secrezione di questo zimogeno è un processo regolato. Il suo rilascio di vescicole, residenti di citosol attraverso l'esocitosi, richiede stimoli ormonali e neurali. L'aumento dei livelli di enzimi gastrici si secernono e gastrina, nonché acetilcolina, colecistochinina, fattore di crescita epidermico e ossido nitrico stimolano la loro sintesi e secrezione.
Inoltre, gli esperimenti condotti con le cellule ATT20, una linea cellulare comunemente usata nello studio delle strade di secrezione nei mammiferi, hanno dimostrato che un aumento dell'AMP ciclico è anche in grado di indurre tale secrezione.
Oltre alla sua normale secrezione a livello di stomaco, una quantità relativamente bassa di pepsinogeno è stata rilevata sia nel sangue che nelle urine, motivo per cui è stato chiamato uropepsinogen.
L'origine dell'uropepsinogen, nonché la funzione che può svolgere in entrambe le posizioni, rimane senza essere determinata. Tuttavia, la loro assenza nei pazienti che hanno totalmente rimosso lo stomaco sembra indicare che la loro origine è ugualmente allo stomaco.
Ragazzi
Finora sono stati descritti due tipi principali di pepsinogen: Pepsinogen I e Pepsinogen II. Entrambi i tipi non presentano differenze nella loro attività catalitica e sono ugualmente attivati dall'idrolisi proteolitica dipendente dall'acido cloridrico.
Può servirti: denaturazione delle proteine: cosa è, fattori, conseguenzeIl pepsinogeno I è sintetizzato e separato da entrambe le cellule principali e dalle cellule fondamentali della mucosa gastrica. Pertanto, la sua secrezione diminuisce nei pazienti con gastrite cronica atrofica, una malattia dello stomaco caratterizzata dalla scomparsa totale delle ghiandole gastriche.
A differenza di quest'ultimo, Pepsinogen II (PGII) è sintetizzato da praticamente tutte le cellule che fanno parte della mucosa gastrica, ma più prominente da quelle della mucosa antrale e da quelle che compongono le ghiandole Brünner presenti nel duodenum.
Nei pazienti con gastrite cronica atrofica, questo tipo di pepsinogeno compensa la riduzione della secrezione di pepsinogeno I.
L'esistenza di questi due tipi di pepsinogen, che differiscono solo per essere secreti da cellule diverse, potrebbe sembrare ridondante. Tuttavia, può essere un adattamento evolutivo per garantire la sintesi di pepsina ogni volta che è necessario.
Attivazione
Pepsinogen acquisisce attività catalitica quando trasformato in pepsina, prodotto dell'eliminazione del peptide di aminoacidi 44 presente nella cavità del sito attivo.
Il suo funzionamento ottimale dipende da bassi valori di pH inclusi nell'intervallo da 1,5 a 2. In condizioni fisiologiche, questi valori sono mantenuti dalla secrezione di acido cloridrico nei canali intracellulari.
La digestione acida a livello di stomaco non ha luogo in tutti gli animali, essendo un esempio di ciò sono gli insetti, che mancano di pepsinogen. Tuttavia, i vertebrati che hanno uno stomaco se hanno attività peptica.
Il pepsinogeno, che viene immagazzinato nelle vescicole secretorie delle cellule principali, viene rilasciato al dotto gastrico quando necessario. Una volta che raggiunge lo stomaco, diventa il prodotto di pepsina dell'ambiente acido e questa attiva molecole pepsinogene.
Per azione delle fibre nervose intrinseche e della stimolazione estrinseca vagale, viene stimolata la produzione di pepsinogen. D'altra parte, l'istamina e la gastrina stimolano le cellule parietali per secernere HCL.
Può servirti: tessuti conduttivi: cosa è, caratteristiche, funzioniLa pepsina, come tutte le endopeptidasi, agisce su collegamenti specifici tra aminoacidi proteici per generare peptidi più piccoli.
In altre parole; Idrolizza i legami peptidici interni di una proteina. La sua azione è più efficace nei collegamenti peptidici vicini agli aminoacidi aromatici (fenilalanina, tirosina). A differenza del suo precursore zimogeno, i cambiamenti adattivi della pepsina nei valori di pH superiori a 6 producono un calo irreversibile di attività catalitica.
Riferimenti
- Bryksa BC, Tanaka T, Yada RY. La modifica N-terminale aumenta la stabilità neutra-ph della pepsina. Biochimica. 2003; 42: 13331-13338.
- Foltmann B, Pedreson VB. Confronto delle strutture primarie di Protessa acida e dei loro zymogeni. Adv Exp Med Biol. 1977; 95: 3-22.
- Guyton A, Hall J. (2006). Libro di testo di Phisiology Medical. (11 ° ed.). USA: Elsevier Saunders.
- Kasper D, Fauci A, Longo D, Braunwald E, Hauser S, Jameson J. (2005). Harrison, Principi di medicina interna. (16 ° ed.). Messico: McGrawhill.
- Kitahara F, Shimazaki R, Sato T, Kojima Y, Morozumi A, Fujino MA. Gastrite atrofica grave con infezione da elicobacter pylori e carcinoma gastrico. Tumore gastrico. 1998; 1: 118-124.
- Lin Y, trovato M, Lin X, Hartsuck JA, Tang J. Dipendenza da pH dei parametri cinetici di pepsina, rizopuspepsina e mutanti di legami idrogeno del sito attivo. J Biol Chem. 1992; 267: 18413-18418.
- MANGEAT p. Secrezione acida e riorganitazione della membrana nella singola cellula parietale gastrica nella coltura primaria. Cellula di biologia. 1990; 69: 223-257.
- Prozialeck J, Wershil BK. (2017). Sviluppo della funzione secretoria gastrica. Fisiologia fetale e neonatale (quinta edizione). Volume 1, pagine 881-888.
- Schubert ML. Segreto gastrico. Opinioni attuali Gastroent 2005; 21: 633-757.
- Sielecki AR, Feorov AA, Boodhoo A, Andreeva NS, James MNG. Le strutture molecolari e cristalline della pepsina suina monoclinica raffinati a 1.8 Å Risoluzione. J Mol Biol. 1990; 214: 143-170.
- Webb PM, Hengels KJ, Moller H, Newell DG, Palli D, Elder JB. L'epidemiologia dei livelli di pepsinogeno A a basso siero e un'associazione internazionale con i tassi di cancro gastrico. Gastroenterologia. 1994; 107: 1335-1344.
- Wolfe MM, Soll Ah. La fisiologia dell'acido gastrico segreto. N English J Med 1998; 319: 1707.
- « Sviluppo di cellule G, gastrina, canali di battitura della torba
- Caratteristiche di Nanche, habitat, proprietà, ricette di cucina »

