Monomeri
- 1452
- 150
- Baldassarre Ross
 Il monomero è una molecola di massa molecolare legata ad altri monomeri da collegamenti chimici
Il monomero è una molecola di massa molecolare legata ad altri monomeri da collegamenti chimici Cosa sono i monomeri?
IL monomeri Sono molecole piccole o semplici che costituiscono l'unità strutturale di base o essenziale di molecole più grandi o complesse chiamate polimeri. Il monomero è una parola di origine greca che significa panino, uno e Semplice, parte.
Mentre un monomero si unisce a un altro, si forma un dimero. Unendosi a questo a sua volta con un altro monomero, forma un trimer, e così via, per formare catene corte chiamate oligomeri o catene più lunghe, che sono i polimeri così chiamati.
I monomeri si legano o polimerizzano formando legami chimici condividendo le coppie di elettroni; Cioè, si uniscono a collegamenti covalenti.
Questa unione di monomeri è nota come polimerizzazione. Possono essere uniti i monomeri dello stesso tipo o diverso e il numero di legami covalenti che possono stabilire con un'altra molecola determinerà la struttura del polimero che si formano (catene lineari, inclinate o strutture tridimensionali).
C'è una vasta gamma di monomeri, tra cui quelli di origine naturale. Questi appartengono e progettano le molecole organiche chiamate biomolecole, presenti nella struttura degli esseri viventi.
Ad esempio, aminoacidi che formano proteine; Le unità monosaccaridi di carboidrati e mononucleotidiche che formano acidi nucleici. Ci sono anche monomeri sintetici, che consentono di elaborare una innumerevole varietà di prodotti polimerici inerti, come dipinti o materie plastiche.
Caratteristiche dei monomeri
I monomeri si legano per legami covalenti
Gli atomi che partecipano alla formazione di un monomero rimangono uniti da legami forti e stabili come il legame covalente. Allo stesso modo, i monomeri polimerizzano o si legano con altre molecole monomeriche attraverso questi collegamenti, dando forza e stabilità ai polimeri.
Questi legami covalenti tra i monomeri possono essere formati da reazioni chimiche che dipenderanno dagli atomi che compongono il monomero, la presenza di doppi legami e altre caratteristiche che presentano la struttura del monomero.
Il processo di polimerizzazione può essere dato da una delle seguenti tre reazioni: per condensa, aggiunta o radicali liberi. Ognuno di essi comporta i propri meccanismi e la modalità di crescita.
Funzionalità monomer e struttura polimerica
Un monomero può essere unito ad almeno altre due molecole monomeriche. Questa proprietà o caratteristica è ciò che è noto come funzionalità dei monomeri, ed è ciò che consente loro di essere le unità strutturali delle macromolecole.
Può servirti: nitrito di potassio (KNO2): struttura, proprietà e usiI monomeri possono essere bifunzionali o polifunzionali, a seconda dei siti attivi o di reagenti del monomero; cioè, degli atomi della molecola che possono partecipare alla formazione di legami covalenti con gli atomi di altre molecole o monomeri.
Questa caratteristica è anche importante, poiché è strettamente legata alla struttura dei polimeri che si conformano, come dettagliato di seguito.
Bifunzionalità: polimero lineare
I monomeri sono bifunzionali quando hanno solo due siti sindacali con altri monomeri; Cioè, il monomero può formare solo due legami covalenti con altri monomeri e formare solo polimeri lineari.
Tra i polimeri lineari, il glicole etilen e gli aminoacidi possono essere menzionati come esempio.
Monomeri polifunzionali - polimeri a tre dimensioni
Ci sono monomeri che possono essere uniti a più di due monomeri e costituiscono le unità strutturali di maggiore funzionalità.
Sono chiamati polifunzionali e sono quelli prodotti da macromolecole polimeriche ramificate, di rete o tridimensionali; Come il polietilene, per esempio.
Scheletro o struttura centrale
Con doppio legame tra carbonio e carbonio
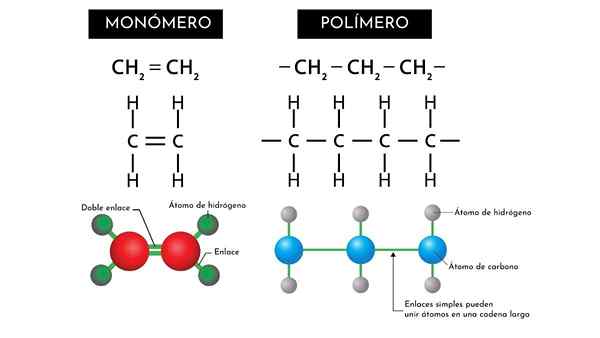
Ci sono monomeri presenti nella loro struttura uno scheletro centrale formato da almeno due atomi di carbonio uniti da un doppio legame (C = C).
A sua volta, questa catena o struttura centrale presenta atomi uniti lateralmente che possono cambiare formando un monomero diverso (R2C = cr2).
Se una delle catene R viene modificata o sostituita, si ottiene un monomero diverso. Inoltre, quando questi nuovi monomeri si uniranno a un polimero diverso.
Può essere menzionato come esempio di questo gruppo di monomeri il propilene (h2C = ch3H), tetrafluoroetilene (f2C = cf2) e cloruro di vinile (H2C = cclh).
Due gruppi funzionali nella struttura
Sebbene ci siano monomeri che hanno un singolo gruppo funzionale, esiste un ampio gruppo di monomeri che hanno due gruppi funzionali nella loro struttura.
Gli aminoacidi ne sono un buon esempio. Hanno un gruppo funzionale amminico (-nh2) e il gruppo funzionale di acido carbossilico (-cooh) unito a un atomo di carbonio centrale.
Questa caratteristica di essere un monomero diffunzionale gli dà anche la capacità di formare lunghe catene polimeri, come la presenza di doppi collegamenti.
Gruppi funzionali
In generale, le proprietà presentate dai polimeri sono fornite dagli atomi che formano le catene laterali dei monomeri. Queste catene costituiscono i gruppi funzionali di composti organici.
Può servirti: legge di più proporzioniCi sono famiglie di composti organici le cui caratteristiche sono fornite da gruppi funzionali o catene laterali. Ad esempio è il gruppo funzionale dell'acido carbossilico R-COOH, il gruppo amino R-NH2, R-OH Alcool, tra molti altri che partecipano alle reazioni di polimerizzazione.
Unione di monomeri uguali o di diversi tipi
Unione di monomeri uguali
I monomeri possono formare diverse classi di polimeri. Possono unirsi a monomeri uguali o dello stesso tipo e generare omopolimeri così chiamati.
Ad esempio, puoi menzionare l'allungamento, un monomero che forma il polistirene. L'amido e la cellulosa sono anche esempi di omopolimeri formati da lunghe catene ramificate del monomero del glucosio.
Unione di diversi monomeri
L'unione di diversi monomeri formano i copolimeri. Le unità vengono ripetute in diversi numeri, ordine o sequenza in tutta la struttura delle catene polimeriche (A-B-B-B-B-A-A-B-A-A-A- ……).
Come esempio di copolimeri, il nylon può essere menzionato, un polimero formato da unità ripetitive di due diversi monomeri. Si tratta di acido dicarbossilico e una molecola di diamicina, che si legano attraverso la condensazione in proporzioni equimolari (uguali).
Diversi monomeri possono anche essere uniti in proporzioni disuguali, come il caso di formazione di un polietilene specializzato che ha come struttura di base il monomero 1-tone più il monomero dell'etilene.
Tipi di monomeri
Ci sono molte caratteristiche che consentono di stabilire diversi tipi di monomeri, tra cui la loro origine, funzionalità, struttura, tipo di polimero che formano, come si distinguono i legami covalenti.
Monomeri naturali
- Esistono monomeri di origine naturale come l'isoprene, che si ottiene dalla linfa o in lattice delle piante e che è anche la struttura monomerica della gomma naturale.
- Alcuni aminoacidi prodotti dagli insetti formano fibroina o proteina di seta. Sono anche aminoacidi che formano il polimero della cheratina, che è la proteina di lana prodotta da animali come le pecore.
- Tra i monomeri naturali ci sono le unità strutturali di base delle biomolecole. Il monosaccaride di glucosio, ad esempio, si unisce ad altre molecole di glucosio per formare diversi tipi di carboidrati come amido, glicogeno, cellulosa, tra gli altri.
- Gli aminoacidi, d'altra parte, possono formare una vasta gamma di polimeri noti come proteine. Questo perché ci sono venti tipi di aminoacidi, che possono essere collegati in qualsiasi ordine arbitrario; E quindi, finiscono per formare una o un'altra proteina con le proprie caratteristiche strutturali.
- I mononucleotidi, che formano le macromolecole chiamate acidi nucleici ADN e RNA rispettivamente, sono anche monomeri molto importanti all'interno di questa categoria.
Monomeri sintetici
- Tra i monomeri artificiali o sintetici (che sono numerosi), alcuni possono essere menzionati con cui vengono elaborate diverse varietà di materie plastiche, come il cloruro di vinile, che forma il cloruro o il polivinil PVC; e gas etilene (H2C = ch2) e il suo polimero in polietilene. È noto che con questi materiali puoi costruire un'ampia varietà di contenitori, bottiglie, oggetti domestici, giocattoli, materiali da costruzione, tra gli altri.
- Il monomero tetrafluoroetilene (f2C = cf2) sta formando il polimero chiamato e commercialmente noto come teflon.
- La molecola Caprolactam derivata da toluene è essenziale per la sintesi di nylon, tra molti altri.
- Esistono diversi gruppi di monomeri acrilici che sono classificati in base alla composizione e alla funzione. Tra questi ci sono acrilamide e metacrilammide, acrilato, acrilici con fluoro, tra gli altri.
Monomeri apolari e polari
Questa classificazione viene eseguita in base alla differenza di elettronegatività degli atomi che formano il monomero. Quando c'è una notevole differenza, si formano monomeri polari; Ad esempio, aminoacidi polari come treonina e asparagina.
Quando la differenza di elettronegatività è zero, i monomeri sono apolari. Ci sono aminoacidi non polari come triptofano, alanina, valina, tra gli altri; e anche monomeri apolari come il vinile acetato.
Monomeri ciclici o lineari
Secondo la forma o l'organizzazione degli atomi all'interno della struttura dei monomeri, questi possono essere classificati come monomeri ciclici, come prolina o ossido di etilene; e lineare o alifatico, come la valina aminoacidica o l'etilen glicole, tra molti altri.
Esempi di monomeri
Oltre a quelli già menzionati, ci sono i seguenti ulteriori esempi di monomeri:
- Formaldeide
- Furfurale
- Cardanolo
- Galattosio
- Stirata
- Alcool polivinilico
- Isoprene
- Acidi grassi
- Epossidi
- E sebbene non siano stati menzionati, ci sono monomeri le cui strutture non sono carbonizzate, ma solforzate, fosforate o hanno atomi di silicio.
Riferimenti
- Carey f. (2006). Chimica organica. (6 °. ed.). Messico: Mc Graw Hill.
- I redattori di Encyclopedia Britannica (2015). Monomero: composto chimico. Preso da: Britannica.com
- Mathews, Holde e Ahern (2002). Biochimica (3 °. ed.). Madrid: Pearson
- Polimeri e monomeri. Recuperato da: materialsworldmodules.org
- Wikipedia (2018). Monomero. Preso da: in.Wikipedia.org

