Caratteristiche della lisina, struttura, funzioni, biosintesi
- 1367
- 130
- Rosolino Santoro
IL Lisina (Lys, K) o il Acido ε-diaminoproico, È uno dei 22 aminoacidi che fanno.
Fu scoperto da Drechsel nel 1889 come prodotto di idrolisi (decomposizione) di caseinogen. Anni dopo, Fischer, Siegfried e Hedin hanno stabilito che faceva anche parte di proteine come gelatina, albumina di uova, conglutina, fibrina e altre proteine.
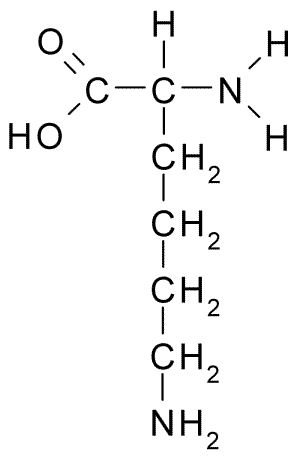
 Struttura chimica della lisina aminoacidica (fonte: Borb, via Wikimedia Commons)
Struttura chimica della lisina aminoacidica (fonte: Borb, via Wikimedia Commons) La sua presenza è stata quindi dimostrata nelle piantine di semi nella germinazione e nella maggior parte delle proteine vegetali esaminate, il che ha determinato la loro abbondanza come elemento costituente generale di tutte le proteine cellulari.
È considerato uno dei principali aminoacidi "limitanti" nelle diete ricche di cereali e per questo motivo si ritiene che la qualità del contenuto proteico consumato dalle diverse popolazioni sottosviluppate del mondo sia colpita.
Alcuni studi hanno determinato che l'assunzione di lisina favorisce la produzione e il rilascio di ormoni insulina e glucagone, che ha effetti importanti sul metabolismo energetico del corpo.
[TOC]
Caratteristiche
La lisina è un α-aminoacido caricato positivamente.53, il che implica che, pH fisiologico, il tuo gruppo amminico sostituente è completamente ionizzato, conferendo un carico netto positivo all'amminoacido.
La sua presenza nelle proteine di diversi tipi di organismi viventi è vicina al 6% e vari autori considerano che la lisina è essenziale per la corretta crescita e la riparazione dei tessuti.
Le cellule hanno molti derivati della lisina, che soddisfano una grande diversità di funzioni fisiologiche. In questi ci sono idrossilisina, metil-lisina e altri.
È un aminoacido chetogenico, il che implica che il suo metabolismo produce scheletri carbonati di substrati intermedi per rotte di formazione di molecole come l'acetil-CoA, con la successiva formazione di corpi chetonici nel fegato.
A differenza di altri aminoacidi essenziali, questo non è un aminoacido glicogeno. In altre parole, il suo degrado non termina con la produzione di intermediari percorsi che producono glucosio.
Struttura
La lisina è classificata all'interno del gruppo di aminoacidi di base, le cui catene laterali hanno gruppi ionizzabili con carichi positivi.
La sua catena laterale o il gruppo R R ha un secondo gruppo amminico primario attaccato all'atomo di carbonio nella posizione ε della sua catena alifatica, da cui il suo nome "ε-aminocaproico".
Ha un atomo di carbonio α, al quale un atomo di idrogeno, un gruppo amminico, un gruppo carbossilico e la catena laterale R, caratterizzati dalla formula molecolare (-Ch2-ch2-ch2-ch2-nh3+) sono uniti.
Poiché la catena laterale ha tre gruppi di metilene e sebbene la molecola di lisina abbia un gruppo aminoa gruppo amino.
Il gruppo amminico della catena laterale della lisina è altamente reattivo e di solito partecipa ai centri attivi di molte proteine con attività enzimatica.
Funzioni
La lisina, essendo un aminoacido essenziale, svolge molteplici funzioni come il micronutriente, specialmente nell'uomo e in altri animali, ma è anche metabolita in diversi organismi come batteri, lieviti, piante e alghe.
Le caratteristiche della sua catena laterale, in particolare quelle del gruppo ε-amino attaccato alla catena di idrocarburi in grado di formare ponti idrogeno, gli danno proprietà speciali che lo fanno partecipare alle reazioni catalitiche in vari tipi di enzimi.
Può servirti: flora e fauna di Zacatecas: specie più rappresentativeÈ molto importante per la crescita normale e il rimodellamento dei muscoli. Inoltre, è una molecola precursore per la carnitina, un composto sintetizzato nel fegato, nel cervello e nei reni che sono responsabili del trasporto di acidi grassi nei mitocondri per la produzione di energia.
Questo aminoacido è anche necessario per la sintesi e la formazione del collagene, un'importante proteina del sistema di tessuto connettivo nel corpo umano, quindi contribuisce al mantenimento della struttura della pelle e delle ossa.
Ha delle funzioni sperimentalmente riconosciute in:
- La protezione dell'intestino contro gli stimoli stressanti, la contaminazione con i patogeni batterici e virali, ecc.
- Diminuire i sintomi dell'ansia cronica
- Favorire la crescita dei neonati che crescono con diete di bassa qualità
Biosintesi
Gli esseri umani e altri mammiferi non possono sintetizzare l'aminoacido lisina In vivo Ed è per questo motivo che devono ottenerlo da proteine animali e vegetali ingerite con cibo.
Nel mondo naturale, due percorsi diversi si sono evoluti per la biosintesi della lisina: uno che usa batteri, piante e funghi "più bassi" e un altro usato da euglénides e funghi "superiori".
Biosintesi della lisina in piante, funghi e batteri inferiori
In questi organismi, la lisina è ottenuta dall'acido diamineo -. Per i batteri, ad esempio, questa via implica la produzione di lisina con scopi di (1) sintesi proteica, (2) sintesi di diaminopimellata e sintesi di (3) lisina che verrà utilizzata nella parete cellulare di Pepidoglin.
L'aspartato, negli organismi che presentano questa rotta non solo dà origine a Lisina, ma deriva anche nella produzione di metionine e treonina.
Il percorso divergente nel semiiado asp.
Biosintesi della lisina in funghi superiori ed euglénidos
Sintesi della lisina di novo In funghi superiori e microrganismi euglénid si verifica attraverso l'intermediario L-α-aminoadipato, che si trasforma numerose volte in diversi modi a quelli che si svolgono in batteri e piante.
Il percorso è composto da 8 passaggi enzimatici, che coinvolgono 7 intermediari liberi. La prima metà del percorso si svolge nei mitocondri e raggiunge la sintesi di α-aminoadipato. La conversione di α-aminoadipato nella l-lisina si verifica più avanti nel citosol.
- Il primo passo della rotta consiste nella condensazione delle molecole α-chetoglutarate e acetil-CoA da parte dell'omochitrata dell'enzima sintasi, che produce acido omocitrico.
- L'acido omocitrico è disidratato in acido Cis-omoaconitico, che viene poi convertito in acido omoisocitrico da un enzima omoaconitatasa.
- L'acido omoisocitrico viene ossidato dall'omoisocitrato deidrogenasi, che raggiunge la formazione di ossiglutarato transitorio, che perde una molecola di anidride carbonica (CO2) e termina come acido α-catoadipico.
- Quest'ultimo composto è transaminato da un processo dipendente dal glutammato grazie all'azione dell'enzima aminoadiparato di aminotransferasi, che produce acido L-α-aminoadipico.
- La catena laterale dell'acido L-α-aminoadipico è ridotta per formare L-α-aminoadipic-Δ-Semi-Assess.
- Sacoopine reduttasi quindi catalyz. Successivamente l'imino viene ridotto e la sacoopina si ottiene.
- Infine, il legame carbonio-nitrogeno nella porzione il glutammato della sacaopina viene "tagliato" dall'enzima sacriopina deidrogenasi, arrendendosi come prodotti finali L-lisina e α-zetoglutarato acido.
Alternative alla lisina
Test sperimentali e analisi condotte con ratti in un periodo di crescita hanno permesso di chiarire che ε-N-L'acetil-lisina può sostituire la lisina per sostenere la crescita dei giovani e questo grazie alla presenza di un enzima: ε-lisina acilasi.
Può servirti: Affotic Zone: Caratteristiche, Flora, FaunaQuesto enzima catalizza l'idrolisi del ε-N-acetil-lisina per produrre lisina e lo fa in modo rapido e abbondante.
Degradazione
In tutte le specie di mammiferi, il primo passo nella degradazione della lisina è catalizzato dall'enzima oxoglutarato lisina-2-ossoglutarato, in grado di convertire la lisina e l'α-ossoglutarato in sacalopina, un derivato aminoacido presente nei fluidi fisiologici animali e la cui esistenza era dimostrata Alla fine degli anni '60.
La sacroopina è tornata a α-aminoadipato Δ-semialdehide e glutammato mediante azione dell'enzima sacaropina deidrogenasi. Un altro enzima è anche in grado di usare sacaropina come substrato per idrolizzato.
La sacaropina, uno dei principali intermediari metabolici nella degradazione della lisina, ha un tasso di sostituzione, in condizioni fisiologiche, estremamente elevata, quindi non si accumula in fluidi o tessuti, che è stato dimostrato dalle alte attività riscontrate dello sviluppatore deidrogenasi.
Tuttavia, la quantità e l'attività degli enzimi coinvolti nel metabolismo della lisina dipende, in larga misura, da vari aspetti genetici di ciascuna specie particolare, poiché vi sono variazioni intrinseche e meccanismi di controllo o regolamentazione specifici.
"Sacaropinuria"
Esiste una condizione patologica legata alla copiosa perdita di aminoacidi come lisina, citrulina e istidina attraverso l'urina e questo è noto come "saropinuria". La sacaropina è un derivato aminoacido del metabolismo della lisina che viene escreto insieme ai tre aminoacidi menzionati nelle urine dei pazienti "saropinurici".
La sacaropina è stata inizialmente scoperta nel lievito di birra ed è un precursore della lisina in questi microrganismi. In altri organismi eucariotici, questo composto viene prodotto durante il degrado della lisina nei mitocondri degli epatociti
Alimenti ricchi di lisina
La lisina è ottenuta dal cibo consumato dalla dieta e un essere umano adulto medio ha bisogno di almeno 0.8 g di questo giorno. Si trova in numerose proteine di origine animale, specialmente in carni rosse come mucca, agnello e pollo.
È in pesci come tonno e salmone e nei frutti del mare come ostriche, gamberi e cozze. È anche presente nelle proteine costituenti dei prodotti lattiero -caseari e dei loro derivati.
Negli alimenti vegetali si trova nelle patate, nei peperoni e nei porri. È anche in avocado, pesche e pere. In legumi come fagioli arriñonados, ceci e soia; Nei semi di zucca, nelle noci della macadamia e negli anacardo (Merey, Marañón, ecc.).
Vantaggi della tua assunzione
Questo aminoacido è incluso in numerosi farmaci di formulazione nutraceutica, ovvero isolato da composti naturali, in particolare le piante.
È usato come anticonvulsivo e la sua efficacia è stata dimostrata anche nell'inibizione della replicazione del Virus dell'herpes simplex Tipo 1 (HSV-1), che di solito si manifesta in momenti di stress, quando il sistema immunitario è depresso o "indebolito" come ampoule o herpes sulle labbra.
L'efficacia degli integratori di L-lisina per il trattamento dell'herpes labiale è dovuta al fatto che questo "compete" o "blocca" l'arginina, un altro aminoacido proteico, che è necessario per la moltiplicazione di HSV-1.
È stato determinato che la lisina ha anche effetti anti-ansolitici, poiché aiuta a bloccare i recettori coinvolti nelle risposte a diversi stimoli stressanti, oltre a partecipare alla diminuzione dei livelli di cortisolo, "ormone dello stress".
Alcuni studi hanno indicato che può essere utile per l'inibizione dei tumori cancerogeni, per la salute degli occhi, per il controllo della pressione sanguigna, tra gli altri.
Può servirti: Media culturale: storia, funzione, tipi, preparazioneNegli animali
Una strategia comune per il trattamento delle infezioni da virus dell'herpes I nei felini è l'integrazione di lisina. Tuttavia, alcune pubblicazioni scientifiche stabiliscono che questo aminoacido non ha, nei felini, nessuna proprietà antivirale, ma agisce piuttosto diminuendo la concentrazione di arginina.
Nella salute dei bambini
L'assunzione sperimentale di L-Lisina, aggiunta nel latte infantile durante il periodo di allattamento al seno, si è rivelata benefica per il guadagno della massa corporea e l'induzione dell'appetito nei bambini durante le prime fasi dello sviluppo postnatale.
Tuttavia, l'eccesso di L-lisina può causare escrezioni urinarie esagerate di aminoacidi, sia caratteristiche neutre che di base, con conseguente squilibrio corpo.
L'eccesso di integrazione della lisina può terminare nella repressione della crescita e di altri effetti istologici ovvi negli organi importanti, probabilmente a causa della perdita di aminoacidi con urina.
Nello stesso studio, è stato anche evidenziato che l'integrazione di lisina migliora le proprietà nutrizionali delle proteine vegetali ingerite.
Altri studi simili condotti su adulti e bambini di entrambi i sessi in Ghana, Siria e Bangladesh, hanno messo in evidenza le proprietà benefiche dell'assunzione di lisina per ridurre la diarrea nei bambini e alcune condizioni respiratorie mortali negli uomini adulti negli uomini.
Disturbi della carenza di lisina
La lisina è, come tutti gli aminoacidi essenziali e non essenziali, necessari per la sintesi corretta delle proteine cellulari che contribuiscono alla formazione di sistemi organici del corpo.
Marcate carenze di lisina nella dieta, poiché è un aminoacido essenziale che non è prodotto dal corpo, può provocare lo sviluppo di dipinti ansiosi mediati dalla serotonina, oltre alla diarrea, anche correlato ai recettori della serotonina.
Riferimenti
- Ciotola, s., & Bunnik, e. M. (2015). La supplica di lisina non è efficace per la prevenzione o il trattamento dell'infezione da herpesvirus 1 felino nei gatti: una revisione sistematica. Ricerca veterinaria BMC, undici(1).
- Carson, n., Scally, b., Neill, d., & Carré, i. (1968). Saccharopinuria: un nuovo errore innato del metabolismo della lisina. Natura, 218, 679.
- Colina R, J., Díaz E, M., Manzanilla M, L., Araque M, H., Martínez G, G., Rossini v, m., & Jerez-Timaure, N. (2015). Valutazione dei livelli di lisina digeribile nelle diete con alta densità di energia per la finitura di suini. Rivista MVZ Córdoba, venti(2), 4522.
- Fellows, b. F. C. Yo., & Lewis, M. H. R. (1973). Metabolismo della lisina nei mammiferi. Diario biochimico, 136, 329-334.
- Fornazier, r. F., Azevedo, r. A., Ferreira, r. R., & Varisi, V. A. (2003). Catabolismo della lisina: flusso, ruolo metabolico e regolazione. Brasiliano Journal of Plant Fisiologia, quindici(1), 9-18.
- Ghosh, s., Smriga, m., Vuvor, f., Suri, d., Mohammed, h., Armah, s. M., & Scrimshaw, N. S. (2010). Effetto della supplica di lisina sulla salute e sulla morbilità in soggetti appartenenti a povere famiglie peri-urbane ad Accra, Ghana. American Journal of Clinical Nutrition, 92(4), 928-939.
- Hutton, c. A., Perugini, m. A., & Gerrard, J. A. (2007). Inibizione della biosintesi della lisina: una strategia antibiotica in evoluzione. Biosistemi molecolari, 3(7), 458-465.
- Kalogeropoul, d., Lafave, l., Schweim, k., Gannon, m. C., & Nuttall, F. Q. (2009). L'ingestione di lisina attenua notevolmente la risposta al glucosio al glucosio ingerito senza un cambiamento nella risposta all'insulina. American Journal of Clinical Nutrition, 90(2), 314-320.
- Nagai, h., & Takeshita, s. (1961). Effetto nutrizionale della supplementazione di l-lisina sulla crescita di neonati e bambini. Paediatria giapponese, 4(8), 40-46.
- O'Brien, s. (2018). Healthline. Estratto il 4 settembre 2019 da WWW.Healthline.com/nutrizione/lisina-benefici
- Zabriskie, t. M., & Jackson, M. D. (2000). Biosintesi della lisina e metabolismo nei funghi. Rapporti sui prodotti naturali, 17(1), 85-97.

