Isomería
- 728
- 101
- Cosetta Messina
Cos'è l'isomeria?
Isomería è un fenomeno chimico che è caratterizzato in cui le molecole con lo stesso numero di atomi hanno proprietà chimiche o fisiche diverse. Pertanto, si verifica negli isomeri, che a loro volta sono molecole le cui formule chimiche sono le stesse, ma le loro strutture o disposizioni spaziali differiscono sostanzialmente l'una dall'altra.
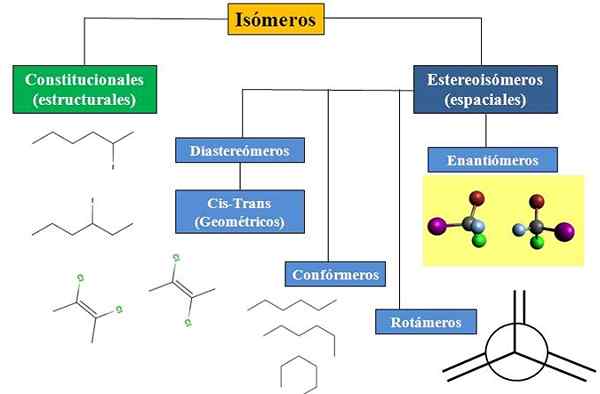
Abbiamo l'isomeria costituzionale o strutturale e lo spazio Isomería, che concentra molta attenzione nella stereochimica. Il diagramma di flusso dell'immagine inferiore mostra che gli isomeri sono principalmente divisi nei due tipi di isomería appena menzionati: costituzionale e stereoisomeri.
 Diagramma di flusso per diversi tipi di isomeri nella chimica organica. Fonte: Gabriel Bolívar.
Diagramma di flusso per diversi tipi di isomeri nella chimica organica. Fonte: Gabriel Bolívar. Tutti gli isomeri, per un determinato composto, hanno la stessa formula chimica. Ma le strutture che possono costruire questi atomi e le loro proporzioni sono uniche per ogni molecola o isomero. Inoltre, anche se la struttura stessa è la stessa, atomi o gruppi possono occupare diverse posizioni spaziali.
Nel diagramma di flusso, sono mostrati alcuni esempi di isomeri che saranno discussi nelle sezioni successive.
Tipi di isomeri
Costituzionale
Gli isomeri costituzionali o strutturali sono quelli che differiscono nell'ordinamento dello scheletro molecolare. Cioè, i loro atomi non sono collegati allo stesso modo, quindi la struttura o i gruppi funzionali in questione possono diventare molto diversi.
Ad esempio, per la stessa formula chimica C7H10Oppure potrebbero esserci più molecole che soddisfano quel numero di atomi; Tutti avranno un singolo atomo di ossigeno, ma la disposizione strutturale degli altri atomi sarà unica per ogni isomero.
E quindi, le proprietà chimiche e fisiche di tutti gli isomeri costituzionali per la formula C7H10O differirà anche molto l'uno dall'altro.
D'altra parte, gli isomeri costituzionali possono essere molto semplici, variando solo nella posizione relativa di un singolo atomo o gruppo. Nella sezione seguente un esempio di questo e quanto sopra verrà visto.
Stereoisomeri
Gli stereoisomeri sono quelli che hanno lo stesso ordine strutturale, ma differiscono nelle posizioni spaziali e negli orientamenti dei loro atomi o gruppi.
Può servirti: ampiezza modulataAffinché la loro esistenza sia possibile, le molecole devono contenere centri stereogenici, essendo i più famosi in chimica organica gli atomi di carbonio asimmetrici o chirali; cioè, con quattro diversi sostituenti.
Oltre ai carboni asimmetrici, la molecola considerata deve non avere elementi di simmetria. Altrimenti, è impossibile per il sistema spaziale maturare nello stereoisoma.
Enantiomeri
Gli enantiomeri sono stereoisomeri costituiti da immagini specchio non superimposti. Ad esempio, le mani a destra e sinistra non si sovrappongono, proprio come le scarpe o i guanti. Nella sezione seguente verrà affrontato il classico esempio di enantiomeía: bromocloreyodomethane: cbrcli.
Diastreomeres
I diastreomeri, d'altra parte, sono anche stereoisomeri ma non sono immagini speculatori. Cioè, che mette l'uno davanti all'altro non sono il riflesso di se stessi. Dei diastomeri più noti che abbiamo l'isomeria cis-trans, chiamata anche isomerie geometriche, specialmente se applicate agli alcheni.
Conforme
I conformatori, anche se rientrano nello spettro dello stereoisoma, in realtà non sono isomeri. Queste sono configurazioni di spazio che una molecola, in un determinato tempo o stato energetico, acquisisce attraverso le rotazioni di molti dei suoi collegamenti. L'esempio dei conformatori del N-esano.
Rotámeros
Finalmente abbiamo i Rotarmers, che assomigliano ai conformatori nel senso che dipendono dalla rotazione dei legami covalenti.
Tuttavia, un singolo legame tra due atomi di carbonio viene preso come riferimento e vengono confrontate le posizioni relative, essere eclissata o alternata, di sostituenti per entrambi i carboni. Successivamente si vedrà l'esempio dei rotami di propilene.
Esempi di isomeri
Iodio esano
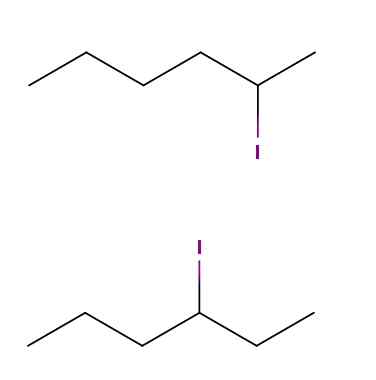 Isomeri costituzionali di iodio esano. Fonte: Gabriel Bolívar via Molview.
Isomeri costituzionali di iodio esano. Fonte: Gabriel Bolívar via Molview. Sopra abbiamo due molecole le cui formule chimiche sono C6H13Yo. Nel primo, abbiamo il 2-inithexan, mentre nel secondo il 3-inithexan. Sono isomeri costituzionali posizionali, poiché lo scheletro è lo stesso, con la differenza che la posizione dell'atomo di iodio varia da un carbonio a un altro.
Può servirti: attrito statico: coefficiente, esempio, esercizio fisicoC3H8O
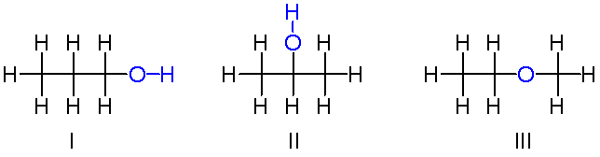 Fonte: V8RIK, CC BY-SA 3.0, via Wikimedia Commons
Fonte: V8RIK, CC BY-SA 3.0, via Wikimedia Commons Up abbiamo un altro esempio di isomeri costituzionali per la formula chimica C3H8O. Le molecole I e II sono rispettivamente 1-propanolo e 2-propanolo. Entrambi sono alcoli. Invece, la molecola III è etil-metil-ote.
Pertanto, parliamo di un altro gruppo funzionale. Si noti che le tre molecole hanno lo stesso numero di atomi, ma le loro strutture sono diverse.
2,3-decloro-2-butene
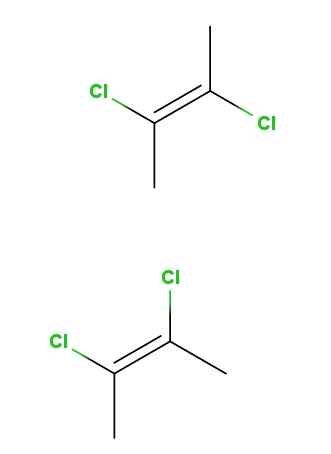 Isomeri geometrici di 2,3-decloro-2-butene. Fonte: Gabriel Bolívar via Molview.
Isomeri geometrici di 2,3-decloro-2-butene. Fonte: Gabriel Bolívar via Molview. Su abbiamo l'isomero trans-22,3-decloro-2-butene e sotto l'isomero CIS-2,3-dicloro-2-butene. Nel primo, gli atomi di cloro si trovano in posizioni opposte per quanto riguarda il doppio legame, mentre nel secondo si trovano sullo stesso lato del doppio legame.
Lo scheletro per entrambe le molecole è lo stesso, ma differisce nelle posizioni spaziali degli atomi di cloro; Pertanto, sono stereoisomeri e non sono immagini speculatori, diventano diamereomeri.
3-flúor-2-metilciclohexan
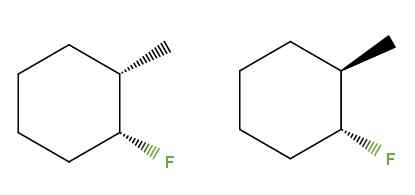 3-flúor-2-metilciclohexano diastereomeri. Fonte: Gabriel Bolívar via Molview.
3-flúor-2-metilciclohexano diastereomeri. Fonte: Gabriel Bolívar via Molview. Questa volta, invece di un doppio legame, abbiamo un anello cicloesano per il composto 3-flúor-2-metilciclohexan. Nell'isomero a sinistra, i gruppi3 e f si trovano sotto il piano dell'anello; Mentre a destra, Cho3 è attivo e f sotto.
Pertanto, quello a sinistra corrisponderebbe all'isomero cis e quello a destra sarebbe il trans isomero. Sono quindi diamereomeri, perché non sono più immagini speculatori.
Conformeros del N-esano
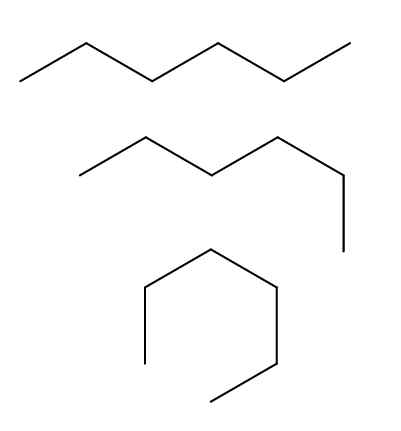 Conformatori del N-esano. Fonte: Gabriel Bolívar via Molview.
Conformatori del N-esano. Fonte: Gabriel Bolívar via Molview. Abbiamo tre conformatori del N-Hexano, che risulta dalle rotazioni e dalle "pieghe" della catena gassata in diversi orientamenti. Tutti corrispondono alla stessa molecola di N-Esano con diversi livelli di piegatura, che dipenderà dall'ambiente e dall'energia interna di ciascuna molecola.
3-Bromo-2-Penol
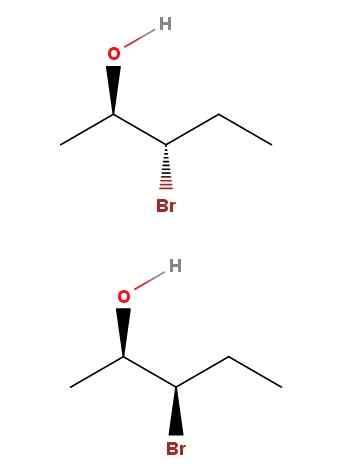 Diastreomeri di 3-Bromo-2-pentanolo. Fonte: Gabriel Bolívar via Molview.
Diastreomeri di 3-Bromo-2-pentanolo. Fonte: Gabriel Bolívar via Molview. In 3-Bromo-2-Pantanolo abbiamo un altro esempio di una coppia di diastereomeri. Si noti che ancora una volta, nell'isomero sopra abbiamo l'OH e il BR che puntano verso direzioni contrarie al piano scheletro; Mentre nell'isomero sottostante, entrambi i gruppi indicano la direzione del lettore.
Può servirti: seconda legge della termodinamica: formule, equazioni, esempi1-bromo-3-cloro-5-etilciclohexan
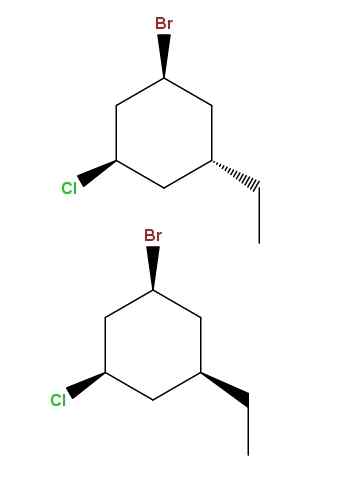 Diastreomeri di 1-Bromo-3-Clor-5-Etilciclohexan. Fonte: Gabriel Bolívar via Molview.
Diastreomeri di 1-Bromo-3-Clor-5-Etilciclohexan. Fonte: Gabriel Bolívar via Molview. E ancora una volta, abbiamo un'altra coppia di diastereomeri, con la differenza che ora la differenza risiede nella posizione spaziale di un singolo gruppo: Ethyl, -Ch2Cap3.
Questo tipo di isomeri ha un nome molto specifico: gli epigmers, che sono diastheomer la cui variazione è osservata solo nella configurazione spaziale di un singolo carbonio asimmetrico; In questo caso, quello che è collegato a -CH2Cap3.
Bromocloreyodometano
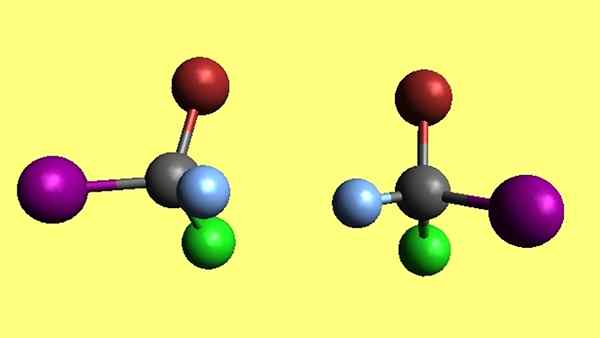 La coppia di bromocloreyodometano enantimers. Fonte: Gabriel Bolívar.
La coppia di bromocloreyodometano enantimers. Fonte: Gabriel Bolívar. Si noti che le due molecole di bromocloroyodometano, cbrcli, sono enantiomeri perché uno è il riflesso non superimposibile dell'altro. Per quanto ci provi, i tuoi quattro atomi non coincideranno mai. Si dice che abbiano configurazioni di spazio opposte.
2-Bromo-4-Etilciclohexan
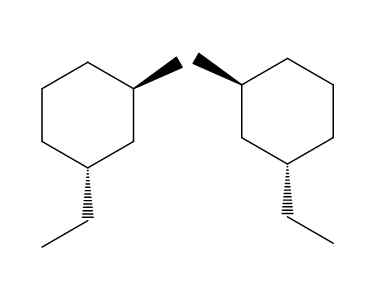 Inantimers di 2-Bromo-4-Etilciclohexan. Fonte: Gabriel Bolívar via Molview.
Inantimers di 2-Bromo-4-Etilciclohexan. Fonte: Gabriel Bolívar via Molview. Nell'esempio della coppia di molecole 2-bromo-4-etilciclohexan. Se proviamo a capovolgere la molecola di destra, vedremo che il gruppo -CH2Cap3 Non si troverà sotto l'anello ma sopra.
Allo stesso modo, Cho3 Non punterà l'anello ma sotto. Le impostazioni dello spazio sono investite, sono opposte. Questa è un'altra delle caratteristiche più importanti di Enatiomeía.
Rotámeros del Propileno
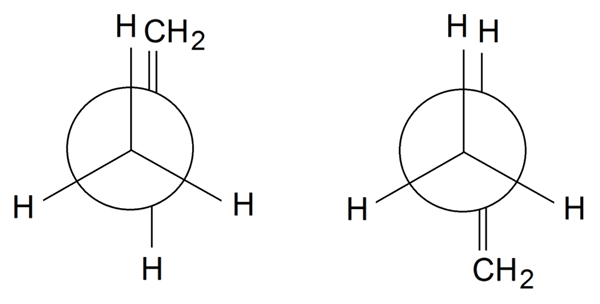 Rotámeros del Propileno. Fonte: Samuele Madini, CC BY-SA 4.0, via Wikimedia Commons
Rotámeros del Propileno. Fonte: Samuele Madini, CC BY-SA 4.0, via Wikimedia Commons Nel Rotámeros del Propileno, per finire, ruotiamo il semplice legame tra la C1 e C2: H3C-CH = CH2. Il gruppo = CH2 È in una posizione eclissata con una delle H H3 Anteriore nel rotamer a sinistra. Nel frattempo, il = Cho2 E H si trovano in posizioni alternate nella maniera giusta.
A seconda dell'eclissaggio o meno dei gruppi, avremo un impedimento sterico, che destabilizzerà il Rotamero. Pertanto, la rota di destra è più stabile di quella a sinistra.
Riferimenti
- Graham Solomons t.W., Craig b. Frigorifero. (2011). Chimica organica. (10th Edizione.). Wiley Plus.
- Carey f. (2008). Chimica organica. (Sesta edizione). Mc Graw Hill.
- Morrison e Boyd. (1987). Chimica organica. (Quinta edizione). Addison-Wesley Iberoamericana.
- Dottore. S. Gevorg. (2020). Enantiomeri, diastreomeri, isomeri identici o costituzionali. Passaggi di chimica. Recuperato da: Chemistroysteps.com
- Wikipedia. (2020). ISOMERO. Recuperato da: in.Wikipedia.org
- Allison Soult. (13 agosto 2020). Isomeri. Chimica librettexts. Recuperato da: Chem.Librettexts.org
- James Ashenhurst. (2020). Stereochimica e chiralità. Recuperato da: MasterOrganicChemistry.com

