Struttura dell'ormone della crescita (somatotropina), funzioni
- 2844
- 21
- Lidia Valentini
IL Somatotropina (STH) U Ormone della crescita (GH) è una proteina relativamente piccola prodotta a livello di adenoipofisi e coinvolta nei processi di sviluppo, crescita longitudinale dell'organismo e nel controllo di diversi processi metabolici.
È un ormone non glaro. Gli ormoni della ghiandotropas dell'ipofisi si radunano.
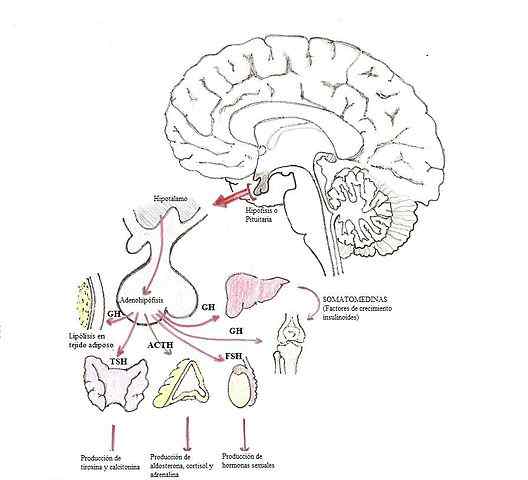
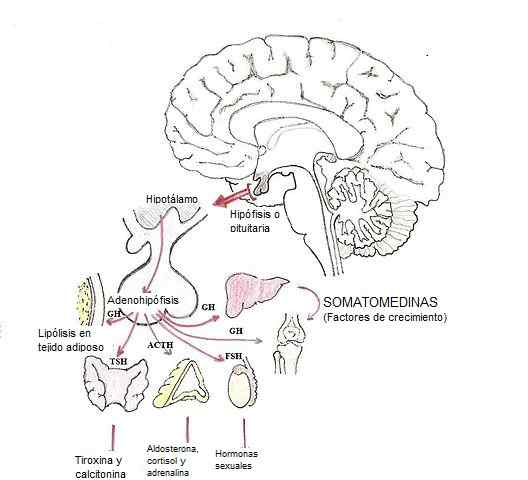 Modifica degli ormoni nell'ipofisi (Fonte: Dubaele / Public Domain, tramite Wikimedia Commons)
Modifica degli ormoni nell'ipofisi (Fonte: Dubaele / Public Domain, tramite Wikimedia Commons) Gli ormoni delle ghiandotropas sono, ad esempio, adrenocortopina (ACTH), gonadotropine (FSH e LH) e ormone stimolante la tiroide (TSH).
Gli ormoni non glandropas, d'altra parte, e tra i quali sono inclusi la prolattina e l'ormone della crescita, agiscono senza il contesto di qualsiasi altra ghiandola endocrina, poiché esercitano le loro azioni direttamente sui globuli bianchi le cui attività regolano.
[TOC]
Struttura
L'ormone della crescita è una proteina relativamente piccola che si verifica in diverse isoforme. L'isoforma principale è composta da circa 191 aminoacidi, ha un peso molecolare di 22 kDa e proviene da un peptide precursore più lungo (pre-GH) di 28 kDa, che è anche secreto ma che manca di funzioni fisiologiche.
Nella sua struttura, la somatotropina sembra essere omologata per la prolattina e la somatomamamamototropina corionica (CS), ha prodotto quest'ultimo nella placenta. Tale è la somiglianza, che si ritiene che i tre formino una famiglia ormonale.
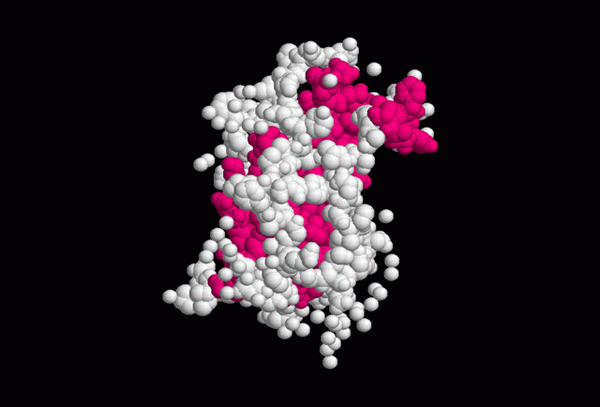 Struttura approssimativa dell'ormone della crescita (fonte: роман бекер, tramite Wikimedia Commons)
Struttura approssimativa dell'ormone della crescita (fonte: роман бекер, tramite Wikimedia Commons) La struttura secondaria della somatotropina mostra 4 eliche alfa stabilizzate con due ponti disolfuro, la cui configurazione è necessaria per l'interazione dell'ormone con il suo ricevitore.
Un fatto in relazione alla struttura, e degno di essere evidenziato, rappresenta il fatto che nonostante il fatto che gli ormoni della crescita di diverse specie abbiano notevoli somiglianze con l'uomo, solo quest'ultimo e quello dei primati, esercitano effetti significativi negli esseri umani.
Funzioni
Le funzioni di somatotropina sono generalmente descritte come quelle associate allo sviluppo e alla crescita dell'organismo. Anche quelli associati al metabolismo, che includono modifiche nel metabolismo lipidico e nel glucosio promosso dall'ormone.
Le funzioni di crescita, tuttavia, possono anche essere considerate metaboliche, poiché implicano funzioni anaboliche associate alla sintesi proteica, che non esclude alcune altre funzioni senza associazione diretta con il metabolismo come la proliferazione cellulare.
Alcune delle funzioni o delle azioni distribuite dalla somatotropina sono esercitate da questo ormone direttamente sui suoi tessuti bianchi, ma molte di esse sono eseguite da alcune altre sostanze la cui sintesi e rilascio sono stimolati dall'ormone della crescita.
Sintesi IGF
La prima linea di azione di somatotropina è precisamente la sintesi di queste sostanze che sono note come fattori di crescita simili all'insulina (IGF), di cui i tipi 1 e 2 sono stati identificati. Sono designati come IGF1 (i più importanti) e IGF2, secondo il suo acronimo in inglese.
Questi fattori erano inizialmente noti e sono ancora designati, come mediatori della somatotropina o delle somatomedine C (IGF1) e A (IGF2) o anche come attività simile all'insulina non sospepibile (NSILA). Sono sintetizzati da molti tipi di cellule, ma si verificano principalmente nel fegato.
Le azioni di SHH e IGF1 sono molto diverse. Alcuni esercitano ciascuna di queste sostanze in modo indipendente, a volte in combinazione e sinergicamente e altre volte agiscono antagonicamente.
Può servirti: elettroforesi: fondazione, tecnica, a cosa serve, esempiInduzione della crescita
Questa è una delle azioni più importanti promosse dalla somatotropina, ma eseguita in combinazione con l'IGF1. Sebbene entrambi inducano la crescita di numerosi tessuti corporei, il loro effetto più importante viene esercitato sulla crescita dello scheletro.
Questo risultato finale è prodotto da diversi effetti indotti dall'ormone e dall'IGF1. Includono l'aumento del deposito proteico da parte delle cellule condrocitiche e osteogeniche, il più alto tasso di riproduzione di queste cellule e la conversione dei condrociti in cellule osteogeniche; Tutto ciò porta al nuovo deposito osseo.
Durante la crescita e lo sviluppo dell'organismo e prima della chiusura delle epifisi ossee, la nuova cartilagine viene depositata in epifisi seguita dalla sua conversione in un nuovo osso, che allunga la diafisi e le epifisi sono separate.
Il consumo progressivo di cartilagine epifisaria lo esaurisce e l'osso non può continuare a crescere. Alla fine dell'adolescenza la diafisi e l'epifisi e la crescita della lunga lunghezza ossea vengono rallentate su ciascuna estremità e infine si ferma.
Un secondo meccanismo può spiegare l'aumento dello spessore osseo. Gli osteoblasti del periosteium stanno depositando un nuovo osso sul vecchio e gli osteoclasti stanno eliminando il vecchio osso. Se il tasso di deposizione supera l'eliminazione, lo spessore aumenta.
Poiché l'ormone della crescita esercita una intensa stimolazione sugli osteoblasti, sotto il suo effetto, lo spessore delle ossa può continuare ad aumentare, sebbene la sua lunghezza non sia più modificata a causa della chiusura dell'epifisi.
Promozione del deposito proteico nei tessuti
Questo effetto può essere ottenuto attraverso diversi meccanismi: l'aumento del trasporto di aminoacidi attraverso le membrane cellulari, l'aumento della traduzione dell'RNA a livello di ribosomi, l'aumento della trascrizione del DNA all'RNA nel nucleo e una riduzione della proteina e dell'aminoacido catabolismo.
Altre azioni metaboliche
Nel tessuto grasso, l'ormone della crescita promuove la lipolisi e il rilascio di acidi grassi nel torrente circolatorio, il che aumenta la sua concentrazione nei fluidi corporei. Allo stesso tempo, favorisce in tutti i tessuti la conversione degli acidi grassi in acetil coenzima A e il suo uso come fonte di energia.
La stimolazione dell'uso di grassi, insieme all'accumulo di proteine a causa del loro effetto anabolico, porta ad un aumento del tessuto magro.
L'aumento della mobilizzazione dei grassi può essere così elevato che il fegato produce grandi quantità di acido acetoacetico che portano alla chetosi e un fegato grasso può essere generato.
In relazione al metabolismo dei carboidrati, gli effetti della somatotropina includono la diminuzione della raccolta del glucosio nel tessuto adiposo e muscolare muscolare, aumento della produzione di fegato di glucosio e aumento della secrezione di insulina.
Tutti questi effetti sono chiamati diabetogeni e la secrezione di ormoni ad alta crescita può riprodurre alterazioni metaboliche che accompagnano il diabete di tipo II non -insulina dipendente.
Altre funzioni
Le azioni anaboliche e mitogeniche del GH e dell'IGF1 si manifestano anche nella crescita e nella funzione del cuore, del fegato, della milza, della tiroide, del timo e della lingua. L'ormone può contribuire all'ispessimento della pelle, alla stimolazione delle ghiandole sudore e alla crescita dei capelli.
Nei reni il tasso di filtrazione glomerulare e la sintesi del calcitriolo aumentano, che favorisce non solo la crescita, ma anche la mineralizzazione ossea. Promuove anche l'eritropoiesi e la sintesi del fibrinogeno e la risposta immunitaria mediante la stimolazione dei linfociti T e dei macrofagi.
Può servirti: tessuto epiteliale: caratteristiche, descrizione, funzioni, tipiRecettori per la somatotropina
Le azioni di somatotropina, inclusa la promozione della sintesi di fattori di crescita simili all'insulina, sono mediate attraverso la loro unione con recettori specifici espressi nelle membrane a cellule bianche.
Esistono due forme di questi recettori, la seconda delle quali è una breve variante (troncata) della prima; Forma troncata che inibisce la funzione del lungo ricevitore e che se sovraespresso produrrebbe insensibilità tissutale all'ormone.
Il ricevitore lungo è composto da 638 aminoacidi e ha un dominio extracellulare di 250, un dominio transmembrale alfa di circa 38 e un dominio intracellulare di 350 aminoacidi. Ogni molecola di somatotropina finisce per unire due molecole di ricevitore e produrre quella che viene chiamata dimerizzazione del recettore.
Questa dimerizzazione attiva una proteina JAK2 chinasi situata sulle estremità intracellulari di ciascun monomero del ricevitore e questi fosforilati della chinasi attiva altri substrati come STAT5 e il recettore della somatotropina stesso.
Le molecole stat5 fosforilate soffrono anche di una dimerizzazione che le rende regolatori molto precisi dell'espressione genica e della sintesi proteica.
Produzione
La somatotropina è sintetizzata a livello delle cellule di adenoipofisi somatotropas. Queste cellule sono tinte intensamente con sostanze acide, quindi sono anche chiamate acidofili. Sono insieme il gruppo cellulare più abbondante della ghiandola poiché rappresentano il 50% del totale di 5 tipi diversi.
Esiste un complesso genetico di 5 geni nel lungo braccio del cromosoma umano 17 che codifica per le diverse isoforme dell'ormone della crescita e il somatomamototropina corionica umana (HCS).
Uno di questi è il normale HGH-N, che codifica la forma più abbondante di ormone della crescita umana che è la suddetta di 22 kDa e rappresenta il 75% dell'ormone della crescita circolante totale.
Il suo RNA messaggero è soggetto a "Taglia e giunzione" per produrre una forma più piccola di ormone, di 20 kDa, privo di rifiuti di aminoacidi da 32 a 46 e rappresenta il 10%.
Un secondo gene (HGH-V) è espresso principalmente nella placenta e codifica una forma variante di HGH di cui solo quantità significative compaiono nella circolazione durante la gravidanza. Gli altri 3 geni codificano le isoforme dell'umano di somatomamototropina.
Pubblicazione
Sia la sintesi che la secrezione o il rilascio dell'ormone della crescita sono regolati da fattori stimolanti e inibitori di tali funzioni.
Influenze stimolanti
Tra le principali influenze umoristiche stimolanti la sintesi e la secrezione di somatotropina vi sono i peptidi GHRH (ormone della crescita che rilascia l'ormone) e la grelina).
L'ormone della crescita che libera l'ormone (GHRH) è un peptide ipotalamico che esiste in due varianti rispettivamente di 40 e 44 aminoacidi. Si comporta nelle cellule Somatotropas alla sintesi di AMPC e all'attivazione del fattore di trascrizione PIT1 specifico per l'ormone della crescita.
La grelina è un'endogena dell'ormone della crescita dell'ormone della crescita. È un peptide di circa 28 aminoacidi sintetizzati a livello di ipotalamo e stomaco. Agisce in modo sinergico con GHRH la cui versione promuove, inibendo la somatostatina. Agisce attraverso recettori che attivano la fosfolipasi C.
Alcuni parametri metabolici come l'ipoglicemia, bassi livelli di acidi grassi liberi nel sangue e alte concentrazioni di aminoacidi sono importanti stimoli per la secrezione dell'ormone della crescita.
Può servirti: le 12 fasi dello sviluppo umano e le sue caratteristicheAltri fattori stimolanti che contano sono stress acuto, sovraccarico del corpo, dolore, steroidi sessuali (pubertà), dopamina, stimolazione dei recettori α2, acetilcolina, galanina, serotonina e β-endorfina.
Influenze inibitorie
Tra questi ci sono la somatostatina o l'inibitore ormonale del rilascio di ormoni della crescita (GHRIH) e il feedback negativo.
La somatostatina è un peptide ipotalamico di 14 aminoacidi che inibisce la secrezione, ma non la sintesi, dell'ormone della crescita. Una variante lunga, 28 aminoacidi, è sintetizzata nel tratto gastrointestinale. Entrambe le varianti si legano allo stesso ricevitore e inibiscono la sintesi ciclica dell'AMP.
Per quanto riguarda il feedback negativo, il GH ha rilasciato, attraverso un'azione auto -sociale, inibisce la propria ulteriore rilascio. L'IGF1 inibisce l'ipotalamo all'ormone della crescita dell'ormone della crescita e stimola la somatostatina, mentre inibisce la sintesi di GH nell'ipofisi.
Alcuni parametri metabolici come iperglicemia, alti livelli plasmatici di acidi grassi liberi e bassi livelli di aminoacidi sono inibitori della secrezione di somatotropina.
Gli inibitori sono anche freddi, stress cronico, adiposità, progesterone, ormoni tiroidei, deficit o eccessi di cortisolo e stimolazione dei recettori adrenergici β2 β2.
Dose
L'uso terapeutico dell'ormone della crescita biosintetizzato è indicato per il trattamento di quelle sofferenze in cui è stata rivelata una carenza nella sua secrezione, nel nanismo ipofisario e nei bambini a bassa dimensione dalla sindrome di Turner.
L'amministrazione è effettuata sotto forma di una soluzione iniettabile ricostruita da una strada che contiene un liofilizzato con 40 u.Yo. dell'ormone biosintetico e a cui vengono aggiunti i compagni da 2 ml di soluzione di cloruro di sodio allo 0,9 %.
Nella deficit dell'ormone della crescita nei bambini è raccomandato tra 0,07 e 0,1 U.Yo./kg di peso corporeo al giorno. Nella sindrome di Turner 0.14 U.Yo./kg di peso corporeo al giorno. Per la carenza di ormoni della crescita negli adulti: da 0,018 a 0,036 U.Yo./kg di peso corporeo al giorno.
Effetti
La somministrazione terapeutica dell'ormone della crescita può essere accompagnata da alcuni effetti collaterali avversi come l'ipersensibilità manifest attraverso orticaria generalizzata, ipoglicemia a digiuno, infiammazione nel sito di iniezione e mal di testa passeggeri.
È stato descritto lo sviluppo di una certa ipertensione intracranica benigna, più frequente nei bambini e meno negli adulti.
Per quanto riguarda il metabolismo dei carboidrati, lo sviluppo del diabete mellito è stato riportato in pazienti che hanno ricevuto un trattamento con ormone della crescita.
In relazione al sistema muscolare scheletrico ci sono prove di miosite infiammatoria con mialgia e debolezza muscolare, prodotta non dall'ormone, ma forse dal metacresolo usato come conservatore nella formula.
Sono stati riportati casi di ginecomastia, anemia e pancreatite acuta.
Riferimenti
- Ganong WF: The Pituitary Gland, 25a ed. New York, McGraw-Hill Education, 2016.
- Guyton AC, Hall JE: ormoni pituitari e il loro controllo da parte dell'ipotalamo, in Libro di testo di fisiologia medica, 13 ° ED, AC Guyton, JE Hall (a cura di). Filadelfia, Elsevier Inc., 2016.
- Lang F, Verrey F: Ormone, in Physiologie des Menschen AcHyophysiologie, 31 ° ED, RF Schmidt et al (eds). Heidelberg, Springer Medizin Verlag, 2010
- Voigt K: System Endokrinines, in Physiologie, 6 ° ed; R Klinke et al (Eds). Stuttgart, Georg Thieme Verlag, 2010.
- Widmaier EP, Raph H e Strang KT: The Endocrine System. L'ipotalamo e la ghiandola pituitaria, nella fisiologia umana di Vander: i meccanismi della funzione corporea, 13 ° ed; EP Windmaier et al (Eds). New York, McGraw-Hill, 2014.
- « Concetto di allitterazione, caratteristiche ed esempi
- Caratteristiche di comunicazione di gruppo, elementi, esempi »

