Idrossidi
- 2460
- 779
- Kayla Serr
Cosa sono gli idrossidi?
IL Idrossidi Sono composti inorganici e ternari che consistono nell'interazione tra un catione metallico e il gruppo funzionale OH (idrossido anione, OH-). La maggior parte di loro è di natura ionica, sebbene possano anche avere legami covalenti.
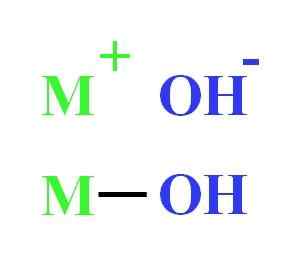
Ad esempio, un idrossido può essere rappresentato come interazione elettrostatica tra cation M+ e anione oh-, o come l'unione covalente attraverso il collegamento M-OH (IMMICA inferiore). Nel primo viene dato il legame ionico, mentre nel secondo il covalente. Questo fatto dipende essenzialmente dal metallo o dal cazionale+, così come la sua radio di carico e ioni.
 Rappresentazione idrossido. Fonte: Gabriel Bolívar
Rappresentazione idrossido. Fonte: Gabriel Bolívar Perché molti di loro provengono dai metalli, è equivalente a menzionarli come idrossidi metallici.
Come si formano gli idrossidi?
Esistono due principali percorsi sintetici: per reazione dell'ossido corrispondente con l'acqua o con una base forte in un mezzo acido:
Mo + h2O => m (oh)2
Mo + h+ + OH- => M (OH)2
Solo quegli ossidi metallici solubili in acqua reagiscono direttamente per formare idrossido (prima equazione chimica). Altri sono insolubili e richiedono specie acide che rilasciano m+, che quindi interagisce con l'OH- da basi forti (seconda equazione chimica).
Tuttavia, queste basi forti sono NaOH, KOH e altri dei metalli alcalini (Lioh, RBOH, CSOH) idrossidi metallici (CSOH). Questi sono composti ionici altamente solubili in acqua, quindi il loro oh- Sono liberi di partecipare alle reazioni chimiche.
D'altra parte, ci sono idrossidi metallici insolubili e di conseguenza sono basi molto deboli. Anche alcuni di loro sono acidi, come nel caso di acido telluico, TE (OH)6.
L'idrossido stabilisce un equilibrio di solubilità con il solvente che lo circonda. Se è acqua, ad esempio, l'equilibrio viene quindi espresso come segue:
M (OH)2 M2+(AC) + OH-(AC)
Dove (AC) indica che il mezzo è acquoso. Quando il solido è insolubile, la concentrazione disciolta è piccola o spregevole. Per questo motivo, gli idrossidi metallici insolubili non possono generare soluzioni basiche come NaOH.
Da quanto sopra si può dedurre che gli idrossidi presentano proprietà molto diverse, legate alla struttura chimica e alle interazioni tra metallo e OH. Pertanto, sebbene molti siano ionici, con varie strutture cristalline, altri hanno invece strutture polimeriche complesse e disordinate.
Proprietà idrossido
Oh anione-
Lo ione idrossilico è un atomo di ossigeno collegato a un idrogeno. Quindi, questo può essere facilmente rappresentato come oh-. Il carico negativo si trova sull'ossigeno, rendendo questo anione un donatore di specie di elettroni: una base.
Se oh- Fatto i suoi elettroni su un idrogeno, si forma una molecola H2O. Puoi anche donare i tuoi elettroni a specie di carico positivo: come centri metallici M+. Pertanto, si forma un complesso di coordinamento attraverso il collegamento Dativo M-OH (l'ossigeno fornisce la coppia di elettroni).
Tuttavia, affinché ciò accada, l'ossigeno deve essere in grado di coordinarsi in modo efficiente con il metallo, altrimenti, le interazioni tra M e OH avranno un marcato carattere ionico (M+ OH-).
Può servirti: pipetta volumetrica: caratteristiche, usi, calibrazione ed erroriPoiché lo ione idrossilico è lo stesso in tutti gli idrossidi, la differenza tra tutti si trova nel catione che lo accompagna.
Allo stesso modo, poiché questo catione può provenire da qualsiasi metallo dalla tavola periodica (gruppi 1, 2, 14, 15, 16 o dai metalli di transizione), le proprietà di tali idrossidi variano notevolmente, sebbene tutti contempino in comune alcuni aspetti.
Carattere ionico e di base
Gli idrossidi, sebbene abbiano collegamenti di coordinamento, hanno un carattere ionico latente. In alcuni, come NaOH, i suoi ioni fanno parte di una rete cristallina costituita da na cationi+ e oh anioni- in proporzioni 1: 1; cioè, per ogni na ione+ C'è uno ione oh- di controparte.
A seconda del carico in metallo, ci saranno più o meno anioni- intorno ad esso. Ad esempio, per un catione metallico m2+ Ci saranno due ioni oh- interagire con lui: m (oh)2, Cosa sono gli schizzi come Ho- M2+ OH-.
Allo stesso modo si verifica con i metalli m3+ e con altre cariche più positive (sebbene raramente superano 3+).
Questo carattere ionico è responsabile di molte proprietà fisiche, come la fusione e i punti di ebollizione. Questi sono alti, il che riflette le forze elettrostatiche che funzionano all'interno della rete cristallina. Inoltre, quando gli idrossidi vengono sciolti o fusi, possono condurre corrente elettrica a causa della mobilità dei loro ioni.
Tuttavia, non tutti gli idrossidi hanno le stesse reti cristalline. Quelli con il più stabile, saranno meno inclini a dissolversi in solventi polari come l'acqua. Come regola generale, più disparate sono le radio ioniche di M+ e oh-, Più solubile sarà lo stesso.
Tendenza periodica
Quanto sopra spiega perché la solubilità degli idrossidi metallici alcalini aumenta quando il gruppo scende. Pertanto, il crescente ordine di solubilità in acqua per questi è il seguente: lioh OH- È un anione piccolo e man mano che il catione diventa più ingombrante, la rete cristallina indebolisce l'energia. D'altra parte, i metalli alcalinotherro formano meno idrossidi solubili a causa dei loro più grandi carichi positivi. Questo perché m2+ Attira più forza nell'OH- rispetto a m+. Allo stesso modo, i suoi cationi sono più piccoli, e quindi meno ineguale rispetto a OH-. Il risultato di ciò è l'evidenza sperimentale che NaOH è molto più semplice di Ca (OH)2. Lo stesso ragionamento può essere applicato ad altri idrossidi, sia per quelli dei metalli di transizione, sia per quelli del blocco P (AL, PB, TE, ecc.). Inoltre, il raggio ionico più piccolo e grande e il carico positivo di m+, Minore sarà il carattere ionico dell'idrossido, in altre parole, quelli con densità di carico molto elevate. Un esempio di ciò si verifica con idrossido di beryl, essere (OH)2. Lui è2+ È un catione molto piccolo e il suo carico divalente lo rende elettricamente molto denso. M idrossidi (OH)2 reagire con gli acidi per formare un acquacomplex, cioè m+ Fine circondate da molecole d'acqua. Tuttavia, esiste un numero limitato di idrossidi che possono anche reagire con le basi. Questi sono quelli che sono noti come anfoteros idrossidi. Gli idrossidi di anfoter reagiscono sia con acidi che basi. La seconda situazione può essere rappresentata con la seguente equazione chimica: M (OH)2 + OH- => M (OH)3- Ma come determinare se un idrossido è anfoter? Attraverso un semplice esperimento di laboratorio. Perché molti idrossidi metallici sono insolubili in acqua, aggiungendo una base forte a una soluzione con ioni m+ sciolto, ad esempio, a3+, Precipiterà l'idrossido corrispondente: Al3+(AC) + 3OH-(AC) => AH (OH)3(S) Ma avendo un eccesso di oh- L'idrossido continua a reagire: Al (Oh)3(s) + oh- => Al (OH)4-(AC) Di conseguenza, il nuovo complesso di carico negativo è solvetato dalle molecole d'acqua circostanti, dissolvendo il solido idrossido di alluminio bianco. Quegli idrossidi che rimangono invariati con l'aggiunta di base extra non si comportano come acidi e, quindi, non sono anfotici. Gli idrossidi possono avere strutture cristalline simili a quelle di molti sali o ossidi; alcuni semplici e altri molto complessi. Inoltre, quelli in cui vi è una diminuzione del carattere ionico può presentare centri metallici uniti dai ponti di ossigeno (hom-o-moh). In soluzione le strutture sono diverse. Sebbene per idrossidi molto solubili sia sufficiente considerarli come ioni sciolti in acqua, per altri è necessario tenere conto della chimica del coordinamento. Pertanto, ogni catione m+ Può essere coordinato a un numero limitato di specie. Più ingombrante, maggiore è il numero di acqua o molecole OH- collegato a lui. Da qui sorge il famoso ottaedro di coordinamento di molti metalli disciolti in acqua (o in qualsiasi altro solvente): M (OH2)6+N, Essere uguali al carico di metallo positivo. CR (OH)3, Ad esempio, davvero un ottaedro. COME? Considerando il composto come [Cr (oh2)3(OH)3], di cui tre delle molecole d'acqua sono sostituite da OH Anions-. Se tutte le molecole sono state sostituite da OH-, Quindi il carico negativo e il complesso della struttura ottaedrica [Cr (OH) sarebbero ottenuti6"3-. Il carico -3 è il risultato delle sei cariche negative dell'OH-. Gli idrossidi possono essere considerati "ossidi idratati". Tuttavia, in essi "l'acqua" è in contatto diretto con M+; mentre negli ossidi idratati mo · nh2Oppure, le molecole d'acqua fanno parte di una sfera di coordinazione esterna (non sono vicine al metallo). Queste molecole d'acqua possono essere estratte attraverso il riscaldamento di un campione di idrossido: M (OH)2 + Q (calore) => mo + h2O Mo è l'ossido metallico formato a causa della disidratazione dell'idrossido. Un esempio di questa reazione è ciò che si osserva quando l'idrossido cuprico, Cu (OH) è disidratato2: Cu (oh)2 (blu) + Q => CUO (nero) + H2O Qual è il modo corretto per menzionare gli idrossidi? L'IUPAC ha sollevato tre nomenclature per questo scopo: il tradizionale, lo stock e il sistematico. È corretto usare uno dei tre, tuttavia, per alcuni idrossidi può essere più comodo o pratico menzionarlo in un modo o nell'altro. La nomenclatura tradizionale consiste semplicemente nell'aggiungere la più alta valenza che il metallo presenta; e il suffisso -solo il più basso. Pertanto, ad esempio, se il metallo M ha valenze +3 e +1, idrossido M (OH)3 Si chiama idrossido (nome metallico)ICO, mentre l'idrossido di moh (nome metallico)orso. Per determinare cosa è sufficiente la valencia metallica in idrossido per osservare il numero dopo OH chiuso tra parentesi. Quindi, m (oh)5 Significa che il metallo ha un carico o una valenza di +5. Il principale inconveniente di questa nomenclatura, tuttavia, è che può essere complicato per i metalli con più di due stati di ossidazione (come con Chrome e Manganese). Per tali casi, i prefissi iper-e iper vengono utilizzati per indicare le valenze più alte e più basse. Pertanto, se m invece di avere solo valenze +3 e +1, ha anche +4 e +2, allora i nomi dei suoi più grandi idrossidi e valenze minori sono: idrossido iper(Nome metallico)ICO, e idrossido singhiozzo(Nome metallico)orso. Di tutte le nomenclature, questo è il più semplice. Qui il nome di idrossido è semplicemente seguito dal Valencia del metallo bloccato tra parentesi e scritto in numero romano. Ancora una volta per m (oh)5, Ad esempio, la sua nomenclatura di serie sarebbe: idrossido (nome metallico) (V). (V) denota quindi (+5). Infine, la nomenclatura sistematica è caratterizzata dal ricorrere ai prefissi moltiplicanti (di, tri-, tetra-, penta-, hexa-, ecc.). Questi prefissi vengono utilizzati per specificare sia il numero di atomi di metallo che ioni OH-. In questo modo, il M (OH)5 È chiamato: pentahidroxide di (nome metallico). Nel caso di Hg2(OH)2, Ad esempio, sarebbe il diidrossido di dimercurio; Uno degli idrossidi la cui struttura chimica è complessa a prima vista. Alcuni esempi di idrossidi e le loro corrispondenti nomenclature sono quelli che seguono: -NaOH (idrossido di sodio) -Ca (OH) 2 (idrossido di calcio) -Faith (Oh)3 (Idrossido ferrico; idrossido di ferro (III); o triidrossido di ferro). -V (Oh)5 (Idrossido di pervanate; idrossido di vanadio (V); o pentahidroxide del vanadio). -Sn (Oh)4 (Idrossido isñico; idrossido di stagno (IV); o tetraidrossido di stagno). -Ba (oh)2 (Idrossido di bario o diidrossido di bario). -Mn (oh)6 (Idrossido manganico, idrossido di manganese (VI) o esaidrossido di manganese). -Aguga (idrossido argico, idrossido d'argento o idrossido d'argento). Si noti che per questo composto non vi è alcuna distinzione tra stock e nomenclature sistematiche. -PB (OH)4 (Idrossido plúmbic, idrossido di piombo (IV) o tetraidrossido di piombo). -Liop (idrossido di litio). -CD (OH) 2 (idrossido di cadmio). -Ba (oh)2 (Idrossido di bario). -Idrossido di cromo.Anfoterismo
Strutture
Reazione di disidratazione
Nomenclatura idrossido
Tradizionale
Azione
Sistematico
Esempi di idrossidi
 Aspetto idrossido di sodio
Aspetto idrossido di sodio  Aspetto dell'idrossido di calcio a stato solido
Aspetto dell'idrossido di calcio a stato solido Riferimenti

