Proprietà di idrocarburi aromatici, esempi, applicazioni
- 2769
- 692
- Dante Morelli
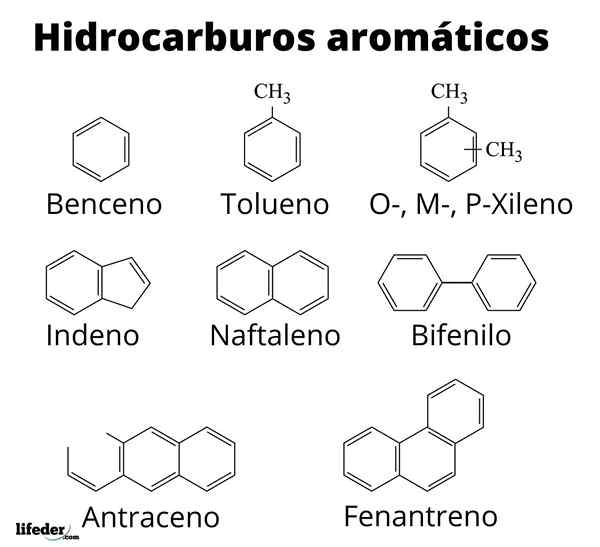
IL idrocarburi aromatici o di sabbia Sono un insieme di composti organici composti solo da carboni e idrogeni e che sono caratterizzati da unità di anelli di benzene nelle loro strutture molecolari.
Alcuni, come sottolinea il suo nome, sparano odori dolci e piacevoli; Motivo per cui i primi prodotti chimici organici si riferivano a loro come aromatici. Il gas metano, ad esempio, è un idrocarburo igienico; Mentre il toluene, liquido volatile, presenta un odore abbastanza peculiare e forte.
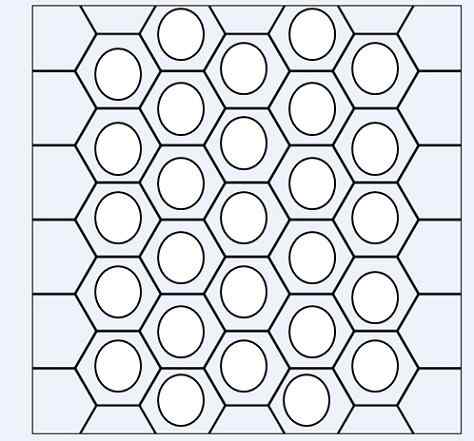 Gli idrocarburi aromatici sono riconosciuti dalle unità di anelli benncitenici
Gli idrocarburi aromatici sono riconosciuti dalle unità di anelli benncitenici Nell'immagine superiore abbiamo una sorta di rete o mesh composta da anelli benzenici. Nota le tue geometrie esagonali e il cerchio all'interno. Questo cerchio rappresenta ciò che è noto come aromaticità, che è una proprietà interamente chimica e non fisica, indipendente dagli odori di questi idrocarburi.
Gli idrocarburi aromatici sono tra i minerali più importanti, estratti o prodotti, petrolio e carbonio. Il benzene è la pietra angolare di questi idrocarburi e le loro applicazioni, poiché da esso derivano sinfine di composti che vengono utilizzati come materie prime per la produzione di fertilizzanti, materie plastiche, adesivi, detergenti, profumi, farmaci, ecc.
[TOC]
Come vengono nominati idrocarburi aromatici?
Un singolo anello di benzene
Per gli idrocarburi aromatici abbiamo la peculiarità che i loro nomi tradizionali o comuni di solito prevalgono rispetto a quelli governati dalla nomenclatura IUPAC.
Tutti contengono l'anello di benzene, o un anello che soddisfa la proprietà dell'aromaticità. Il più semplice può essere nominato secondo il benzene e le posizioni relative dei loro sostituenti.
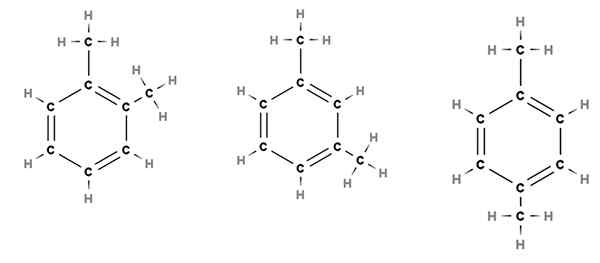 Posizioni relative dei sostituenti in un anello benzenico per la molecola di dimetilbenzene. Fonte: Gabriel Bolívar via Molview.
Posizioni relative dei sostituenti in un anello benzenico per la molecola di dimetilbenzene. Fonte: Gabriel Bolívar via Molview. Ad esempio, considera l'immagine superiore. Nelle tre strutture vediamo l'anello esagonale del benzene, che ha due sostituenti metilici, Cho3. Pertanto, questo composto è chiamato dimetilbenzene, perché è costituito da un benzene con due metilos.
Può servirti: solfato di potassio (K2SO4): struttura, proprietà, usi, sintesiDa sinistra a destra, vediamo che la separazione tra i due3 Diventa maggiore, il che non solo colpisce le proprietà fisiche della molecola, ma modifica anche i rispettivi nomi. Per differenziarli, poiché sono tutti chiamati dimetilbenzene, orto prefissi (o-), obiettivo (m-) e per (p-) vengono utilizzati (p-).
Pertanto, e ancora, da sinistra a destra abbiamo: orto-dimetilbenzene, meta-dimetilbenzene e parametrobenzene. Tuttavia, il nome tradizionale per questo composto è lo xilene, quindi i nomi diventano: orto-xilene, meta-xilene e para-xilene.
Se ci sono più di due sostituenti diversi, viene utilizzato per elencare i carboni seguendo le stesse regole di nomenclatura di tutti gli idrocarburi.
Anelli multipli
Per idrocarburi aromatici con più di un anello benzenico, i nomi tradizionali diventano ancora più importanti. Questo perché i nomi sistematici che descrivono le loro strutture sono ingombranti e difficili da memorizzare. Considera l'esempio di naftalene:
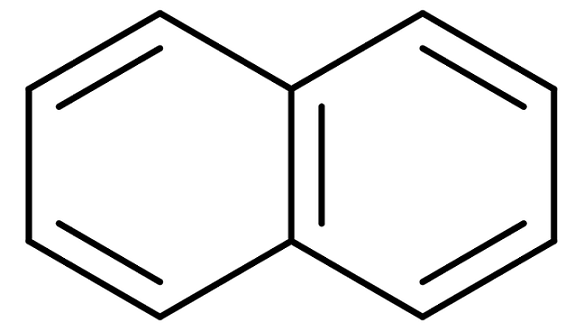 Struttura naftalene
Struttura naftalene Il naftalene è anche commercialmente noto come naftalina o canfora bianca. Tuttavia, il suo nome sistematico è: Biciclo [4,4,0] Dec-1,3,5,7,9 Pentane. E questo solo per un composto con due anelli benzenici uniti; La nomenclatura diventa molto più complicata per i composti con tre o più anelli.
Proprietà degli idrocarburi aromatici
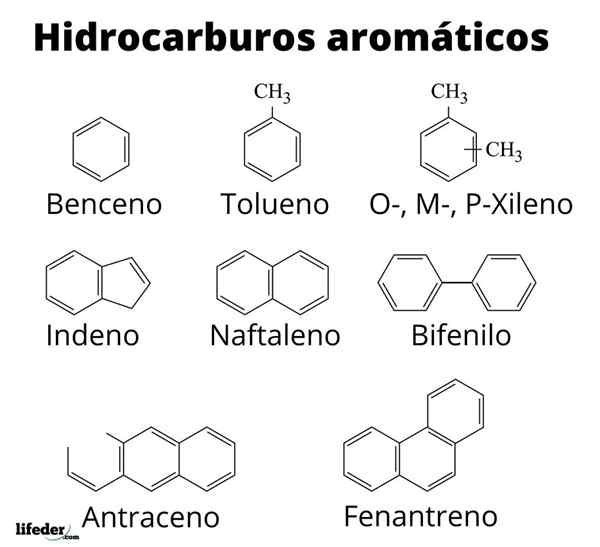 Struttura di alcuni idrocarburi aromatici
Struttura di alcuni idrocarburi aromatici Aromaticità
Gli idrocarburi aromatici contengono anelli che obbediscono alle regole di Huckel. Cioè, i loro anelli devono avere atomi con ibridazioni SP2, essere il più piatto possibile e avere un numero di elettroni π elocati pari a 4N + 2. Ad esempio, il benzene è aromatico perché ha 6 elettroni democati per N= 1 (4 · 1 + 2 = 6).
Alte relazioni C/H
Le relazioni c/h per idrocarburi aromatici sono alte o superiori a 1. Ad esempio, per il benzene, C6H6, Il tuo C/H è uguale a 6/6 o 1. Nel frattempo, per Naftalene, C10H8, Il tuo C/H è uguale a 10/8 o 1.25. Cosa significa questo? Che questi idrocarburi siano molto "gassati" rispetto ad altri composti.
Può servirti: acido solfonico: struttura, nomenclatura, proprietà, usiFiamme gialle
Proprio a causa delle loro alte relazioni C/H, quando gli idrocarburi aromatici vengono bruciati fiamme gialle di fuoco, il prodotto delle particelle di carbone formate (fuliggine).
Reazioni di sostituzione
Gli idrocarburi aromatici possono sostituire i loro atomi di idrogeno con qualsiasi altro sostituente. Ciò si ottiene attraverso due tipi di reazioni organiche: sostituzione elettrofila aromatica (SEAR) o sostituzione nucleofila aromatica (SNAR).
Fragranze
Gli idrocarburi aromatici, come suggeriscono il loro nome, sono caratterizzati da odori dolci o forti. Questa proprietà ha permesso loro di differenziarli, in linea di principio, da idrocarburi gassosi e alcuni paraffini di scarabei.
Esempi di idrocarburi aromatici
Gli idrocarburi aromatici, a rigor di termini, riguardano solo quelli composti da carbonio e idrogeno. Non dovrebbe esserci eteroátomos (o, p, n, s, ecc.). Pertanto, i seguenti esempi che verranno menzionati lasciano fuori composti come piridina, furano o fenolo.
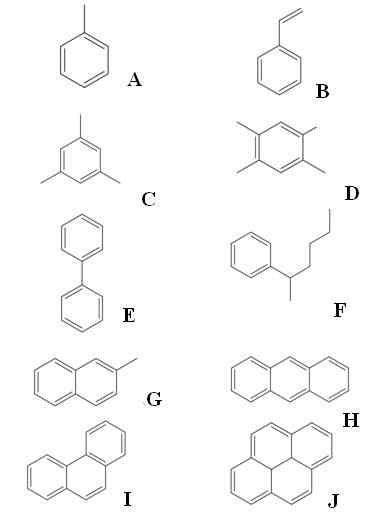 Esempi di idrocarburi aromatici. Fonte: Gabriel Bolívar via Molview.
Esempi di idrocarburi aromatici. Fonte: Gabriel Bolívar via Molview. Up abbiamo dieci esempi di idrocarburi aromatici. Nota che tutti hanno almeno un anello benzenico. I loro nomi sono:
A: toluene
B: allungamento
C: Mesitileno
D: tardi
E: bifenil
F: 2-Fenilhexan
G: 2-metilnaftene
H: Antracen
I: Fenantreno
J: Pireno
Di tutti loro, il toluene è quello con il più grande valore industriale.
Applicazioni/usi
La maggior parte delle applicazioni di idrocarburi aromatici consistono nel fungere da materia prima per la sintesi o la produzione, prodotti con alto valore commerciale. Quasi tutti iniziano dal benzene, che è soggetto a diverse reazioni organiche per ottenere derivati funzionali.
Fibre e materie plastiche
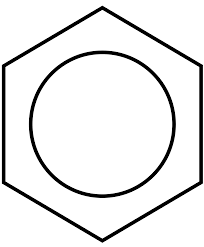 Benzene
Benzene Dal benzene c'è cicloesano, che viene successivamente trasformato in altri composti per sintetizzare il nylon 6 o il nylon 66. D'altra parte, il tratto può essere ottenuto anche dal benzene, che consiste nel monomero del polistirolo. Pertanto, abbiamo i polimeri necessari per la produzione di fibre e materie plastiche.
Può servirti: energia di attivazioneResine epossidiche
Dal benzene, inoltre, il bisfenolo A può essere sintetizzato, con cui si verificano, seguendo varie rotte di sintesi, resine epossidiche, colla, adesivi e persino dipinti.
Detergenti
Gli alchines con lunghe catene laterali servono per la produzione di detergenti; Tra questi, alchio.
Tnt
Dal toluene puoi produrre TNT: trinitrotoluene, uno degli esplosivi più noti.
Acido benzoico
Dal toluene, l'acido benzoico è ottenuto come composto derivato, essenziale per le formulazioni di molti profumi, medicinali e cibo.
Solventi
Benzene, toluene e Xileno (BTX), sono i solventi organici più usati nella ricerca sull'olio.
Benzina
Gli idrocarburi aromatici fanno anche parte della composizione della benzina, con il ruolo principale di aumentare il suo indice di ottano o ottano.
Riferimenti
- Graham Solomons t.W., Craig b. Frigorifero. (2011). Chimica organica. (10th Edizione.). Wiley Plus.
- Carey f. (2008). Chimica organica. (Sesta edizione). Mc Graw Hill.
- Morrison e Boyd. (1987). Chimica organica. (Quinta edizione). Addison-Wesley Iberoamericana.
- Wikipedia. (2020). Composto aromatico. Recuperato da: in.Wikipedia.org
- Ed Vitz et al. (8 settembre 2020). Idrocarburi aromatici. Chimica librettexts. Recuperato da: Chem.Librettexts.org
- Wyman Elizabeth. (2020). Idrocarburi aromatici: definizione, esempio e uso. Studio. Recuperato da: studio.com
- Boluda, c. J., Macías, m., & González Marrero, J. (2019). La complessità chimica della benzina automobilistica. Scienza, ingegneria e applicazioni,2(2), 51-79. Doi: doi.org/10.22206/CYAP.2019.V2i2.PP51-79
- « Conservazione del principio di momenta lineare, esempi, esercizi.
- Preghiere con G Esempi e regole di utilizzo »

