Struttura, proprietà e usi Eptano (C7H16)
- 1839
- 195
- Rufo Longo
Lui Eptano È un composto organico la cui formula chimica è C7H16 e comprende nove isomeri strutturali, di cui il più noto è il lineare. È un idrocarburo, in particolare un alcano o paraffina, che è nella maggior parte dei laboratori di chimica organica, sia che insegnamento o ricerca.
A differenza di altri solventi paraffinici, l'eptano ha una volatilità inferiore, che rende relativamente più sicuro; Ogni volta che non vi è alcuna fonte di calore che circonda i tuoi vapori e viene lavorato all'interno di una campana di estrattore. Lasciando da parte la sua infiammabilità, è un composto sufficientemente inerte per servire come mezzo di reazioni organiche.
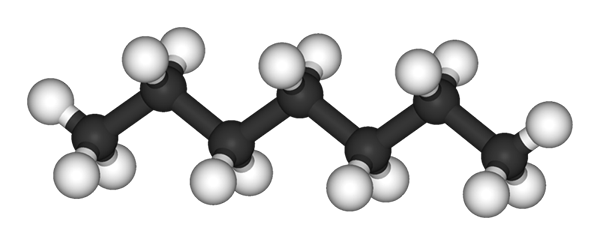
 Molecola n-heptano rappresentato da un modello di sfere e barre. Fonte: Ben Mills e Jynte [dominio pubblico]
Molecola n-heptano rappresentato da un modello di sfere e barre. Fonte: Ben Mills e Jynte [dominio pubblico] Nell'immagine superiore hai la struttura del N-Eptano, l'isomero lineare di tutti gli eptani. Poiché è l'isomero più comune e di maggiore valore commerciale, così come il più semplice da sintetizzare, tende ad essere alla fine che il termine "eptano" si riferisce esclusivamente a N-Eptano; salvo diversa indicazione.
Tuttavia, nelle bottiglie di questo composto liquido si specifica che contiene N-Eptano. Devono scoprire all'interno di una campana di estrattore ed eseguire attentamente le misurazioni.
È un solvente eccellente per grassi e oli, quindi viene spesso usato durante le essenze vegetali o altri prodotti naturali.
[TOC]
Struttura
n-eptano e le sue interazioni intermolecolari
Come si può vedere nella prima immagine, la molecola di N-L'eptano è lineare e a causa dell'ibridazione chimica dei suoi atomi di carbonio, la catena adotta una forma di zigzagueada. Questa molecola è dinamica, perché i suoi legami C-C possono ruotare, il che fa piegare leggermente la catena con angoli diversi. Ciò contribuisce alle sue interazioni intermolecolari.
Può servirti: PI LinkLui N-L'eptano è una molecola apolare e idrofobica, e quindi le sue interazioni si basano sulle forze dispersive di Londra; Questi sono, quelli che dipendono dalla massa molecolare del composto e dalla sua area di contatto. Due molecole di N-eptano.
Queste interazioni sono abbastanza efficaci da mantenere le molecole di N-Eptano coeso in un liquido che bolle a 98 ºC.
Isomeri
 I nove isomeri di Heptan. Fonte: Steffen 962 [dominio pubblico]
I nove isomeri di Heptan. Fonte: Steffen 962 [dominio pubblico] All'inizio si diceva che la formula C7H16 rappresentava un totale di nove isomeri strutturali, essendo il N-Eptane il più rilevante (1). Gli altri otto isomeri sono mostrati nell'immagine superiore. Nota ad occhio nudo che alcuni sono più ramificati di altri. Da sinistra a destra, a partire dall'alto, abbiamo:
(2): 2-metilhexan
(3): 3-metilhexan, che consiste in una coppia di enantiomeri (A e B)
(4): 2,2-dimetilpentano, noto anche come neoheptano
(5): 2,3-dimetilpentano, di nuovo con una coppia di enantiomeri
(6): 2,4-dimetilpentano
(7): 3.3-dimetilpentano
(8): 3-etilpentane
(9): 2,2,3-trimetilbutano.
Ognuno di questi isomeri ha proprietà e applicazioni indipendenti del N-Eptano, riservato più di ogni altra cosa per le aree di sintesi organica.
Proprietà di Hepthane
Aspetto fisico
Liquido incolore con un odore simile alla benzina.
Massa molare
100.205 g/mol
Punto di fusione
-90.549 ºC, diventando un cristallo molecolare.
Punto di ebollizione
98.38 ºC.
Pressione del vapore
52,60 atm a 20 ºC. Nota quanto è alta la pressione del vapore, nonostante sia meno volatile di altri solventi paraffinici, come Hexano e Pentan.
Densità
0,6795 g/cm3. D'altra parte, i vapori di Heptano sono 3,45 volte densi dell'aria, il che significa che i loro vapori dureranno negli spazi dove una piccola fuoriuscita del loro liquido.
Può servirti: acido formico (hcooh)Solubilità dell'acqua
L'eptano per essere un composto idrofobico può appena dissolversi nell'acqua per causare una soluzione con una concentrazione dello 0,0003% a una temperatura di 20 ºC.
Solubilità in altri solventi
L'epthane è miscibile con tetracloruro di carbonio, etanolo, acetone, etere di petrolio e cloroformio.
Indice di rifrazione (ND)
1.3855.
Sostanza vischiosa
0,389 mpa · s
Capacità termica
224.64 J/K · Mol
punto di accensione
-4 ºC
Temperatura di autorezione
223 ºC
Tensione superficiale
19,66 mn/m a 25 ºC
Calore a combustione
4817 kJ/mol.
Reattività
I vapori di Hepthane quando sono vicini a una fonte di calore (una fiamma), reagiscono esotermicamente e vigorosamente con l'ossigeno dell'aria:
C7H16 + 11o2 => 7co2 + 8h2O
Tuttavia, al di fuori della reazione di combustione, l'eptano è un liquido abbastanza stabile. La sua mancanza di reattività è dovuta al fatto che i loro collegamenti C-H sono difficili da rompere, quindi non è suscettibile alle sostituzioni. Inoltre non è molto sensibile agli agenti ossidanti forti, a condizione che non vi sia fuoco nelle vicinanze.
Il più grande pericolo di eptano è rappresentato dalla sua elevata volatilità e infiammabilità, quindi c'è un rischio di incendio se viene versato in siti caldi.
Applicazioni
Solvente e mezzo di reazione
 Hepthane è un solvente eccellente per dissolvere oli e grassi. Fonte: pxhere.
Hepthane è un solvente eccellente per dissolvere oli e grassi. Fonte: pxhere. Il carattere idrofobico di Eptano è un eccellente solvente per sciogliere oli e grassi. In questo aspetto è stato usato come sgrassatore. Tuttavia, la sua più grande applicazione risiede nell'essere utilizzata come solvente di estrattore, poiché dissolve i componenti lipidici, così come gli altri composti organici di un campione.
Ad esempio, se desideri estrarre tutti i componenti del caffè macinato, sarebbe macerato a eptano anziché in acqua. Questo metodo e le sue varianti sono stati implementati con tutti i tipi di semi, grazie a cui sono state ottenute essenze vegetali e altri prodotti naturali.
Può servirti: cellula unitaria: proprietà, costanti e tipi rossiL'eptano, che è naturalmente incolore, sarà tinto dal colore dell'olio estratto. Quindi, questo viene ruotato per avere finalmente un volume di olio il più puro possibile.
D'altra parte, la piccola reattività dell'eptano ti consente anche di essere un'opzione quando si considera un mezzo di reazione per effettuare una sintesi. Essendo un buon solvente di composti organici, garantisce che i reagenti rimangono in soluzione e interagiscono tra loro mentre reagiscono.
Agente precipitante
In chimica del petrolio è una pratica comune precipitare gli asfaltensi di un campione grezzo aggiungendo eptano. Questo metodo consente di studiare la stabilità di diversi grezzi e determinare quanto sia sensibile il suo contenuto di asfaltene è quello di precipitare e trasportare un'intera serie di problemi per l'industria petrolifera.
Ottano
L'eptan è stato usato come carburante a causa della grande quantità di calore che offre quando brucia. Tuttavia, per quanto. Perché brucia in modo molto esplosivo, serve a definire lo 0 sulla scala ottana di benzina.
La benzina contiene un'alta percentuale di eptano e altri idrocarburi per livellare l'ottano a valori noti (91, 95, 87, 89, ecc.).
Riferimenti
- Morrison, r. T. e Boyd, r, n. (1987). Chimica organica. 5a edizione. Editoriale Addison-Wesley Inter-American.
- Carey f. (2008). Chimica organica. (Sesta edizione). Mc Graw Hill.
- Graham Solomons t.W., Craig b. Frigorifero. (2011). Chimica organica. (10a edizione.). Wiley Plus.
- Wikipedia. (2020). Eptano. Recuperato da: in.Wikipedia.org
- Centro nazionale per le informazioni sulla biotecnologia. (2020). Database pubchem Heptane. CID = 8900. Recuperato da: pubchem.NCBI.Nlm.NIH.Gov
- Elsevier b.V. (2020). Eptani. Scienceirect. Estratto da: ScienceDirect.com
- Bell Chem Corp. (7 settembre 2018). Usi industriali di eptano. Recuperato da: Bellchem.com
- Andrea Kropp. (2020). Eptane: struttura, usi e formula. Studio. Recuperato da: studio.com
- « Formula condensata cosa è ed esempi (metano, etano, glucosio ...)
- Formule di energia meccanica, concetto, tipi, esempi, esercizi »

