Formula condensata cosa è ed esempi (metano, etano, glucosio ...)
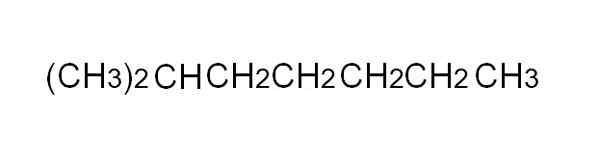
- 2631
- 783
- Lino Lombardi
IL Formula condensata È una rappresentazione puramente testuale di una molecola in cui vengono omessi i collegamenti. Il suo scopo è sapere qual è l'ordinamento degli atomi. Le molecole generalmente lineari o ramificate hanno formule condensate, tranne cicliche o quelle altamente ramificate.
Nella chimica organica c'è di solito la confusione di quale sia la differenza tra questa formula e molecolare. In effetti, è comune trovarli come sinonimi. Nel frattempo, in chimica inorganica le formule molecolari sono più usate, poiché nella maggior parte dei casi i composti covalenti descrivono giustamente; Come l'acqua, h2O.
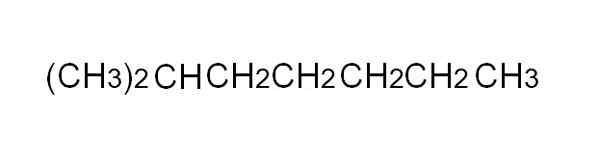 Formula condensata di 2-metilheptano. Fonte: Gabriel Bolívar.
Formula condensata di 2-metilheptano. Fonte: Gabriel Bolívar. [TOC]
Qual è la formula condensata?
Per definirlo in modo più conveniente, la formula condensata è una rappresentazione semplificata del semi -sviluppato. Non è necessario scrivere i collegamenti semplici, né coprire più di una riga in un testo. Ad esempio, il 2-metilheptano, un alcano ramificato, può essere rappresentato nella stessa linea dell'immagine superiore.
Le formule condensate sono utili per rappresentare alcune molecole senza doverle disegnarle. Questo è eccellente quando vengono scritte equazioni chimiche in cui le molecole cicliche o molto ramificate non partecipano. Si vedrà che queste formule ricorrono alle parentesi per semplificare ulteriormente la rappresentazione di una molecola.
Esempi
Metano
Il metano è l'unico composto chimico che ha una singola formula: CH4. Ciò corrisponde all'empirico, molecolare, condensato e semi -sviluppato allo stesso tempo. Ecco perché molte volte, per salvare una confusione tra tutti questi concetti, le persone preferiscono fare riferimento semplice e impreciso alla "formula chimica" di un composto.
Etano
Estano ha una formula molecolare C2H6. La formula condensata invece è Cho3Cap3. Si noti che i collegamenti C-C e i collegamenti C-H sono omessi. L'idea è di essere in grado di scrivere la formula come se fosse una "parola", senza dover disegnare strisce o disegnare strutture.
Può servirti: pycnometerPer definizione, la formula molecolare è C2H6 e non ch3Cap3; Tuttavia, per le molecole semplici, entrambe le formule sono consuete da scambiare, sebbene sia ancora errata. Questo è un punto di discrepanza tra diverse fonti, in cui vi sono apparentemente regole specifiche al riguardo.
Glucosio e fruttosio
Ecco un esempio in cui viene immediatamente osservato un errore quando si desidera scambiare la formula molecolare con la condensa.
La coppia dolce, glucosio e fruttosio ha la stessa formula molecolare: C6H12O6, E quindi questo non serve a differenziarli. Al contrario, le formule strutturali e semi -sviluppate stabiliscono molecole diverse in vista.
Tuttavia, il glucosio o il fruttosio hanno una formula condensata. Questo perché indipendentemente dalla loro rappresentazione o proiezione, le loro strutture non possono essere scritte nella stessa linea; O almeno, in un modo piacevole e semplice agli occhi del lettore.
Butano
Butano ha una formula molecolare C4H10. Ha due isomeri: il lineare, N-Butano e ramificato, 2-metilpropano. Entrambi possono essere rappresentati dalle loro formule condensate. Lui N-Butano è Ch3Cap2Cap2Cap3 o ch3(Ch2)2Cap3, E il 2-metilpropano è Cho3Ch (Ch3)2 o (ch3)3Cap.
Nel 2-metilpropano abbiamo un gruppo di gruppo circondato da tre Cho3. Le sue due formule sono valide e le parentesi vengono utilizzate per evidenziare le ramificazioni, l'abbonamento è un indicatore di quanti gruppi compongono questo ramo.
Etanolo
L'etanolo ha una formula condensata CH3Cap2OH. Nota quanto assomiglia alla sua formula semi -sviluppata: CH3-Cap2-OH. Allo stesso modo è fatto con il propanolo, Cho3Cap2Cap2Oh, il N-Butanolo, ch3Cap2Cap2Cap2Oh, e con tutti gli altri alcoli.
Può servirti: fosfato di sodio: struttura, proprietà, sintesi, usiSe hanno un ramo, sarà indicato all'interno di una parentesi a destra dell'atomo con cui è collegato. Ad esempio, il 2-metilbutanolo potrebbe essere scritto come: CH3Cap2Ch (Ch3) Ch2OH. Si noti che per molte molecole inizia ad essere più conveniente ricorrere a una formula strutturale o semi -sviluppata.
Pentano
L'isomero lineare di Pentan, N-Pentano, è facile da rappresentare per la sua formula condensata: Cho3Cap2Cap2Cap2Cap3. Questa formula può anche essere semplificata usando parentesi: CH3(Ch2)3Cap3, indicando che tra i due ch3 Ci sono tre ch2.
Gli altri due isomeri del Pentan, tuttavia, sono un po 'più complicati: CH3Cap2Ch (Ch3)2, Per 2-metilbutane e c (CH3)4 Per 2,2-dimetilpropano o neopantum. Si noti che l'atomo di carbonio a sinistra della parentesi è quello che forma i collegamenti a sostituenti o ramificazioni.
Ottano
L'isomero lineare dell'ottano, N-Octane, per la sua lunghezza, è ora opportuno rappresentare la sua formula condensata come Cho3(Ch2)6Cap3. È a questo punto in cui dovrebbe essere qualcosa di chiaro dalle formule condensate: cercano di risparmiare tempo quando rappresentano molecole o composti, senza scrivere così tanto su carta.
Cicloesano
Il caso del cicloesano è simile a quello del glucosio e del fruttosio: ha formalmente manca una formula condensata per essere un composto ciclico. Un modo per cercare di rappresentarlo sarebbe: (Ch2)6, che implica che sei gruppi Cho2 Devono essere collegati, essendo possibili solo se si chiudono in un anello esagonale. Tuttavia, è meglio disegnare l'anello.
Acetone
L'acetone presenta la peculiarità di possedere un gruppo carbonilico, c = o. Pertanto, per scrivere la tua formula condensata abbiamo tre opzioni: (CH3)2CO, Ch3C (o) ch3 o ch3(C = o) ch3.
Può servirti: acido caffè: struttura, proprietà, biosintesi, usiIn effetti, nelle molecole più grandi il gruppo carbonilico è generalmente rappresentato come (O), tenendo conto del fatto che l'atomo di carbonio alla sua sinistra è quello che forma il doppio legame con ossigeno, c = o.
Acido acetico
La formula condensata dell'acido acetico è Cho3COOH O CH3Co2H. Ecco un punto importante: i gruppi funzionali scritti nella stessa linea sono parti di una formula condensata. Questo è stato il caso di etanolo e acetone e si applica anche ai tiolle (-sh), aldeide (-cho) gli esteri (-co2R o -coor) e ammine (-nh2).
Commento generale
Ci sono molte confusione tra formule molecolari e condensate. Forse è perché queste rappresentazioni da sole forniscono già un'immagine approssimativa della molecola, quindi pensiamo che sia la formula molecolare.
Inoltre, formule come C6H12O6 Sono anche considerati condensati, perché sono semplificati, "condensa" la molecola in atomi e abbonamenti. Ecco perché è comune vedere come vengono menzionate le due formule come se fossero sinonimi.
In molte fonti, compresi gli articoli di Wikipedia, i termini "formula chimica" sono usati per fare riferimento a molecolare (tipo C6H12O6 e altri) e "formula" per fare riferimento alla condensa.
Riferimenti
- Whitten, Davis, Peck e Stanley. (2008). Chimica. (8 ° ed.). Apprendimento del Cengage.
- Helmestine, Anne Marie, PH.D. (18 novembre 2019). Definizione della formula condensata in chimica. Recuperato da: Thoughtco.com
- James Ashenhurst. (11 dicembre 2019). Formule condensate: decifrare cosa significano le spalle. Chimica organica principale. Recuperato da: MasterOrganicChemistry.com
- Copolingenieria. (2 maggio 2016). Formula empirica, strutturale e condensata. Estratto da: Chemiotecablog.WordPress.com
- Introduzione alla chimica: generale, organico e biologico. (S.F.). Formule strutturali e angolo di linea condensate. Recuperati da: libri 2012.Lardbucket.org

