Caratteristiche statali gassose, diritto generale, esempi

- 3396
- 116
- Kayla Serr
Lui Stato gassoso È uno stato di aggregazione del soggetto in cui le particelle sono tenute insieme da interazioni deboli, essendo in grado di muoversi attraverso tutte le direzioni del contenitore che li contiene. Di tutti gli stati fisici del soggetto, il gassoso è quello che manifesta la più grande libertà e il caos.
I gas esercitano pressione, trasportano calore e sono composti da qualsiasi tipo di piccola particelle. La nostra atmosfera e l'aria che respiriamo è una manifestazione dello stato gassoso qui sulla terra.
 Nelle emanazioni di fumo il comportamento dei gas può essere osservato prima di dispersi nell'atmosfera. Fonte: Pexels.
Nelle emanazioni di fumo il comportamento dei gas può essere osservato prima di dispersi nell'atmosfera. Fonte: Pexels. Esempi di gas sono gas serra, come vapore acqueo, anidride carbonica, metano o ozono. L'anidride carbonica che espiriamo nella respirazione è un altro esempio di sostanza gassosa.
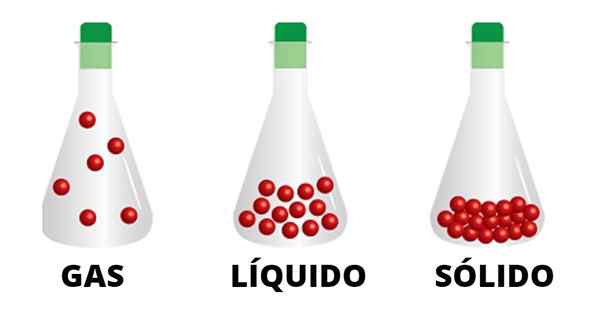 Le particelle gassose sono collegate da interazioni deboli e si muovono dal contenitore. Si osserva che le particelle dello stato liquido sono più unite e quelle del solido strettamente collegato
Le particelle gassose sono collegate da interazioni deboli e si muovono dal contenitore. Si osserva che le particelle dello stato liquido sono più unite e quelle del solido strettamente collegato Liquidi e solidi, ad esempio, non si sposteranno in posizioni oltre i propri limiti di materiale, un fatto che non accade con i gas. Il fumo delle sigarette, i camini e le torri, dimostrano da soli come il gas è salito e disperso dall'ambiente senza fermarlo.
[TOC]
Caratteristiche statali gassose
Manca di volume o forma
Lo stato gassoso è caratterizzato dal non avere forma o volume definita. Se non ci sono confini per trattenerlo, si disperderà in tutta l'atmosfera. Anche come con l'elio, fuggirà fuori dalla terra.
Un gas può acquisire solo la forma imposta da un contenitore. Se un contenitore è cilindrico, il gas "avrà" forma del cilindro.
Può servirti: calorimetria: quali studi e applicazioniCattivo driver di calore
Questo stato è anche caratterizzato da un cattivo conduttore di calore ed elettricità. In generale, è meno denso rispetto agli stati solidi e liquidi.
Poiché la maggior parte dei gas sono incolori, come l'ossigeno e l'anidride carbonica, si può determinare quanto ci sono in un contenitore per mezzo della misura della loro pressione.
Reagenti
I gas tendono ad essere più reattivi, ad eccezione dei gas nobili, rispetto ai liquidi o al solido.
Piccole particelle
Le particelle gassose sono anche di solito piccole, essendo atomi o molecole semplici.
Ad esempio, idrogeno gassoso, h2, È una molecola molto piccola formata da due atomi di idrogeno. Abbiamo anche l'elio, lui, i cui atomi sono ancora più piccoli.
Interazioni
Le interazioni nello stato gassoso sono spregevoli. Questo è molto diverso dagli stati liquidi e solidi, in cui le loro particelle sono molto coesive e interagiscono fortemente l'una dall'altra. Nelle molecole che formano gli stati liquidi e solidi non c'è quasi nessun vuoto molecolare tra loro.
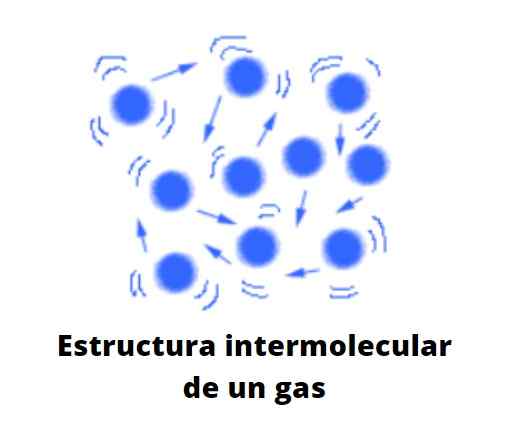
Le particelle nello stato gassoso sono molto distanziate una delle altre, c'è molto vuoto tra loro. Non è più un vuoto su scala molecolare. La distanza che li separa è così tanto che ogni particella nel gas è libera, indifferente all'ambiente circostante, a meno che nella sua traiettoria caotica si colpisca con un'altra particella o contro la parete del contenitore.
Può servirti: soluzione diluitaSe si presume che non vi sia un contenitore, il vuoto tra le particelle di gas può essere occupato dall'aria, che spinge e trascina il gas verso la direzione della sua corrente. Ecco perché l'aria, che consiste in una miscela gassosa, è in grado di deformare e diffondere le sostanze gassose, purché non siano molto più densi di lui.
Legge statale gassosa generale
Lo studio sperimentale del comportamento e dei meccanici dei gas ha portato a diverse leggi (Boyle, Charles, Gay-Lussac) che si combinano per prevedere quali saranno i parametri di qualsiasi sistema di gas o fenomeno, cioè quale sarà la sua temperatura, volume, volume e pressione.
Questa legge generale ha la seguente espressione matematica:
P = kt/v
Dove k è una costante, p la pressione e il volume e la temperatura del gas in scala Kelvin. Pertanto, conoscendo due variabili (per dire, p e v), il terzo può essere cancellato, che sarebbe l'ignoto (t).
Questa legge consente, ad esempio, quale dovrebbe essere la temperatura di un gas, bloccata in un contenitore di volume V, visualizzare una pressione P.
Se aggiungiamo il contributo di Amadeus Avogadro a questa legge, avremo quindi la legge ideale sui gas, che coinvolge anche il numero di particelle e con loro la concentrazione molare del gas:
P = nrt/v
Dove N corrisponde al numero di moli di gas. L'equazione può essere riscritta come:
P = crt
Dove C È la concentrazione molare di gas (N/V). Pertanto, da una legge generale, si ottiene la legge ideale che descrive come si riferiscono la pressione, la concentrazione, la temperatura e il volume di un gas ideale.
Può servirti: setacciatoEsempi di stato gassoso
Elementi gassosi
La stessa tavola periodica offre un buon repertorio di esempi di elementi che sono presentati sulla terra come gas. Tra loro abbiamo:
-Idrogeno

-Elio
-Azoto
-Ossigeno
-Fluoro
-Cloro
-Neon
-Argon
-Kripton
-Xeno
Ciò non significa che altri elementi non possano diventare gassosi. Ad esempio, i metalli possono essere trasformati in gas se sono soggetti a temperature più elevate rispetto ai rispettivi punti di ebollizione. Pertanto, potrebbero esserci gas di ferro, mercurio, argento, oro, rame, circonferenti, iridium, particelle di Osmio; di qualsiasi metallo.
Composti gassosi
Nell'elenco seguente abbiamo alcuni esempi di composti gassosi:
-Monossido di carbonio, CO
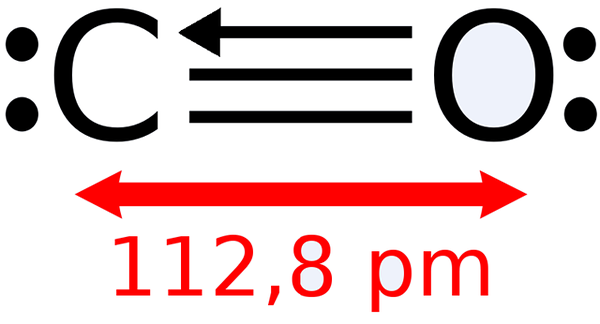 Struttura di Lewis del monossido di carbonio
Struttura di Lewis del monossido di carbonio -Anidride carbonica, co2 (gas che forma le nostre espilazioni)
-Ammoniaca, NH3 (Sostanza vitale per i processi industriali Sinfine)
-Triossido di zolfo, così3
-Metano, ch4 (gas domestico, con cui è cotto)
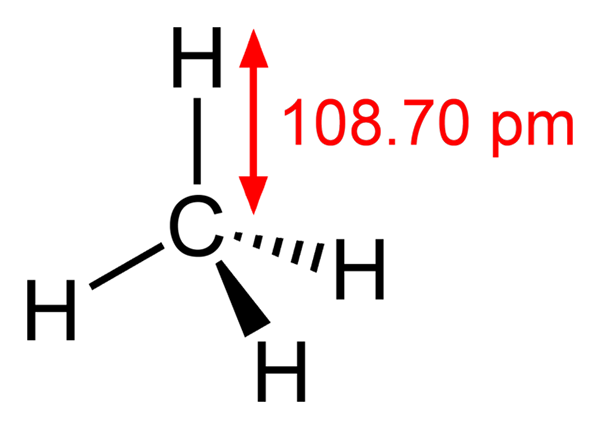 Struttura metano
Struttura metano -Etano, ch3Cap3
-Biossido di azoto, no2 (Gas di colorazione marrone)
-Phosgen, Cocl2 (sostanza altamente velenosa)
-Aria (essendo una miscela di azoto, ossigeno, argon e altri gas)
-Vapore d'acqua, h2O (che fa parte di nuvole, geisers, vaporizzatori di macchine, ecc.).
-Acetilene, hc Tutto
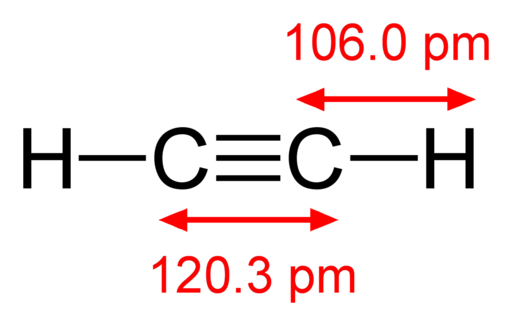 Formula strutturale di acetilene
Formula strutturale di acetilene -Vapori di iodio, io2 (Gas di colore viola)
-Hexafluororo di zolfo, SF6 (gas molto denso e pesante)
-Idrazina, n2H4
-Cloruro di idrogeno, HCl (che sciolto in acqua produce acido cloridrico)
Riferimenti
- Whitten, Davis, Peck e Stanley. (2008). Chimica. (8 ° ed.). Apprendimento del Cengage.
- Wikipedia. (2020). Gas. Recuperato da: in.Wikipedia.org
- Edward a. Muratore. (6 febbraio 2020). Gas. Encyclopædia Britannica. Recuperato da: Britannica.com
- Helmestine, Anne Marie, PH.D. (11 febbraio 2020). Definizione del gas ed esempio in chimica. Recuperato da: Thoughtco.com
- María Estela Raffino. (12 febbraio 2020). Qual è lo stato gassoso? Recuperato da: concetto.Di

