Collegamento glicosidico Cosa sono, caratteristiche, tipi, nomenclatura
- 4005
- 588
- Benedetta Rinaldi
IL Collegamenti glicosidici Sono i legami covalenti che si verificano tra zuccheri (carboidrati) e altre molecole, che possono essere altri monosaccaridi o altre molecole di natura diversa.
Questi collegamenti rendono possibile l'esistenza di più componenti fondamentali per la vita, non solo nella formazione di carburanti di riserva ed elementi strutturali, ma anche di molecole essenziali di trasporto di informazioni per la comunicazione cellulare.
La formazione di polisaccaridi dipende fondamentalmente dalla creazione di legami glicosidici tra alcoli o gruppi idrossile liberi di singoli unità monosaccaridiche.
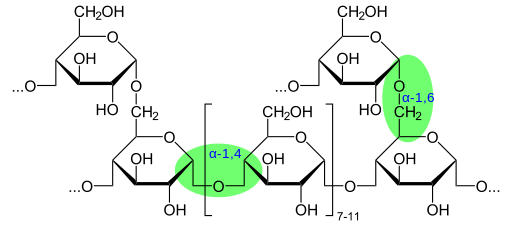 Esempio di legame glicosidico in glicogeno (fonte: glicogeno.SVG-Neurotkerrivative-Work-Marek-M-Public-Domain tramite Wikimedia Commons)
Esempio di legame glicosidico in glicogeno (fonte: glicogeno.SVG-Neurotkerrivative-Work-Marek-M-Public-Domain tramite Wikimedia Commons) I collegamenti glicosidici si verificano in più contesti cellulari, tra cui l'unione del gruppo di testa polare di alcuni sfingolipidi, componenti essenziali delle membrane cellulari di molti organismi e la formazione di glicoproteine e proteoglicani.
Polisaccaridi importanti come cellulosa, chitina, agar, glicogeno e amido non sarebbero possibili senza legami glucosidici. Allo stesso modo, la glicosilazione proteica, che si verifica nel reticolo endoplasmatico e nel complesso del Golgi, è della massima importanza per l'attività di molte proteine.
Caratteristiche
I legami glicosidici sono molto più vari rispetto ai loro analoghi nelle proteine e negli acidi nucleici, poiché in principio due molecole di zucchero possono unirsi in molti modi, perché hanno più gruppi -OH che possono partecipare alla formazione del collegamento.
Inoltre, gli isomeri dei monosaccaridi, cioè uno dei due orientamenti che il gruppo idrossilico può avere nella struttura ciclica rispetto al carbonio anomerico, forniscono un ulteriore livello di diversità.
Gli isomeri hanno diverse strutture tridimensionali, nonché diverse attività biologiche. Cellulosa e glicogeno sono costituiti da unità ripetute di d-glucosio ma differiscono in termini di tipo di legame glucosidico (α1-4 per glicogeno e β1-4 per cellulosa) e quindi hanno proprietà e funzioni diverse.
Proprio come i polipeptidi hanno una polarità con una fine n e un altro c- e i polinucleotidi hanno estremità da 5 'e 3', i polisaccaridi oligo-or hanno una polarità definita dalla riduzione delle estremità e non.
L'estremità riducente ha un centro anomerico libero che non forma un collegamento glicosidico con un'altra molecola, quindi mantiene la reattività chimica dell'aldeide.
Può servirti: fertilizzazione esternaIl legame glucosidico è la regione più flessibile di un polisaccaride oligo-o.
Formazione di legami glicosidici
Il legame glucosidico può unirsi a due molecole monosaccaride attraverso l'una e il gruppo idrossilico dell'altro. Cioè, il gruppo emiacetico di uno zucchero reagisce con il gruppo di alcol di un altro per formare un acetale.
In generale, la formazione di questi collegamenti avviene per reazioni di condensa, in cui una molecola d'acqua viene rilasciata con ciascun collegamento che si forma.
Tuttavia, in alcune reazioni l'ossigeno non abbandona la molecola di zucchero come acqua, ma come parte del gruppo difosfato di un nucleotide di difosfato di uridina.
Le reazioni che danno origine ai collegamenti glucosidici sono catalizzate da una classe di enzimi noti come glicosiltransferasi. Si formano tra uno zucchero covalentemente modificato dall'aggiunta di un gruppo fosfato o un nucleotide (glucosio a 6-fosfato, UDP-galattosio, per esempio) che si lega alla catena di crescita in crescita in crescita.
Idrolisi del legame glicosidico
I legami glicosidici possono facilmente idrolizzare in ambienti leggermente acidi, ma resistono a ambienti piuttosto alcalini.
L'idrolisi enzimatica dei legami glucosidici è mediata dagli enzimi noti come glicosidasi. Molti mammiferi non possiedono questi enzimi per la degradazione della cellulosa, quindi non sono in grado di estrarre energia da questo polisaccaride, nonostante siano una sorgente di fibra essenziale.
Ruminanti come le mucche, ad esempio, hanno batteri associati al loro intestino che producono enzimi in grado di degradare la cellulosa che mangiano, il che li rende in grado di sfruttare l'energia conservata nei tessuti vegetali.
L'enzima liscio, prodotto nelle lacrime dell'occhio e da alcuni virus batterici, è in grado di distruggere i batteri grazie alla sua attività idrolitica, che rompe il legame glucosidico tra l'acido N-acetilglucosamina e l'acido N-acetilmuramico nella parete cellulare della parete cellulare batteri.
Diversità
Oligosaccaridi, polisaccaridi o glicani sono molecole molto diverse e questo è dovuto ai molteplici modi in cui i monosaccaridi possono unirsi formando strutture di ordine superiore.
Questa diversità inizia dal fatto, come menzionato sopra, che gli zuccheri hanno gruppi idrossilici che consentono diverse regioni sindacali e che i legami possono verificarsi tra i due possibili stereoisomeri rispetto al carbonio anomerico dello zucchero (α o β).
Può servirti: blastozoosI collegamenti glicosidici possono essere formati tra uno zucchero e qualsiasi composto idrossilato come alcoli o aminoacidi.
Inoltre, un monosaccaride può formare due legami glucosidici, quindi può fungere da punto di filiale, introducendo una potenziale complessità nella struttura dei glicani o dei polisaccaridi nelle cellule.
Ragazzi
Per quanto riguarda i tipi di legami glucosidici, due categorie possono essere differenziate: i legami glucosidici tra monosaccaridi che costituiscono gli oligo- e i polisaccaridi e i legami glucosidici che si verificano nei glucoproteine o nei glucolipidi, che sono proteine o lipidi con carboidrati.
Collegamenti O-glucosidici
I collegamenti O-glicosidici si verificano tra monosaccaridi, sono formati dalla reazione tra il gruppo idrossile di una molecola di zucchero e il carbonio anomerico di un altro.
I disaccaridi sono dagli oligosaccaridi più comuni. I polisaccaridi hanno più di 20 unità di monosaccaridi uniti insieme linearmente e talvolta hanno più ramificazioni.
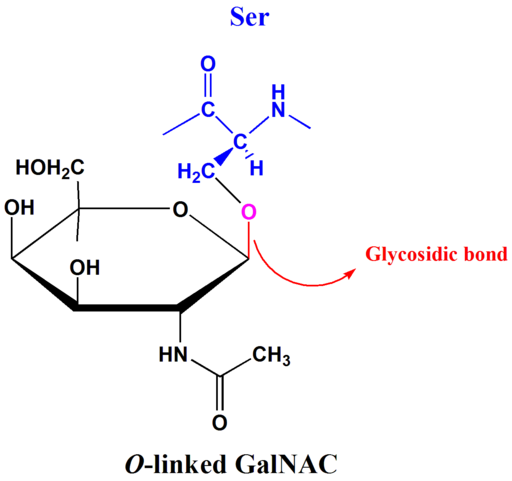 Esempio di collegamento O-glucosidico (fonte: Tpirojsi [dominio pubblico] tramite Wikimedia Commons)
Esempio di collegamento O-glucosidico (fonte: Tpirojsi [dominio pubblico] tramite Wikimedia Commons) In disaccaridi come maltosio, lattosio e saccarosio, il legame glucosidico più comune è il tipo O-glicosidico. Questi collegamenti possono verificarsi tra carboni e -OH delle forme isomeriche α o β.
La formazione di legami glucosidici negli oligo e polisaccaridi dipenderà dalla natura stereochimica degli zuccheri che sono uniti, nonché dal loro numero di atomi di carbonio. In generale, per gli zuccheri con 6 carboni, si verificano legami lineari tra i carboni 1 e 4 o 1 e 6.
Esistono due tipi principali di O-I glicosidi che, a seconda della nomenclatura, sono definiti come α e β o 1.2-Cis e 1.2-trans-Glicosidi.
I rifiuti 1.2-Cis glicosilato, α-glicosidi per d-glicosio, d-galattosio, l-fucosa, d-xilosa o β-glicosidi per d-manosa, l-yarabinosa; così come 1.2-trans (β-glicosidi per d-glucosio, d-galattosio e α-glicosidi per d-many, ecc.), sono di grande importanza per molti componenti naturali.
O-glicosilazione
Una delle modifiche post -traduzionali più comuni è la glicosilazione, che consiste nell'aggiunta di una porzione di glucide a un peptide o proteina in crescita. Le mucine, le proteine di secrezione, possono contenere grandi quantità di catene oligosaccaride collegate da legami O-glucosidici.
Il processo di O -glicosilazione si verifica nel complesso del Golgi degli eucarioti ed è costituito dall'unione delle proteine alla porzione glucidale attraverso un legame glucosidico tra il gruppo -OH di un residuo aminoacid.
Può servirti: glucolipidi: cosa sono, classificazione, struttura, funzioniÈ stata anche osservata la formazione di questi legami tra carboidrati e idrossilisina e idrossilisina e il gruppo fenolico di rifiuti di tirosina.
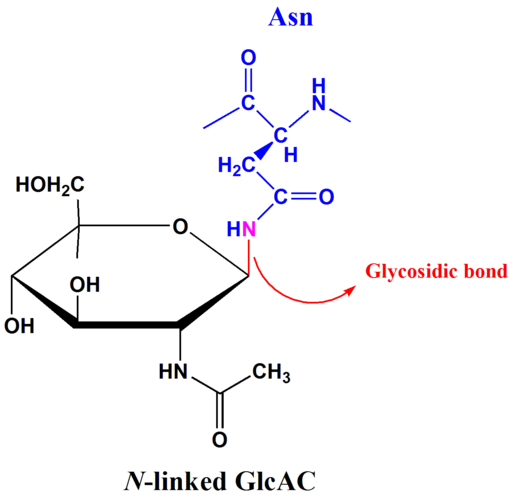
Collegamenti N-glucosidici
I collegamenti N-glycosidic sono i più comuni tra le proteine glicosilate. La n-glicosilazione si verifica principalmente nel reticolo endoplasmatico degli eucarioti, con successive modifiche che possono verificarsi nel complesso del Golgi.
 Esempio di collegamento N-glucosidico (fonte: Tpirojsi [dominio pubblico], via Wikimedia Commons)
Esempio di collegamento N-glucosidico (fonte: Tpirojsi [dominio pubblico], via Wikimedia Commons) La glicosilazione N dipende dalla presenza della sequenza di consenso Series/Thr ASN-XXX. Il legame glicosidico si verifica tra l'azoto in mezzo alla catena laterale di asparagina e carbonio anomerico di zucchero che si lega alla catena peptidica.
La formazione di questi legami durante la glicosilazione dipende da un enzima noto come oligosacariltransferasi, che trasferisce gli oligosaccaridi da un fosfato in dolorlo all'azoto di asparagina.
Altri tipi di collegamenti glucosidici
Collegamenti S-glucosidici
Si verificano anche tra proteine e carboidrati, sono stati osservati tra peptidi con cisteine N-terminali e oligosaccaridi. I peptidi con questo tipo di collegamenti sono stati inizialmente isolati dalle proteine nelle urine e dagli eritrociti umani legati agli oligosaccaridi del glucosio.
Collegamenti c-glucosidici
Sono stati osservati per la prima volta come modifica post -traduzionale (glicosilazione) in un residuo di triptofano in rnasa 2 presente nelle urine umane e nell'eritrocita 2. Una mano si lega al carbonio dalla posizione 2 del nucleo aminoacido mediante un legame c-glucosidico.
Nomenclatura
Il termine glicoside viene utilizzato per descrivere qualsiasi zucchero il cui gruppo anomerico è sostituito da un gruppo -o (o -glicosidi), -sr (tioglicosidi), -ser (selenoglucosidi), -nr (n -glicosidi o glucosamine) o anche -cr (C-glucosidi).
Possono essere nominati in tre modi diversi:
(1) Sostituzione del terminale "-o" del nome della forma ciclica corrispondente del monosaccaride per "-ido" e scrivere prima, come una parola diversa, il nome del gruppo di sostituzione R.
(2) Usando il termine "glicosiloxi" come prefisso del nome del monosaccaride.
(3) Usando il termine O-Glycosil, N-Glycosil, S-glicosil o C-Glicosil come prefisso per il nome del composto idrossilato.
Riferimenti
- Nelson, d. L., & Cox, m. M. (2009). Principi di biochimica Lechinger. Omega Editions (5 ° ed.).
- Nomenclatura dei carboidrati (Raccomandazioni 1996). (millenovecentonovantasei). Estratto da www.Qmul.AC.UK
- « Branchiopoda cosa sono, caratteristiche, riproduzione, cibo
- Deserto del Pacifico Cosa sono, caratteristiche, clima, flora, fauna »

