Concetto di elettroliti deboli, caratteristiche, esempi
- 1968
- 608
- Rosolino Santoro
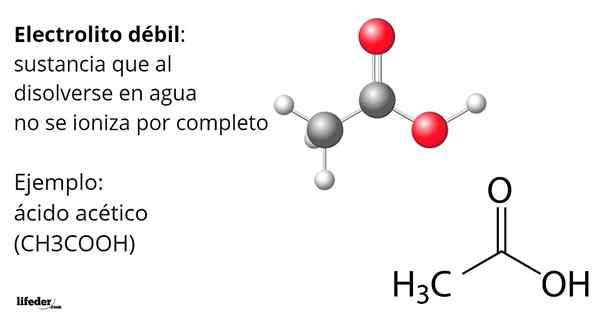
UN Elettrolita debole È tutta quella sostanza che si dissolve nell'acqua non è completamente ionizzata. Ciò significa che la sua dissoluzione produce o rilascia quantità di ioni inferiori di quanto ci si potrebbe aspettare. Questo processo di ionizzazione è stabilito da un equilibrio di idrolisi, in cui si formano ioni come H3O+ o oh-.
Gli elettroliti deboli sono generalmente composti covalenti, le cui molecole tendono a rimanere neutri senza acquisire carichi ionici. Molti di questi elettroliti sono costituiti da molecole organiche con gruppi funzionali ionizzabili, sebbene vi siano anche tipi inorganici, inclusi diversi ossacidi.

Acido acetico, Cho3COOH, è un esempio di un elettrolita debole. La sua molecola ha un gruppo funzionale che caratterizza la sua acidità in acqua. Tuttavia, quando non tutte le sue molecole sono disciolte di prodotti H3O+ Trasformare in acetato anione, Cho3COO-, ma rimangono neutrali, protonati.
Alcuni elettroliti sono più deboli di altri, il che dipenderà dal grado delle loro ionizzazioni. Quando si dissolvono, causano moderati cambiamenti nel pH. Pertanto, abbiamo elettroliti deboli acidi o di base.
[TOC]
Caratteristiche di elettoliti deboli
Sono composti covalenti
In termini generali, gli elettroliti deboli sono composti covalenti, quindi le loro unità costituenti sono molecole.
Soffrono idrolisi
Queste molecole hanno la capacità di acquisire carichi ionici. Per fare ciò, partecipare a un equilibrio di idrolisi, in cui una molecola d'acqua è "parte" in OH-, o accetta un idrogeno per trasformarsi in H3O+.
Il meno probabile o instabile è l'idrolisi, minore è la quantità o le concentrazioni di ioni presenti nella dissoluzione di questi elettroliti.
Hanno una bassa conduttività
Le soluzioni di elettroliti deboli non sono così buoni conduttori di elettricità, rispetto a quelle di elettroliti forti. Ciò è proprio dovuto al suo numero più basso di ioni in soluzione, il che rende difficile passare gli elettroni attraverso l'acqua.
Può servirti: acido manganico o permanganicoEsempi di elettroliti deboli
 L'acido acetico dell'aceto di mela è l'esempio più rappresentativo di un elettrolitico debole. Fonte: pxhere.
L'acido acetico dell'aceto di mela è l'esempio più rappresentativo di un elettrolitico debole. Fonte: pxhere. Acido carbonico
La molecola di acido carbonico, h2Co3, Quando si dissolve in acqua, la seguente reazione di idrolisi subisce:
H2Co3 + H2O ⇌ HCO3- + H3O+
Il problema è che non tutto H2Co3 È ionizzato in HCO3-. Inoltre, h2Co3 Si sproporge in anidride carbonica e acqua, che riduce ulteriormente la conduttività di questa soluzione.
Per i restanti esempi, questo fatto sarà recuperare: una molecola, che in linea di principio è neutro, acquisisce il carico ionico e nel processo mediato dall'idrolisi ci sono ioni H3O+ o oh-.
AmonYoAC
La molecola di ammoniaca, NH3, Quando si dissolve in acqua, la seguente reazione di idrolisi subisce:
NH3 + H2O ⇌ nh4+ + OH-
Queste soluzioni ammoniaali sparano un odore acuto.
Questa volta abbiamo ioni oh-. L'ammoniaca è una base debole, mentre l'acido carbonico, un acido debole. Pertanto, gli acidi e le basi deboli sono classificati come elettroliti deboli, poiché sono parzialmente ionizzati senza rilasciare alte concentrazioni di heles h3O+ o oh-, rispettivamente.
AAcido FOSFOricco
Acido fosforico, h3Po4, È un esempio di oxoacide debole, che a sua volta è un elettrolita:
H3Po4+ H2O ⇌ h2Po4- + H3O+
L'acido fosforico è ancora in grado di subire altre due dissociazioni, una per ogni idrogeno acido (tre in totale). La concentrazione di H3O+ prodotto è più piccolo se rispetto a quello di un forte oxoacide, come l'acido nitrico, HNO3, che è un forte elettrolita. Più debole è l'elettrolita, meno acido o basilare sarà.
HydOGeno
Il fluoruro di idrogeno, HF, è un esempio di un composto covalente inorganico che, senza essere un oxoacido, è un elettrolita debole perché è un acido debole. Quando si dissolve in acqua, viene prodotto acido fluororico, che è parzialmente ionizzato:
Può servirti: idrossido di cobaltoHF+ H2O ⇌ f- + H3O+
Nonostante non sia un forte elettrolita, l'acido fluoruro è in grado di "mangiare" il vetro di materiali che sono comunemente usati per conservare soluzioni di acido.
Piridina
La piridina, c5H5N, è un'ammina idrolizzata per formare ioni oh-:
C5H5N + h2O ⇌ c5H5NH + + OH-
La piridina è più semplice dell'ammoniaca, quindi la sua ionizzazione sarà maggiore e, quindi, produrrà concentrazioni più grandi di ioni OH-.
AAcido di cianhYoDRICO
L'acido cianoidrico, HCN, è anche un altro esempio di acido e elettroliti deboli:
HCN + H2O ⇌ cn- + H3O+
Sali insolubili
Questo punto è controverso. Finora elettroliti deboli sono stati classificati come acidi o basi deboli, caratterizzati dalle loro ionizzazioni parziali. Tuttavia, i sali insolubili in acqua, che sono già ionizzati nei loro cristalli, sono stati considerati anche elettroliti deboli.
Quando si dissolve con difficoltà nell'acqua, la quantità di ioni che rilasciano in soluzione è piccola rispetto a quella dei sali solubili. In questo senso, i sali insolubili producono soluzioni meno conduttive, che le eclissa un po 'come elettroliti forti.
Per questo motivo, qui si presume che questi sali appartengano al gruppo di elettroliti deboli, anche quando si dissolvono genera ioni neutri e molecole neutre con gradi di ionizzazione.
Cloruro d'argento
Cloruro d'argento, AGCL, si dissolve in acqua per produrre ioni+ e cl-. Tuttavia, è un sale abbastanza insolubile. La quantità di ioni che vengono rilasciati è molto inferiore a quello che avrebbe se fosse totalmente solubile, come con il nitrato d'argento, Agno3, Un forte elettrolita.
Può servirti: fase dispersaCarbonato di calcio
Carbonato di calcio, caco3, È un sale insolubile che dissolvendo parzialmente produce ioni di Ca2+ e co32-. Questo sale, a differenza dell'AGCL, è di base, perché il CO32- è idrolizzato per generare ioni oh-.
Zinco solfato
Zinco solfato, zonso4, È parzialmente sciolto nell'acqua per produrre ioni Zn2+ E così42-.
Fluoruro di calcio
Fluoruro di calcio, CAF2, Naturalmente trovato come minerale di fluoriti, si dissolve solo nell'acqua per produrre ioni CA2+ e f-.
Ossido di magnesio
L'ossido di magnesio, MgO, è un composto ionico piuttosto insolubile in acqua. La piccola porzione che dissolve reagisce a trasformarsi nel corrispondente idrossido, MG (OH)2, che è il vero responsabile dell'apparizione degli ioni Mg2+ e oh-.
Pertanto, il MGO, nonostante sia ionico, non può essere classificato come un forte elettrolita, perché nell'acqua non rilascia ioni dei propri cristalli (MG2+ IO2-).
Riferimenti
- Whitten, Davis, Peck e Stanley. (2008). Chimica. (8 ° ed.). Apprendimento del Cengage.
- SHIVER & ATKINS. (2008). Chimica inorganica. (Quarta edizione). Mc Graw Hill.
- Chung & Chieh. (5 giugno 2019). Elettroliti. Chimica librettexts. Recuperato da: Chem.Librettexts.org
- Helmestine, Todd. (11 febbraio 2020). Definizione ed esempio di elettroliti deboli. Recuperato da: Thoughtco.com
- Danielle Reid. (2020). Elettrolita debole: definizione ed esempio. Studio. Recuperato da: studio.com
- « Background gironondinos, chi siete tu e leader
- Caratteristiche triangoli obliqua, esempi, esercizi »

