Discovery, struttura, proprietà, proprietà di Darmstadtio

- 1432
- 7
- Dante Morelli
Lui Darmstadtio È un elemento chimico ultra pesante situato nella serie Transactinid, che inizia subito dopo il Lawrencio Metal. È specificamente nel gruppo 10 e nel periodo 7 della tavola periodica, essendo congeneri dei metalli di nichel, paladio e platino.
Ha un simbolo chimico, con un numero atomico di 110, e i suoi pochissimi atomi che si sono sintetizzati sono praticamente decomposti all'istante. È quindi un elemento effimero. Sintetizzare e rilevare rappresentava un'impresa negli anni '90 del secolo scorso, prendendo il merito della sua scoperta un gruppo di ricercatori tedeschi.
 L'elemento Darmstadtio è stato scoperto presso l'Istituto tedesco GSI, nella città di Darmstadt. Fonte: Commander-Pirx presso tedesco Wikipedia [CC BY-S (https: // creativeCommons.Org/licenze/by-sa/3.0)]
L'elemento Darmstadtio è stato scoperto presso l'Istituto tedesco GSI, nella città di Darmstadt. Fonte: Commander-Pirx presso tedesco Wikipedia [CC BY-S (https: // creativeCommons.Org/licenze/by-sa/3.0)] Prima della sua scoperta e che è stato discusso di quale dovrebbe essere il suo nome, il sistema di nomenclatura IUPAC aveva formalmente chiamato "Unaunilio", che significa "one-zero", pari a 110. E più dietro questa nomenclatura, secondo il sistema Mendeleev, il suo nome era Eka-Platino per aver pensato chimicamente a questo metallo.
Darmstadtio è un elemento non solo effimero e instabile, ma anche altamente radioattivo, nel cui nucleare decade la maggior parte dei suoi isotopi rilascia particelle di alfas; Questi sono, nuclei nudi elio.
A causa della sua fugace vita, tutte le sue proprietà sono stimate e non possono mai essere usate per uno scopo particolare.
[TOC]
Scoperta
Merito tedesco
Il problema attorno alla scoperta di Darmstadtio era che diversi team di ricercatori si erano dedicati alla loro sintesi negli anni successivi. Non appena si è formato il suo atomo, è sbiadito in particelle irradiate.
Pertanto, non poteva tentare quale dei team meritasse il merito di essersi sintetizzato per primo, quando anche rilevandolo rappresentava già una sfida, diminuendo così velocemente e rilasciando prodotti radioattivi.
Può servirti: acido tanico: struttura, proprietà, ottenimento, usiNella sintesi di Darmstadtio hanno lavorato da squadre separate dai seguenti centri investigativi: Central Institute of Nuclear Research a Dubná (a quel punto dell'Unione Sovietica), Lawrence Berkeley National Laboratory (Stati Uniti) e Abbreviato in tedesco come GSI come GSI ).
Il GSI si trova nella città tedesca di Darmstadt, dove nel novembre 1994 hanno sintetizzato l'isotopo radioattivo 269Ds. Le altre squadre hanno sintetizzato altri isotopi: 267Ds in icina, e 273Ds in lnlb; Tuttavia, i suoi risultati non erano stati conclusivi negli occhi critici dell'IUPAC.
Ogni squadra aveva proposto un nome particolare per questo nuovo elemento: Hahnio (icina) e Bequerelio (LNLB). Ma dopo un rapporto IUPAC nel 2001, il team GSI tedesco aveva il diritto di nominare l'elemento come Darmstadtio.
Sintesi
Darmstadtio è un prodotto della fusione di atomi di metallo. Quale? In linea di principio, relativamente pesante che funge da bianco o bersaglio, e un'altra luce che verrà scontrata contro la prima a una velocità pari al decimo della velocità della luce nel vuoto; Altrimenti, le repulsioni tra i suoi due nuclei non potrebbero essere superate.
Una volta che i due nuclei si scontrano in modo efficiente, si verificherà una reazione di fusione nucleare. I protoni si uniscono, ma il destino dei neutroni è diverso. Ad esempio, la GSI ha sviluppato la seguente reazione nucleare, di cui si è verificato il primo atomo 269DS:
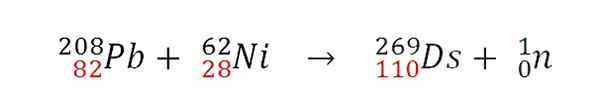 Reazione nucleare per la sintesi di un atomo di isotopo 269DS. Fonte: Gabriel Bolívar.
Reazione nucleare per la sintesi di un atomo di isotopo 269DS. Fonte: Gabriel Bolívar. Si noti che vengono aggiunti i protoni (in rosso). Varie le masse atomiche degli atomi sconfitti, si ottengono diversi isotopi di darmstadtio. In effetti, il GSI ha fatto esperimenti con l'isotopo 64Né invece di 62Né di coloro che hanno sintetizzato solo 9 atomi dell'isotopo 271Ds.
Può servirti: aldeideIl GSI è riuscito a creare 3 atomi di 269DS, ma dopo aver eseguito tre trilioni di bombardamenti al secondo per un'intera settimana. Questi dati offrono una prospettiva schiacciante delle dimensioni di tali esperimenti.
Struttura di Darmstadtio
Poiché solo un atomo di Darmstadtio a settimana può essere sintetizzato o creato, è improbabile che abbiano abbastanza per stabilire un cristallo; Per non parlare del fatto che l'isotopo più stabile è il 281Ds, di chi T1/2 Sono solo 12,7 secondi.
Pertanto, per determinare la loro struttura cristallina, i ricercatori si basano su calcoli e stime che cercano di affrontare il panorama più reale. Pertanto, è stato stimato che la struttura del darmstadtio è centrata cubica sul corpo (BCC); A differenza di quelli dei loro congeneri più leggeri di nichel, paladio e platino, con strutture cubiche centrate sui volti (FCC).
In teoria, gli elettroni più esterni degli Orbitali 6D e 7S devono partecipare al loro collegamento metallico, secondo la loro configurazione elettronica stimata:
[RN] 5f146d87s2
Tuttavia, probabilmente è noto sperimentalmente dalle proprietà fisiche di questo metallo.
Proprietà

Sono inoltre stimate le altre proprietà di Darmstadtio, per le stesse ragioni menzionate per la sua struttura. Tuttavia, alcune di queste stime sono interessanti. Ad esempio, Darmstadtio sarebbe un metallo ancora più nobile dell'oro, oltre a molto denso (34,8 g/cm3) che l'osmio (22,59 g/cm3) ed El Mercurio (13,6 g/cm3).
Per quanto riguarda i suoi possibili stati di ossidazione, è stato stimato che sarebbe +6 (DS6+), +4 (DS4+) e +2 (ds2+), uguale a quelli dei loro coetanei più leggeri. Pertanto, se gli atomi di 281DS prima che si disintegrano, sarebbero stati ottenuti composti come DSF6 o dscl4.
Può servirti: 50 esempi di acidi e basiSorprendentemente, c'è la probabilità di sintetizzare questi composti, perché 12,7 secondi, il T1/2 del 281DS, è più che sufficiente per fare reazioni. Tuttavia, l'inconveniente continua ad essere che con solo un atomo di DS a settimana non è sufficiente raccogliere tutti i dati richiesti da un'analisi statistica.
Applicazioni
Ancora una volta, poiché è un metallo così scarso, attualmente sintetizzato in quantità atomiche e non enormi, non c'è alcuna utilità riservata per lui; Nemmeno nel lontano futuro.
A meno che un metodo per stabilizzare i suoi isotopi radioattivi, gli atomi di Darmstadtio saranno usati solo per suscitare curiosità scientifica, soprattutto per quanto riguarda la fisica e la chimica nucleare.
Ma se viene gestito un modo per crearli in quantità abbondanti, verranno lanciate più luci sulla chimica di questo elemento ultra pesante ed effimero.
Riferimenti
- SHIVER & ATKINS. (2008). Chimica inorganica. (Quarta edizione). Mc Graw Hill.
- Wikipedia. (2020). Darmstadium. Recuperato da: in.Wikipedia.org
- Steve Gagnon. (S.F.). L'elemento Darmstadium. Risorsa di Jefferson Lab. Recuperato da: istruzione.Jlab.org
- Centro nazionale per le informazioni sulla biotecnologia. (2020). Darmstadium. Database PubChem. Recuperato da: pubchem.NCBI.Nlm.NIH.Gov
- Brian Clegg. (15 dicembre 2019). Darmstadium. Chimica nei suoi elementi. Recuperato da: Chemistryworld.com
- « Concetto del numero di ossidazione, come tirarlo fuori ed esempi
- Massa molare come viene calcolato, esempi ed esercizi risolti »

