Costanti di formule Antoine, equazioni, esempi
- 5138
- 528
- Lidia Valentini
IL costanti di Antoine Esistono tre parametri che appaiono in una relazione empirica tra pressione del vapore di saturazione e temperatura per sostanze pure. Dipendono da ogni sostanza e dovrebbero essere costanti in una certa gamma di temperature.
Da quell'intervallo le costanti di Antoine cambiano il loro valore. Le costanti sono correlate attraverso un'equazione creata nel 1888 dall'ingegnere francese Louis Charles Antoine (1825-1897).
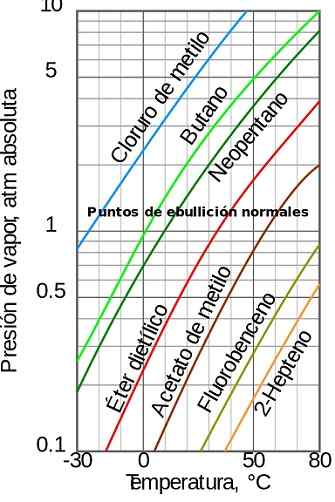
 Figura 1. Pressione del vapore a seconda della temperatura. Fonte: Wikimedia Commons
Figura 1. Pressione del vapore a seconda della temperatura. Fonte: Wikimedia Commons [TOC]
Formule ed equazioni
Il modo più normale di esprimere la funzione di Antoine è:

In questa formula P rappresenta la pressione del vapore di saturazione espressa nei millimetri di mercurio (MMHG), T è la temperatura che è la variabile indipendente ed è espressa in ℃.
A, B e C sono le costanti o i parametri della formula Antoine.
L'importanza di questa formula che nonostante sia empirica, fornisce una semplice espressione analitica che può essere facilmente utilizzata nei calcoli termodinamici.
La formula di Antoine non è unica, ci sono espressioni più precise che sono estensioni di questa formula, ma con lo svantaggio che hanno sei o più parametri e la loro espressione matematica è più complessa, il che le rende molto pratiche da utilizzare nei calcoli termodinamici.
Vapore di saturazione
Poiché la formula di Antoine misura la pressione del vapore di saturazione, è necessario spiegare cosa consiste.
In un'ampoule di vetro o un altro contenitore viene posizionato un liquido. Tutta l'aria aerea viene estratta. Il set viene posto in un bagno termico fino a raggiungere l'equilibrio.
All'inizio tutto è liquido, ma poiché c'è un vuoto, le molecole più veloci iniziano ad abbandonare il liquido che forma un gas della stessa sostanza del liquido.
Può servirti: movimento rettilineo uniforme: caratteristiche, formule, eserciziIl processo precedente è il evaporazione E mentre la pressione del vapore sta aumentando.
Alcune delle molecole di vapore perdono energia e tornano alla fase liquida della sostanza, questo è il processo di condensazione.
Quindi si verificano due processi, evaporazione e condensa. Quando lo stesso numero di molecole liquide che sono incorporate in esso vengono fuori, a equilibrio dinamico E in questo momento si verifica la massima pressione del vapore nota come pressione di saturazione.
È questa pressione di saturazione del vapore che prevede la formula antoina per ciascuna sostanza e ogni temperatura.
In alcuni solidi c'è un fenomeno simile quando passa dalla fase solida direttamente alla soda senza passare attraverso la fase liquida, in questi casi può anche essere misurata una pressione di vapore di saturazione.
Non è facile stabilire un modello teorico a partire dai primi principi poiché sono coinvolti cambiamenti nell'energia cinetica molecolare, che possono essere di tipo traslazionale, rotazionale e vibrazionale, con l'energia del legame molecolare interno. È per questo motivo che in pratica vengono utilizzate formule empiriche.
Come sono la costante di Antoine?
Non esiste un metodo teorico per ottenere le costanti di Antoine, perché è una relazione empirica.
Sono ottenuti dai dati sperimentali di ciascuna sostanza e regolando i tre parametri A, B e C, in modo che minimizzino la differenza quadratica (metodo dei minimi quadrati) della previsione con i dati sperimentali.
Per l'utente finale, che sono generalmente ingegneri chimici, ci sono tabelle nei manuali di chimica in cui queste costanti sono riportate per ciascuna sostanza che indicano le fasce di temperatura massima e minima in cui sono applicabili.
Può servirti: termometro di resistenza: caratteristiche, funzionamento, usiSono inoltre disponibili servizi online che forniscono i valori delle costanti A, B e C come nel caso di DDBST GmbH OnLines Services.
Per la stessa sostanza può esserci più di una gamma di temperature di validità. Quindi a seconda del raggio di lavoro, viene scelto uno o un altro gruppo di costanti.
Le difficoltà possono apparire se l'intervallo di lavoro di temperatura è tra due intervalli di validità delle costanti, poiché le previsioni della pressione della formula non coincidono nella zona borderline.
Esempi
Esempio 1
Trova la pressione del vapore acqueo a 25 ℃.
Soluzione
Abbiamo consultato le tabelle per determinare le costanti di Antoine.
Ci sono due gamme d'acqua:
Tra 1 ℃ e 100 ℃ e tra 99 ℃ a 374 ℃.
Dato che siamo interessati a 25 ℃ prendiamo il primo intervallo in cui sono il valore delle costanti di Antoine:
A = 8.07131
B = 1730.63
C = 233.426
P = 10^(8.07131 - 1730.63/(25 + 233.426))
Calcolo dell'esponente
Calcoliamo prima l'esponente: 1.374499
P = 10^1.374499 = 23.686 mmHg = 0,031166 atm
Analisi dei risultati
Questi risultati sono interpretati come segue:
Supponiamo che l'acqua pura sia posizionata in un contenitore ermetico a cui l'aria è stata estratta da una pompa a vuoto.
Il contenitore con acqua viene posizionato in un bagno termico ad una temperatura di 25 ℃ fino a raggiungere l'equilibrio termico.
L'acqua nel contenitore ermetico evapora parzialmente fino a raggiungere la pressione del vapore di saturazione, che non è altro che la pressione in cui viene stabilita l'equilibrio dinamico tra la fase liquida dell'acqua e la fase del vapore.
Può servirti: Modello atomico di Dirac Jordan: caratteristiche e postulatiQuella pressione in questo caso si è rivelata 0,031166 atm a 25 ℃.
Esempio 2
Trova la pressione del vapore acqueo a 100 ℃.
Soluzione
Abbiamo consultato le tabelle per determinare le costanti di Antoine. Ci sono due gamme d'acqua:
Tra 1 ℃ e 100 ℃ e tra 99 ℃ a 374 ℃.
In questo caso la temperatura di interesse è nelle due gamme.
Usiamo il primo degli intervalli [1 ℃, 100 ℃]
A = 8.07131
B = 1730.63
C = 233.426
P = 10^(8.07131 - 1730.63/(100 + 233.426))
Calcolo dell'esponente
Calcoliamo prima l'esponente: 2.8808
P = 10^1.374499 = 760,09 mmHg = 1.0001 ATM
Successivamente usiamo il secondo degli intervalli [99 ℃, 374 ℃]
In questo caso le costanti sono
A = 8.14019
B = 1810.94
C = 244.485
P = 10^(8.14019 - 1810.94/(100 + 244.485))
Calcoliamo prima l'esponente: 2.88324
P = 10^2.88324 = 764.2602 mmHg = 1.0056 atm
C'è una differenza percentuale tra i due risultati dello 0,55%.
Riferimenti
- Applicazione delle leggi di Raoult e Dalton e dell'equazione Antoine. Estratto da: il mio e il mio antico.WordPress.com
- Calcolatore online della formula Antoine. Recuperato da: ddbonline.Ddbst.di/antOineCalcion/Antoinecalculaticgi.exe
- Gecousb. Termodinamica e tavoli a vapore / costante da Antoine. Recuperato da: Gecousb.com.andare
- Proprietà termiche della materia. Recuperato da: server web.DMT.Upm.È
- Suddici e Yang. Tabelle costanti Antoine per più di 700 composti organici. Recuperato da: utente.Eng.UMD.Edu
- Wikipedia. Equazione Antoine. Recuperato da Wikipedia.com
- Wikipedia. Equazione di Clausius-Clapeyron. Recuperato da Wikipedia.com
- Wisniak J. Sviluppo storico dell'equazione della pressione a vapore da Dalton Toy Antoine. Recuperato da: link.Springer.com
- « Calcolo della densità relativa, esempi, esercizi
- Equazioni del diagramma Moody, a cosa serve, applicazioni »

