Acido solforoso
- 2802
- 16
- Dott. Rodolfo Gatti
 L'acido solforoso è un acido minerale che si verifica quando il biossido di zolfo si dissolve in acqua
L'acido solforoso è un acido minerale che si verifica quando il biossido di zolfo si dissolve in acqua Cos'è l'acido solforoso?
Lui Acido solforoso È un oxácido che si forma quando il biossido di zolfo, quindi2, Si dissolve in acqua. È un acido inorganico debole e instabile, che non può essere rilevato in soluzione, poiché la reazione della sua formazione è reversibile e l'acido si decompone rapidamente nei reagenti che l'hanno prodotta (così2 e h₂o).
È un liquido incolore, con un forte odore di zolfo, instabile e viene utilizzato in vari campi industriali, come materiali colorati di cloro, per la sintesi di prodotti medicinali e chimici, per la produzione di carta o per affinare i derivati del petrolio.
La molecola di acido zolfo al momento è stata rilevata solo nella fase gassosa. Le basi coniugate di questo acido sono anioni comuni sotto le forme di solfiti e bisolfito.
Lo spettro di Raman di SO soluzioni2 Mostra solo segni dovuti alla molecola così2 e ioni bisolfito, HSO3-, Coerentemente con il seguente saldo:
SW2 + H₂o hso3- + H+
Ciò indica che dallo spettro di Raman non è possibile.
Se esposto all'atmosfera, viene rapidamente trasformato in acido solforico. L'acido solforoso è ridotto all'idrogeno solforato a causa dell'azione di acido solforico diluito e zinco.
Il tentativo di concentrare una soluzione SO2 Per evaporazione dell'acqua per ottenere acido zolfo libero d'acqua, non ha prodotto un risultato, poiché l'acido si decompone rapidamente (investendo la reazione di formazione), quindi l'acido non può essere isolato.
Struttura di Acido solforoso
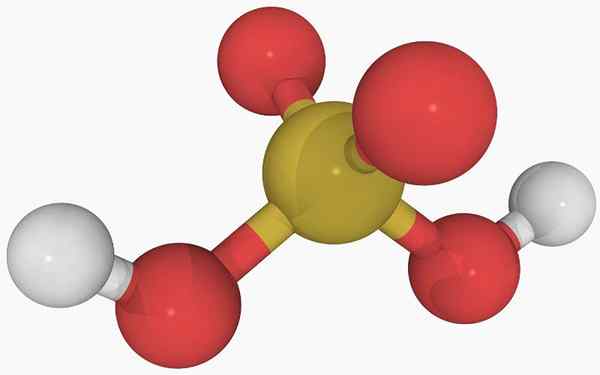
 Struttura chimica dell'acido solforoso
Struttura chimica dell'acido solforoso Nell'immagine principale si può vedere la struttura di una molecola isolata di acido solforoso in uno stato gassoso. La sfera gialla al centro corrisponde all'atomo di zolfo, ai rossi per gli atomi di ossigeno e da bianco agli idrogeni.
Può servirti: diastreomerLa sua geometria molecolare attorno all'atomo S è la piramide trigonale, con gli atomi di o disegnare la base.
Quindi, nello stato gassoso, le molecole H2SW3 Possono essere considerati come piramidi trigonali microscopiche che galleggiano nell'aria, supponendo che siano abbastanza stabili da durare un po 'di tempo senza reagire.
La struttura chiarisce da dove provengono i due idrogeni acidi: dai gruppi idrossilici legati allo zolfo, HO-OH-OH. Pertanto, per questo composto, non è corretto supporre che uno dei protoni acidi, h+, viene rilasciato dall'atomo di zolfo, H-So2(OH).
I due gruppi OH consentono all'acido dello zolfo di interagire usando ponti idrogeno e anche l'ossigeno del legame S = O è un accettore di idrogeno, il che rende h2SW3 Sia in un buon donatore e accettore di questi ponti.
Secondo quanto sopra, h2SW3 Dovrei essere in grado di condensare in un liquido, come fa l'acido solforico, h2SW4. Tuttavia, non è così.
Proprietà fisiche e chimiche del Acido solforoso
Formula molecolare
H2SW3
Peso molecolare
82.073 g/mol.
Aspetto fisico
È un liquido incolore, con un odore di zolfo piccante.
Densità
1.03 g/ml.
Densità del vapore
2.3 (in relazione all'aria presa come 1)
Corrosività
È corrosivo per metalli e tessuti.
Solubilità dell'acqua
Mistibile.
Sensibilità
È sensibile all'aria.
Stabilità
Stabile, ma incompatibile con basi forti.
Costante di acidità (ka)
1.54 x 10-2
PKA
1.81
ph
1.5 sulla scala del pH.
punto di accensione
Non infiammabile.
Decomposizione
Quando riscaldato, l'acido dello zolfo può essere scomposto, emettendo un fumo tossico di ossido di zolfo.
Può servirti: idrossido di cromo: struttura, proprietà, sintesi, usiNomenclatura
Lo zolfo ha le seguenti valenze: ± 2, +4 e +6. Dalla formula h2SW3, Può essere calcolato quale valenza o numero di ossidazione ha zolfo nel composto. Per fare questo, è sufficiente risolvere una somma algebrica:
2 (+1) + 1V + 3 (-2) = 0
Poiché è un composto neutro, la somma dei carichi degli atomi che lo costituisce deve essere 0. Clearing V per l'equazione precedente, hai:
V = (6-2)/1
Pertanto, V è uguale a +4. Cioè, lo zolfo partecipa al suo secondo Valencia e, secondo la tradizionale nomenclatura, il suffisso deve essere aggiunto al nome -ooso. Per questo motivo, a H2SW3 È noto come acido zolfoorso.
Un altro modo più veloce per determinare questo Valencia è confrontare H2SW3 con h2SW4.
In h2SW4 Lo zolfo ha Valencia +6, quindi se una o, Valencia scende a +4, e se un altro viene rimosso, Valencia scende a +2 (che sarebbe il caso dell'acido singhiozzoZolfoorso, H2SW2).
Sebbene meno noto, a h2SW3 Può anche essere chiamato acido trioxosulfurico (IV), secondo la nomenclatura azionaria.
Formazione di acido solforoso in natura
L'acido solforoso si forma in natura a causa della combinazione di anidride solforosa, prodotto dell'attività di grandi fabbriche, con acqua atmosferica.
Per questo motivo, è considerato un prodotto intermedio della pioggia acida, causando gravi danni all'agricoltura e all'ambiente.
Sintesi
Tecnicamente, lo zolfo è formato per formare il biossido di zolfo. Quindi, si dissolve in acqua per formare acido zolfo. Tuttavia, la reazione è reversibile e l'acido si rompe rapidamente nei reagenti.
Questa è una spiegazione del perché l'acido zolfo non si trova in soluzione acquosa (come già menzionato nella sezione della sua struttura chimica).
Può servirti: legge della birra-lambeApplicazioni
Generalmente, gli usi e le applicazioni dell'acido solforoso, poiché la sua presenza non può essere rilevata, si riferiscono agli usi e alle applicazioni degli anidrici di zolfo e alla base e ai sali di acido.
In legno
Nel processo solfito, si verifica una polpa di legno sotto forma di fibre di cellulosa quasi pura. Diversi sali di acido di zolfo vengono utilizzati per l'estrazione di lignina dalle schegge di legno, usando contenitori ad alta pressione chiamati digester.
Agente disinfettante
L'acido solforoso viene usato come disinfettante.
Candeggina
Viene anche usato come sbiancamento morbido, specialmente per i materiali sensibili al cloro. Inoltre, viene utilizzato come candeggina dentale e additivo alimentare.
Cosmetici
È un ingrediente di vari cosmetici per la cura della pelle ed è stato usato come elemento di pesticidi nell'eliminazione dei ratti. Elimina le macchie causate da vino o frutta su tessuti diversi.
Antisettico
Funge da antisettico, essendo efficace per evitare le infezioni della pelle. In alcuni momenti, è stato usato nelle fumigazioni per disinfettare le navi, gli effetti personali delle vittime di epidemie, ecc.
Agente conservante
L'acido zolfo viene usato come conservante di frutta e verdura e per evitare la fermentazione di bevande come vino e birra, essendo un elemento antiossidante, antibatterico e fungicida.
Prodotti chimici
L'acido solforoso viene utilizzato nella sintesi di farmaci e sostanze chimiche, nell'elaborazione del vino e della birra, nel raffinatezza dei prodotti derivati dall'olio e come reagente analitico.
Riferimenti
- Nomenclatura di acidi. Recuperato da 2.Chimica.Gatech.Edu
- Calvo Flores, F. G. Formulazione di chimica inorganica. Ugr recuperato.È

