Struttura dell'acido solfanilico, proprietà, sintesi, usi
- 995
- 16
- Ruth Cattaneo
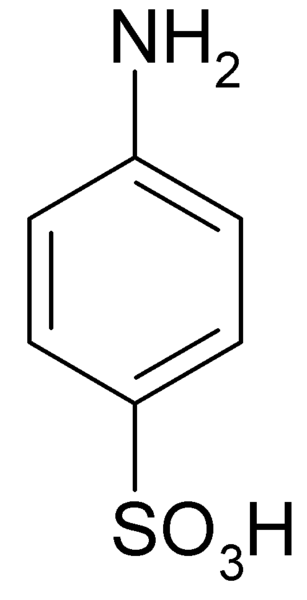
Lui Acido solfanilico È un composto cristallino la cui molecola è formata da un anello di benzene a cui un gruppo di base è contemporaneamente unito (-nh2) e un gruppo acido (-so3H). La sua formula chimica è NH2C6H4SW3H.
È anche noto come acido 4-aminobenosolfonico. È preparato mediante solfonazione di anilina nella posizione per. I suoi cristalli sono bianchi o in grove bianchi. Il suo comportamento è più simile a quello di un sale di quello di un composto organico con gruppi NH2 orso3H. Pertanto, è insolubile nella maggior parte dei solventi organici.
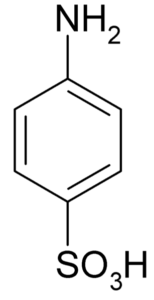 Formula molecolare di acido solfanilico o acido 4-aminobenzeulfonico. Klaus Hoffmeier [dominio pubblico]. Fonte: Wikipedia come noi
Formula molecolare di acido solfanilico o acido 4-aminobenzeulfonico. Klaus Hoffmeier [dominio pubblico]. Fonte: Wikipedia come noi Uno dei suoi usi principali è nella sintesi dei coloranti, in quanto forma facilmente un diazocopato che è materia prima per tale applicazione.
Sia il sulfanil acido che i suoi derivati sono stati usati come agenti antibatterici. È usato nella sintesi di composti mucolitici, poiché hanno la capacità di ridurre la viscosità del muco o dei fluidi biologici molto viscosi.
Viene anche utilizzato nel settore della carta e nelle formule per incisioni o litografie. Fa parte delle resine che vengono utilizzate in miscele in cemento o mortai per consentire loro di mantenere la loro fluidità per molto tempo, senza influenzare il tempo di impostazione finale.
È un metabolita xenobiotico, ciò significa che non è naturalmente prodotto dagli esseri viventi. È una pelle, gli occhi e la mucosa irritanti. Inoltre, puoi contaminare l'ambiente.
[TOC]
Struttura
L'acido solfanilico ha cristalli bianchi formati da fogli ortorrombici o monoclinici. Il suo monoidrato si cristallizza in acqua sotto forma di fogli ortorombici. Se la cristallizzazione viene eseguita molto lentamente, cristallizza diidrato. Il monoidrato diventa anidro quando è di circa 100 ºC.
Nomenclatura
- Acido solfanilico.
- Acido p-amynobenosolfonico.
- Acido 4-amybonzefonic.
Proprietà
Stato fisico
Solido cristallino bianco o bianco.
Peso molecolare
173,19 g/mol.
Punto di fusione
Si rompe a circa 288 ºC senza sciogliere. È anche segnalato a> 320 ºC.
Densità
1,49 g/cm3
Solubilità
Quasi insolubile in acqua: 10,68 g/L a 20 ºC.
Insolubile in etanolo, benzene ed etere. Leggermente solubile in metanolo caldo.
Solubili in soluzioni di base acquose. Insolubile in soluzioni acquose di acido minerale. Solubile in acido cloridrico concentrato.
Proprietà chimiche
Le sue proprietà differiscono da quelle di altri composti ammina o solfonati, essendo simili a quelle di un sale. Questo perché la sua struttura contiene i gruppi -nh3+ E così3-, Ciò che gli dà le caratteristiche degli ioni dipolo.
Può servirti: soluzione supersaturataContiene un gruppo acido e un gruppo di base in poli opposti della stessa molecola. Ma lo ione idrogeno è collegato all'azoto anziché all'ossigeno perché il gruppo -NH2 È una base più forte del gruppo -so3-.
Perché è uno ione dipolo presenta un punto più alto di fusione e insolubilità nei solventi organici.
L'acido solfanilico è solubile in soluzione alcalina perché ioni idrossido OH-, Essendo fortemente semplice, inizia uno ione idrogeno (h+) del gruppo di base debole -nh2, Formare lo ione p-aminobenosulfonato, che è solubile in acqua.
In soluzione acida la struttura dell'acido sulfanil non cambia, quindi rimane insolubile.
Altre proprietà
Quando riscaldato alla sua decomposizione emette vapori tossici di azoto e ossidi di zolfo.
L'esposizione all'acido sulfanil può portare a sintomi come irritazione della pelle, occhi e mucose. È un composto corrosivo.
Sintesi
Viene preparato reagendo l'anilina con acido solforico (h2SW4) ad alte temperature. Inizialmente, si forma il sale di solfato di acido aniliniano, che quando si riscaldano a 180-200 ºC viene riorganizzato per formare l'anello sostituito in posizione, perché è il prodotto più stabile.
Per prepararlo con un alto grado di purezza, viene eseguita la solfonazione di una miscela di anilina e solfolano2SW4 a 180-190 ºC.
Applicazioni
Nel settore da colorare
L'acido di sulfanil viene usato nella sintesi o nella preparazione di diversi coloranti, come metil arancione e tartrazina. Per questo è diazotizzato, generando acido diazotizzato di sulfanil.
È importante sottolineare che la tartrazina è stata usata come colorazione nel cibo. Ma una volta ingerito, genera alcuni metaboliti nell'organismo umano, incluso l'acido delfanil, che sono possibili responsabili della formazione di specie reattive dell'ossigeno. Questi possono colpire renali (reni) o tessuti epatici (fegato).
 Caramelli con colorante giallo. David Adam Kess [CC BY-SA 4.0 (https: // creativeCommons.Org/licenze/by-sa/4.0)]. Fonte: Wikipedia Commons
Caramelli con colorante giallo. David Adam Kess [CC BY-SA 4.0 (https: // creativeCommons.Org/licenze/by-sa/4.0)]. Fonte: Wikipedia Commons In chimica analitica
È usato come reagente nella determinazione di diversi composti chimici, compresi i nitriti.
In medicina come agente antibatterico
Il sulfanilammide, derivato dall'acido del sulfanil, ha l'applicazione nell'industria farmaceutica perché ha attività antibatterica.
Nel corpo umano i batteri lo confondono con l'acido p-aminobenzoico che è un metabolita essenziale. Questa sostituzione provoca la riproduzione dei batteri e muoiono.
Può servirti: idrogeno: storia, struttura, proprietà e usi Batterio. Immagine Raman Oza. Fonte: Pixabay
Batterio. Immagine Raman Oza. Fonte: Pixabay Un altro derivato dall'acido del sulfanil, ottenuto dalla condensa con altri composti, ha anche proprietà antibatteriche, che si basano sulla sua capacità di spostare l'acido folico (membro del complesso vitamina B).
Questo composto può essere preso per via orale, iniettato per via endovenosa o applicata esternamente in un unguento.
In medicina come agente mucolitico
È stato utilizzato un derivato dell'acido di sulfanil che ha attività mucolitica. Questo è che presenta l'attività del muco di LicueFattiva, per sciogliere il muco o i fluidi biologici molto viscosi.
Il composto può essere usato per produrre muco prodotto da un tessuto a causa di condizioni patologiche. Ad esempio la congestione del sistema respiratorio o quella del tratto vaginale, tra gli altri.
Quando si tratta di liquefazione del muco nel tratto respiratorio, il prodotto viene somministrato per inalazione, gocce nel naso, rugiada, aerosol o nebulizzatori. È un trattamento applicabile all'essere umano o ai mammiferi. È un composto più potente della cisteina.
 Applicazione di gocce nasali per il freddo. Immagine frenzel Thorsten. Fonte: Pixabay
Applicazione di gocce nasali per il freddo. Immagine frenzel Thorsten. Fonte: Pixabay Viene anche utilizzato in laboratorio quando si desidera ridurre la viscosità dei fluidi biologici per facilitare le determinazioni analitiche.
Nei laboratori di bioanalisi
L'acido diazotizzato sulfanil (un derivato che viene preparato reagendo sul solfanil acido con nitrito di sodio) viene utilizzato nella determinazione della bilirubina.
La bilirubina è un pigmento giallo che si trova in bile. L'eccesso di sangue di bilirubina è una conseguenza di malattie epatiche, disturbi ematologici (o sangue) o disturbi nel tratto biliare.
Per misurare la quantità di bilirubina nel sangue, viene reagida la dialisi derivata dall'acido di solfanil con bilirubina per formare il complesso di azobilirubin, il cui colore è misurato l'intensità con un colorimetro o uno spettrofotometro. In questo modo, il contenuto di bilirubina nel sangue è determinato nel sangue.
Nell'industria cartacea
L'acido solfanilico consente di sintetizzare una lucidatura della carta, ovvero un composto che fornisce luminosità ottica o aspetto bianco, poiché neutralizza il colore giallo della carta naturale o non tracciata.
 Taccuino white paper. Fonte: Pexels
Taccuino white paper. Fonte: Pexels Ha il vantaggio rispetto ad altri composti, poiché può essere utilizzato in concentrazioni relativamente elevate per trattare la polpa di carta in condizioni di pH basso, senza aumentare la carta giallo.
Può servirti: solfato di ammonioIl risultato viene evidenziato quando la carta si osserva con la luce UV (ultravioletta), in base al quale fluoro molto più di quando vengono utilizzati altri composti e con luce visibile si osserva che il grado di giallo è molto basso.
È molto solubile in acqua, permettendogli di utilizzare in soluzioni più concentrate. Può essere utilizzato in qualsiasi tipo di carta, inclusa la carta prodotta con polpa di legno macinata, polpa di solfito o qualsiasi altro processo.
In impressioni, incisioni o litografie
L'acido solfanilico funziona come un'acidificazione in soluzioni concentrate per la litografia, senza presentare i problemi di altri acidi come il fosforico, essere meno tossici e meno inquinanti rispetto a quest'ultimo.
Nei materiali da costruzione
Le soluzioni acquose di resina di melamina-formaldeide modificate con acido di solfanil sono state testate specificamente (calcestruzzo), mortaio o pasta di cemento. Lo scopo è stato quello di ridurre il contenuto dell'acqua e prevenire la diminuzione della fluidità della miscela con il passare del tempo, senza che il tempo di impostazione diminuisca.
Il calcestruzzo o il mortaio preparato con queste soluzioni è molto efficace in estate, quando la diminuzione della fluidità nel tempo costituisce un problema.
Con queste soluzioni, se il mortaio o il calcestruzzo sono preparati e per qualsiasi motivo deve essere permesso di riposare, la composizione del cemento può essere facilmente scaricata in stampi o simili, poiché non ha perso la fluidità nel tempo.
 Scarico in cemento. Igor Image Ovsyannykov. Fonte: Pixabay
Scarico in cemento. Igor Image Ovsyannykov. Fonte: Pixabay Riferimenti
- Windholz, m. et al. (Redattori) (1983). L'indice Merck. Un'enciclopedia di sostanze chimiche, drarug e biologici. Decima edizione. Merck & co., INC.
- Kirk-Othmer (1994). Enciclopedia della tecnologia chimica. Volume 2. Quarta edizione. John Wiley & Sons.
- Biblioteca nazionale di medicina. (2019). Acido solfanilico. Recuperato da: pubchem.NCBI.Nlm.NIH.Gov
- Urist, h. e Martin, G.J. (1950). Derivati dell'acido solfanilico. Brevetto americano n. 2.504.471. Assegnatari alla National Drug Company. 18 aprile 1950.
- Villaume, Federico G. (1964). Composizione di cartoni luminosi per carta dercata dall'acido metanile e sulfanilico. Brevetto americano n. 3.132.106. 5 maggio 1964.
- Martin, Tellis a. e mangiare, William t. (1979). Derivato di acido benzoico e processo mucolitico dell'acido benzenolfonico. Brevetto americano n. 4.132.802. 2 gennaio 1979.
- Druker, l.J. e kincaid, r.B. (1979). Concentrata di fontane litografiche. Brevetto americano n. 4.150.996. 24 aprile 1979.
- Shull, Bruce C. (1983). Dosaggio di bilirubina. Brevetto americano n. 4.404.286. 13 settembre 1983.
- Uchida, j. et al. (2001). Processo per preparare una soluzione acquosa di resina di melamina-formaldeide modificata con acido solfanile e una composizione di cemento. Brevetto americano n. 6.214.965 B1. 10 aprile 2001.
- Corradini, m.G. (2019). Volume 1. In enciclopedia della chimica alimentare. Recuperato da ScienceDirect.com.

