Acido silícico
- 4460
- 492
- Baldassarre Ross
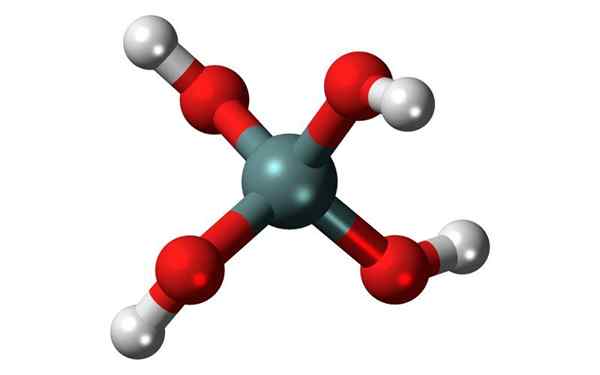
 Struttura chimica dell'acido ortosilico, il più comune della silicica. Fonte: Jynto, CC0, Wikimedia Commons
Struttura chimica dell'acido ortosilico, il più comune della silicica. Fonte: Jynto, CC0, Wikimedia Commons Cos'è l'acido silicico?
Lui Acido silícico È una forma idratata di ossido di silicio. È il nome generale per la famiglia di composti chimici formati dal silicio, attaccato a gruppi di ossido o idrossile.
La formula generale di questi acidi è [SIOX(OH)4-2x"N, E il modo più comune in cui si trova di solito è quello dell'acido ortosillico, h4Sio4.
L'acido silícico fa parte della famiglia di silati vari. Ciò significa che il più grande oxoanione metallico è silicato e che nessun atomo non metallico è unito.
Ci sono alcuni casi isolati in cui hanno un atomo non metallico, ma mai più di uno.
Proprietà fisiche dell'acido silícico
- L'acido silícico esiste solo in due stati, amorfo e cristallino. Il primo è ottenuto da un processo di precipitazione e il secondo è presentato come cristallo di roccia.
- Acido silícico, nella sua forma amorfa (SIO3), è bianco, insipido, insolubile in acqua e non si forma con molecole di se stesso qualsiasi massa coesiva di plastica, come con l'alluminio.
- Nel suo stato cristallino, non è sciolto da nessun oxacido. Quando una soluzione molto diluita di soluzione di silice viene trattata con acido solforico, nitrico o cloridrico, l'acido silicico non viene precipitato. Invece, sembra essere sciolto in acqua come un idrato.
- Quando una soluzione acida o acida viene aggiunta a una soluzione di silicato, l'idrato viene precipitato in una forma gelatina, che durante l'essiccazione e successivamente il riscaldamento con molta energia, diventa una sostanza insolubile.
Può servirti: acido zolfoReazioni chimiche
L'acido silícic è estremamente debole e perde il suo primo protone solo quando si avvicina a pH 10. Solo 3 reazioni con questo acido sono note nelle normali condizioni fisiologiche della vita.
- La reazione con se stessa, quando viene superata la solubilità per formare la silice idrata amorfa.
- La sua reazione con idrossido di alluminio per formare idrossido di silicato di alluminio.
- Reazione in eccesso di Molibdale per formare eteropoliehacidi, come il silicomolibdato.
Dov'è l'acido silicico?
Dopo l'ossigeno, il silicio è l'elemento più comune della natura. È sotto forma di cristalli. Quando è in ambiente acquoso diventa non -ionizzante, quindi sale di silicio in silicio.
Le forniture nette di acido silicico nell'oceano mondiale sono state trovate a 6,1 ± 2,0 Terramoli di silicio all'anno (1 Terramolo = 1012 moli). Quasi l'80% di questo contributo proviene dai fiumi, la cui concentrazione media mondiale è 150 micromolare (concentrazione di acqua).
Nei moderni sedimenti marini, le rese di silicio biogenico netto (trasformazione del silicato disciolto in materiale scheletrico in particelle) è 7.1 ± 1.8 teramoli all'anno.
La produzione di silice biogenica di Bruta nelle acque superficiali è di 240 ± 40 termoli di silicio all'anno e il rapporto di conservazione (accumulo di opali in sedimenti / produzione lordo nelle acque superficiali) è del 3%.
Nella flora, può essere trovato sulla pianta Borago officinalis (Borage), che nella sua composizione presenta fino al 2,2% di acido silicico.
Può servirti: acetato di sodio: struttura, proprietà, sintesi, usiL'acido ortosilico è la forma più comune di acido silicico, che può essere trovata in luoghi diversi. Le più grandi fonti biodisponibili di questo acido si trovano in acqua, sia in acqua di mare che in altre bevande, come la birra.
Per ottenere il laboratorio, lo stesso principio viene seguito come nell'oceano: può essere ottenuto dall'acidificazione del silicato di sodio in una soluzione acquosa.
Usi nella vita di tutti i giorni
Dentifricio
È il gel abrasivo usato nel dentifricio o nella parte chiara della pasta dentale Rayada, poiché in combinazione con carbonato di calcio, aiuta a rimuovere in sicurezza la piastra con la spazzolatura.
È registrato come un composto sicuro in Food & Drug Administration degli Stati Uniti e non ha tossicità o cancerogenicità nota.
Essiccante
Se asciugato in un forno, perde acqua e diventa un essiccante (sostanza che attira aria dall'aria). Pertanto, è possibile trovare piccoli pacchetti di cristalli di gel di silice in contenitori il cui contenuto può essere danneggiato dall'umidità, come bottiglie di vitamine, elettronica, scarpe o prodotti in pelle.
Altri usi
Può essere trovato in negozi regalo come pietre magiche, giardino chimico o giardino di vetro. La sua forma secca è miscelata con sali di metalli diversi.
Quando si lancia in acqua, il sodio viene sostituito dal metallo e poiché il silicato di metallo non è solubile in acqua, si forma un precipitato del colore caratteristico del metallo. Il silicato metallico si espande anche come gel e cresce come stalagmiti colorati in acqua.
Può servirti: idrossido di nichel (III): struttura, proprietà, usi, rischiVantaggi medici dell'acido ortosillico (OSA)
L'acido ortosilico è il miglior silicio biodisponabile per l'uomo. Questo può essere usato per trattare diverse condizioni di salute, come la malattia di Alzheimer, l'artrite, l'aterosclerosi, l'ipertensione, le malattie cardiache, l'osteoporosi o l'ictus.
Salute delle ossa
Studi scientifici indicano che l'acido ortosillico stimola la produzione di collagene (proteina trovata nel tessuto connettivo) e nel promuovere lo sviluppo di cellule formanti ossee.
Salute dei capelli
Allo stesso modo, l'evidenza scientifica suggerisce che questo acido può aiutare a migliorare la qualità e la salute dei capelli. Questo acido può aumentare la forza dei capelli e dello spessore. In generale, la qualità dei capelli migliora con gli integratori di acido ortosalicilico.
Riferimenti
- Centro nazionale per le informazioni sulla biotecnologia. Recuperato da Pubchem.NCBI.Nlm.NIH.Gov.
- Graham, t. (1863). Sulle proprietà dell'acido silicico e di altre sostanze colloidali analoghe. Atti della Royal Society di Londra. Recuperato da Jstor.org.
- Composto chimico dell'acido silicico. Recuperato dalla Britannica.com.

