Struttura di acido ipocloroso (HCLO), proprietà, usi, sintesi
- 4137
- 1080
- Dante Morelli
Lui Acido ipocloroso È un composto inorganico la cui formula chimica è HCLO. Corrisponde almeno arrugginito agli oxoacidi di cloro, perché contiene solo un atomo di ossigeno. Da lui deriva l'anione dell'ipoclorito, clo-, e i suoi sali, ampiamente usati come disinfettanti d'acqua commerciali.
L'HCLO è l'agente ossidante e antimicrobico più forte di quello che viene generato quando il cloro gassoso si dissolve in acqua. La sua azione antisettica è nota da più di un secolo, anche prima che le soluzioni di cloro fossero usate per pulire le ferite dei soldati nella prima guerra mondiale.
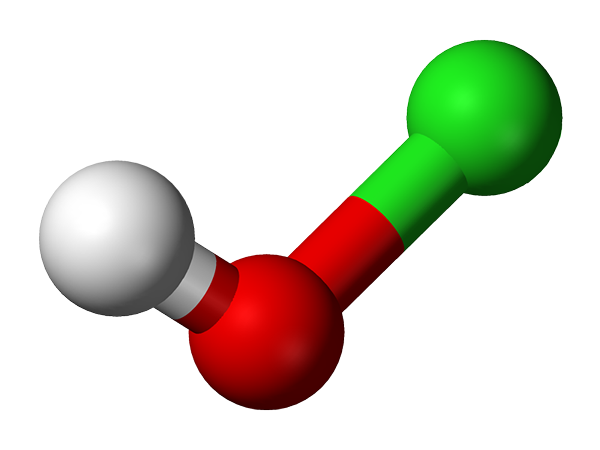
 Molecola di acido ipocloro rappresentato da un modello di sfere e barre. Fonte: Ben Mills e Jynte [dominio pubblico]
Molecola di acido ipocloro rappresentato da un modello di sfere e barre. Fonte: Ben Mills e Jynte [dominio pubblico] La sua scoperta di fatto risale al 1834, dal chimico francese Antoine Jérôme Balard, che ha raggiunto l'ossidazione parziale del cloro che lo faceva gorgogliare in una sospensione acquosa di ossido di mercurio, hgo. Da allora, è stato usato come disinfettante e agente antivirale.
Dal punto di vista chimico, l'HCLO è un agente ossidante che finisce per dare il suo atomo di cloro ad altre molecole; Cioè, con lui che i composti clorurati possono essere sintetizzati, essendo cloroamine di grande rilevanza nello sviluppo di nuovi antibiotici.
Negli anni '70, è stato scoperto che il corpo è in grado di produrre naturalmente questo acido attraverso l'azione dell'enzima mieloperossidasi; enzima che agisce su perossidi e anioni di cloruro durante la fagocitosi. Quindi, dallo stesso organismo questo "assassino" di intrusi può sorgere, ma su una scala innocua per il suo benessere.
[TOC]
Struttura
La struttura HCLO mostra nell'immagine superiore. Si noti che la formula contraddice la struttura: la molecola è H-O-CL e NO H-CL-O; Tuttavia, quest'ultimo è solitamente preferito essere in grado di confrontarlo direttamente con le sue controparti più ossidate: HCLO2, HCLO3 E hclo4.
 Struttura chimica dell'acido ipocloroso.
Struttura chimica dell'acido ipocloroso. Idrogeno acido, h+, Rilasciato dall'HCLO si trova nel gruppo OH collegato all'atomo di cloro. Nota le notevoli differenze di lunghezza nei collegamenti O-H e Cl-O, quest'ultimo è il più lungo a causa del basso grado di sovrapposizione di orbitali di cloro, più diffusi, con quelli di ossigeno.
La molecola di hocl può rimanere a malapena stabile in condizioni normali; Non può essere isolato dalle sue soluzioni acquose senza sproporzione o rilascio come cloro gassoso, CL2.
Pertanto, non ci sono cristalli anidri (nemmeno idrati di essi) di acido ipocloroso; E ad oggi, non ci sono indicazioni che possano essere preparate con metodi stravaganti. Se per cristallizzare, le molecole HCLO interagirebbero tra loro attraverso i loro dipoli permanenti (carichi negativi orientati verso ossigeno).
Può servirti: cicloesco: struttura, proprietà, sintesi e usiProprietà
Acidità
HCLO è un acido monoprotico; Cioè, puoi solo donare un H+ all'ambiente acquoso (che è dove si forma):
HCLO (AC) + H2O ↔ clo-(AC) + H3O+(AC) (PKA = 7,53)
Da questa equazione di equilibrio si osserva che una diminuzione degli ioni h3O+ (Un aumento della basicità dell'ambiente), favorisce la formazione di più anioni di ipoclorito, CLO-. Di conseguenza, se si desidera conservare una soluzione di CLO relativamente stabile- È necessario che il pH sia di base, che si ottiene con NaOH.
La sua costante di dissociazione, PKA, è consapevole che l'HCLO è un acido debole. Pertanto, quando lo manipola concentrato, non dovremmo preoccuparci così tanto degli ioni H3O+, ma dall'HCLO stesso (data la sua alta reattività e non dalla sua corrosività).
Agente ossidante
È stato detto che l'atomo di cloro nell'HCLO ha un numero di ossidazione di +1. Ciò significa che richiede a malapena il guadagno di un singolo elettrone di tornare al suo stato basale (CL0) e per essere in grado di formare la molecola CL2. Di conseguenza, l'HCLO sarà ridotto a CL2 e h2Oppure, ossidando un'altra specie più rapidamente rispetto allo stesso CL2 o clo-:
2HCLO (AC) + 2H+ + 2e- ↔ Cl2(g) + 2h2O (l)
Questa reazione consente di intravedere quanto stabile l'HCLO nelle sue soluzioni acquose.
La sua potenza ossidante non è misurata solo dalla formazione di Cl2, ma anche per la sua capacità di rinunciare al suo atomo di cloro. Ad esempio, è possibile reagire con le specie di azoto (comprese le basi di ammoniaca e azoto), per causare cloroamine:
HCLO + N-H → N-CL + H2O
Si noti che un collegamento N-H, un gruppo amino (-nh è rotto (-nh2) principalmente, ed è sostituito da un n-cl. Lo stesso vale per i legami O-H dei gruppi idrossilici:
HCLO + O-H → O-CL + H2O
Queste reazioni sono cruciali e spiegano l'azione disinfettante e antibatterica dell'HCLO.
Stabilità
HCLO è instabile quasi dove guarda. Ad esempio, l'anione dell'ipoclorito è sproporzionato nelle specie di cloro con un numero di ossidazione di -1 e +5, più stabile di +1 nell'HCLO (H+Cl+O2-)
3cl-(AC) ↔ 2Cl-(AC) + CLO3-(AC)
Questa reazione sposterebbe l'equilibrio verso la scomparsa dell'HCLO. Inoltre, l'HCLO partecipa direttamente a un equilibrio parallelo con acqua e gas di cloro:
Può servirti: fusioneCl2(g) + H2O (l) ↔ hclo (ac) + h+(AC) + CL-(AC)
Ecco perché cercare di riscaldare una soluzione HCLO per concentrarla (o isolarla) porta alla produzione di CL2, che è identificato essendo un gas giallo. Allo stesso modo, queste soluzioni non possono essere esposte alla luce per troppo tempo o alla presenza di ossidi metallici, mentre si rompono il CL2 (HCLO scompare ancora di più):
2cl2 + 2h2O → 4HCL + O2
L'HCL reagisce con l'HCLLO per generare più cl2:
HCLO + HCL → CL2 + H2O
E così via fino a quando non c'è più HCLO.
Sintesi
Acqua e cloro
Uno dei metodi per preparare o sintetizzare l'acido ipocloroso è già stato implicitamente spiegato: dissolvere il cloro gassoso in acqua. Un altro metodo abbastanza simile è quello di dissolversi in acqua l'anidride di questo acido: il monossido di dicloro, CL2O:
Cl2O (g) + h2O (l) ↔ 2HCLO (AC)
Ancora una volta non c'è modo di isolare l'HCLO puro, poiché evapora l'acqua sposterebbe l'equilibrio alla formazione di CL2Oppure, gas che sarebbe fuggito dall'acqua.
D'altra parte, è stato possibile preparare soluzioni più concentrate di HCLO (al 20%) usando l'ossido di mercurio, HGO. Per fare ciò, il cloro si dissolve in un volume d'acqua proprio nel suo punto di congelamento, in modo che si ottenga il ghiaccio clorato. Quindi, questo stesso ghiaccio viene agitato e mentre si scioglie, viene mescolato con l'HGO:
2cl2 + HGO + 12h2O → 2HCLO + HGCL2 + 11h2O
Il 20% di dissoluzione HCLO può finalmente essere distillato nel vuoto.
Elettrolisi
Un metodo più semplice e più sicuro per preparare soluzioni di acido ipocloroso è usare i salmuelas come materia prima anziché il cloro. I salmueras sono ricchi di anioni di cloruro, CL-, che attraverso un processo di elettrolisi può ossidare2:
2h2O → o2 + 4h+ + 4e-
2cl- ↔ 2e- + Cl2
Queste due reazioni si verificano nell'anodo, in cui viene prodotto il cloro che si dissolve immediatamente per avere origine HCLO; Mentre nel compartimento catodico, l'acqua viene ridotta:
2h2O + 2e- → 2OH- + H2
In questo modo, l'HCLO su scala commerciale a industriale può essere sintetizzato; E queste soluzioni ottenute da Salmueras sono, in effetti, i prodotti disponibili nel mercato di questo acido.
Applicazioni
Caratteristiche generali
L'HCLO può essere usato come agente ossidante per ossidare gli alcoli ai chetoni e per sintetizzare cloramine, cloramidi o cloridri (a partire dagli alcheni).
Tuttavia, tutti gli altri suoi usi possono essere racchiusi in una parola: Biocida. È un fungo, batteri, virus e tossine rilasciate da agenti patogeni.
Può servirti: acido maleico: struttura, proprietà, ottenimento, usiIl sistema immunitario del nostro corpo sintetizza il proprio HCLO mediante l'azione dell'enzima mieloperossidasi, aiutando i globuli bianchi a sradicare gli intrusi che causano l'infezione.
Gli infiniti degli studi propongono vari meccanismi di azione HCLO sulla matrice biologica. Ciò dona il suo atomo di cloro ai gruppi amminici di alcune proteine e ossida anche i loro gruppi SH presenti ai disolfuri S-S, risultando come denaturazione di essi.
Smette anche la replicazione del DNA reagendo con basi di azoto, influisce sulla completa ossidazione del glucosio e può anche deformare la membrana cellulare. Tutte queste azioni finiscono per causare la morte ai germi.
Disinfezione e pulizia
Ecco perché HCLO Solutions finisce per essere utilizzato per:
-Trattamento delle ferite infettive e di Gangrene
-Disinfettare le forniture idriche
-Agente sterilizzante del materiale chirurgico o strumenti utilizzati in veterinaria, medicina e odontoiatria
-Disinfettante di qualsiasi tipo di superficie o oggetto in generale: barre, corrimano, macchine per il caffè, ceramica, tavoli di vetro, locande da laboratorio, ecc.
-Sintetizzare cloroamine che servono come antibiotici meno aggressivi, ma allo stesso tempo più durevoli, specifici e stabili dello stesso HCLO
Rischi
Le soluzioni HCLO possono essere pericolose se sono molto concentrate, poiché possono reagire violentemente con le specie che potrebbero ossidare. Inoltre, tendono a rilasciare cloro gassoso destabilizzante, quindi devono essere conservati in un rigoroso protocollo di sicurezza.
L'HCLO è così reattivo nei confronti dei germi, che dove viene irrigato scompare nell'atto, senza rappresentare un rischio in seguito per coloro che toccano le superfici da lui trattate. Lo stesso accade all'interno dell'organismo: viene rapidamente scomposto o viene neutralizzato da qualsiasi specie dell'ambiente biologico.
Quando l'organismo stesso genera, è presumibilmente che ciò possa tollerare basse concentrazioni di HCLO. Tuttavia, se è molto concentrato (utilizzato per scopi sintetici e non coninfettanti), può portare a effetti indesiderati attaccando anche cellule sane (pelle, ad esempio).
Riferimenti
- SHIVER & ATKINS. (2008). Chimica inorganica. (Quarta edizione). Mc Graw Hill.
- Gottardi, w., Debabov, d., & Nagl, m. (2013). N-cloramine, una classe promettente di anti-infettativi topici ben rafforzati. Agenti antimicrobici e chemioterapia, 57 (3), 1107-1114. Doi: 10.1128/AAC.02132-12
- Di Jeffrey Williams, Eric Rasmussen e Lori Robins. (6 ottobre 2017). Acido ipocloroso: sfruttare una risposta innata. Recuperato da: InfectionControl.Suggerimenti
- Strumenti idro. (S.F.). Chimica di base della clorazione. Estratto da: Hydroinstrunts.com
- Wikipedia. (2019). Acido ipocloroso. Recuperato da: in.Wikipedia.org
- Serhan Sakarya et al. (2014). Acido ipocloroso: un agente ideale per la cura della ferita con potente potenza di guarigione del microbicida, antibiofilm e ferite. Ferite HMP. Recuperato da: WoundsResearch.com
- Prebchem. (2016). Preparazione di acido ipocloroso. Recuperato da: prepchem.com
- « 15 Vantaggi delle mele per la salute fisica e mentale
- Origine del campo magnetico della Terra, caratteristiche, funzione »

