Formazione anione, caratteristiche e tipi
- 2087
- 432
- Dante Morelli
UN anione Sono tutte specie chimiche con carico negativo, oltre ad essere uno dei due tipi di ioni esistenti. Il suo carico negativo proviene dal fatto che presenta un eccesso di elettroni rispetto alla forma neutra della specie; Per ogni elettrone aggiuntivo, il suo carico negativo aumenta in un'unità.
Il carico negativo può essere posizionato in uno o più atomi, oltre a coprire la sua influenza su una molecola nella sua interezza. Attraverso la semplificazione, indipendentemente da dove sia (-), è considerato un anione per l'intera specie, composto o molecola.
 Anioni. Fonte: Gabriel Bolívar.
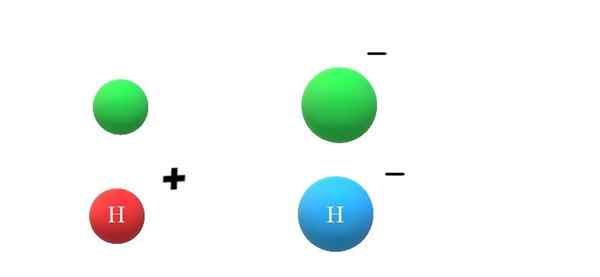
Anioni. Fonte: Gabriel Bolívar. Se una specie neutra vince un elettrone, i carichi negativi in eccesso si manifesteranno nella formazione di anione x-, che porterà anche l'aumento del suo raggio atomico (immagine superiore, con sfere verdi). X e X- differiscono molto nelle loro proprietà e nel modo in cui interagiscono con l'ambiente.
Se ora dovrebbe+ o h-, rispettivamente. Il catione h+ È lo ione idrogeno, chiamato anche protone; e h- È l'anione idruro, il più "semplice" di tutti gli anioni noti.
[TOC]
Allenamento di un anione
La formazione di un anione può essere facilmente spiegata all'interno della teoria; Sebbene, sperimentalmente, può diventare una sfida, soprattutto se vuoi puro, senza accuse positive attratte dalle tue accuse negative.
Carichi formali e meno collegamenti
Un anione si formerà quando c'è un eccesso o guadagno di elettroni in un atomo. Questo guadagno può essere determinato usando carichi formali in una struttura Lewis. Inoltre, attraverso il metodo precedente puoi sapere esattamente quale atomo o gruppo di essi arriva il carico negativo.
Può servirti: acetonitrile (C2H3N)Quando gli atomi formano legami covalenti, sebbene la distribuzione di elettroni sia equa, potrebbe esserci una perdita parziale di elettroni. In questo senso, meno collegamenti formano le coppie più elettroniche, più senza elettroni che avranno e quindi visualizzano carichi negativi.
Considera ad esempio la molecola di ammoniaca, NH3. Il NH3 È neutro e quindi non ha cariche elettriche. Se una H fosse rimossa, cioè un collegamento N-H è stato rotto, l'anione NH sarebbe stato ottenuto2-. Disegnare la sua struttura di Lewis e calcolare il carico formale di n puoi verificarlo.
Seguendo la rottura di più collegamenti N-H, ora hai l'anione NH2-; ed eliminando l'ultima h, l'anione n si ottiene finalmente3-, Chiamato Nitruro anionico. L'azoto non ha più come guadagnare più elettroni e il suo carico -3 è il più negativo che può raggiungere; I suoi orbitali non danno di più.
Riduzioni
Un anione può formare un prodotto di una riduzione: guadagna elettroni ossidanti a un'altra specie, che li perde. L'ossigeno, ad esempio, rappresenta molto bene questo tipo di reazione chimica.
Quando l'ossigeno è ridotto, ossidato a un'altra specie e diventa anione di ossido, o2-; presente in innumerevoli minerali e composti inorganici.
Fisico
Un atomo può guadagnare elettroni se è in una fase gassosa:
X (g) + e- => X-(G)
Questo modo di formare un anione implica un'ampia conoscenza delle tecniche fisiche, mentre gli anioni gassosi non sono facili da studiare, né tutte le specie sono volatilizzate o atomizzate con semplicità nella fase gassosa.
Caratteristiche
In termini generali, le caratteristiche tipiche di un anione saranno menzionate di seguito prima di affrontare i suoi tipi ed esempi:
-È più ingombrante del atomo neutro da cui.
Può servirti: biossido di cloro (CLO2): struttura, usi, ottenimento, rischi, proprietà-Può essere più o meno stabile, nonostante la crescente repulsione elettronica tra i suoi elettroni.
-Se l'anione proviene da un piccolo atomo elettronegativo, come il carbonio, è molto reattivo.
-Impostare forti momenti di dipolo.
-Aumenta ulteriormente la sua interazione con i solventi polari.
-L'anione monoatomico è isolettronico per il gas nobile del suo periodo; cioè, ha nel suo strato di valenza lo stesso numero di elettroni.
-Può polarizzare la nuvola elettronica di un atomo vicino, respingendo i suoi elettroni esterni.
Ragazzi
Monoatomico
Come suggerisce il nome, è un anione che consiste in un singolo atomo: il carico negativo è ben posizionato. Ogni gruppo nella tabella periodica ha carichi negativi caratteristici; E poiché sono anioni, sono i non metallici situati nel blocco P. Alcuni esempi e i loro nomi sono sotto:
-Cl-, cloruro.
-Yo-, io duro.
-F-, fluoruro.
-Br-, bromuro.
-O2-, ossido.
-S2-, solfuro.
-LUI2-, Seleniuro.
-Tè2-, TelUruro.
-Po2-, Polyoniuro.
-N3-, Nitruro.
-P3-, fosfuro.
-Asso3-, Arseniuro.
-Sb3-, Antimoniuro.
-C4-, carburo.
-Sì4-, Siliciuro.
-B3-, Boruro.
Oxoanions
Gli oxoanioni sono caratterizzati dall'avere un legame x = o, dove x può essere qualsiasi elemento non metallico (tranne il fluoruro) o un metallo (cromo, manganese, ect.). Possono anche avere uno o più semplici collegamenti X-O.
Alcuni oxoanioni con i loro rispettivi nomi sono:
-Clo-, ipoclorito.
-Fra-, Hipobromito.
-Io-, ipoyodite.
-Clo2-, Clorito.
-Clo3-, clorato.
-Io3-, Yodutato.
-Clo4-, perclorato.
-Po43-, fosfato.
-Co32-, carbonato.
-CRO42-, cromato.
-Cr2O72-, Dicromato.
-SW42-, solfato.
-S2O32-, Tiosulfato.
-NO3-, nitrato.
-NO2-, nitrito.
-Bo33-, borato.
-Aso43-, Arseniato.
-Po33-, fosfito.
-MNE4-, permanganato.
Biologico
Le molecole organiche hanno gruppi funzionali che possono essere caricati elettricamente. COME? Mediante formazione o rottura di legami covalenti, molto simili all'esempio della molecola NH3.
Può servirti: ferro (elemento): caratteristiche, struttura chimica, usiAlcuni anioni organici sono:
-Cap3COO-, acetato.
-Hcoo-, Formato.
-C2O42-, Ossalato.
-Rcoo-, Carbossilato.
-Cap3Conh-, Amidato.
-Ro-, Alcossido.
-R3C-, Carbanion.
-Cap3O-, Metossido.
Poliiatomico
Gli oxoanioni sono anche anioni poliatomici, cioè sono costituiti da più di un atomo. Lo stesso vale per gli anioni organici. Tuttavia, il poliiatomico non inserisce nessuna delle classificazioni precedenti. Alcuni di loro sono:
-Cn-, cianuro (ha un triplo collegamento, cistico).
-Ocn-, Cianato.
-Scn-, Tiociarato.
-NH2-, Amiduro.
-OH-, idrossile, idrossido o ossigrillo.
-O2-, superossido.
-O22-, perossido.
Molecolare o complesso
Negli anioni organici sono stati menzionati alcuni gruppi funzionali caricati negativamente. Questi gruppi possono far parte di una grande molecola, e quindi l'anione può essere un composto robusto e molti collegamenti. Il più semplice di questo tipo di anioni è l'ipotetica molecola H2-.
Tra un altro esempio di questi anioni ci sono Polysulfuros, sN2-, che consistono in catene con più collegamenti S-S. Allo stesso modo, si possono conteggiare i composti di coordinazione del metallo con carico negativo, come [COCL4(NH3)2"- e [Cucl4"2-.
Riferimenti
- Whitten, Davis, Peck e Stanley. (2008). Chimica. (8 ° ed.). Apprendimento del Cengage.
- Wikipedia. (2019). Anione. Recuperato da: è.Wikipedia.org
- Helmestine, Anne Marie, PH.D. (21 marzo 2019). Elenco della tabella degli anioni e formule comuni. Recuperato da: Thoughtco.com
- Fondazione CK-12. (29 giugno 2016). Formazione di anioni. Chimica librettexts. Recuperato da: Chem.Librettexts.org
- Francis e. (2002). Anioni. Clackamas Community College. Estratto da: DL.Clackama.Edu
- Società fisica americana. (3 novembre 2011). Sinossi: l'anione molecolare più semplice. Recuperato da: fisica.APS.org
- « Biografia, stile, opere e frasi di Fernando del Paso
- Struttura di Anisol, proprietà, nomenclatura, rischi e usi »

