Struttura dell'alcool terziario, proprietà, esempi
- 5086
- 1546
- Baldassarre Ross
UN Alcool terziario È quello in cui il gruppo idrossilico, OH, è collegato a un carbonio terziario. La sua formula continua ad essere ROH, come altri alcoli; Ma è facilmente riconosciuto perché OH è vicino a una x nella struttura molecolare. Inoltre, la sua catena gassata è generalmente più corta e la sua massa molecolare principale.
Quindi, un alcol terziario tende ad essere più pesante, è più ramificato ed è anche il meno reattivo rispetto all'ossidazione; Cioè, non può essere trasformato in un cetone o acido carbossilico come si verifica rispettivamente con alcoli secondari e primari.
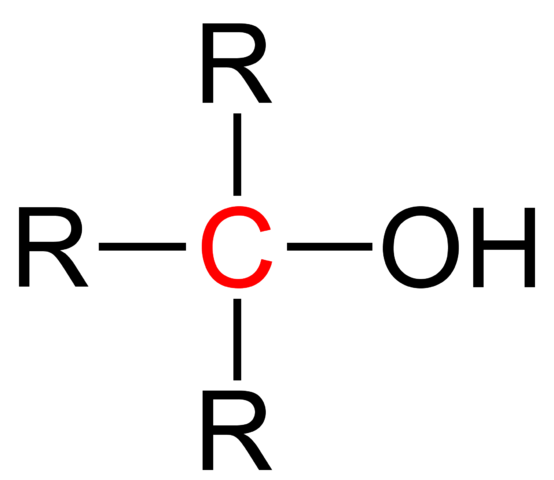
 Formula strutturale di un alcol terziario. Fonte: Jü [dominio pubblico].
Formula strutturale di un alcol terziario. Fonte: Jü [dominio pubblico]. La formula strutturale generale per un alcol terziario è mostrata nell'immagine superiore. Secondo lei, potrebbe essere scritta una nuova formula di tipo R3COH, dove R può essere un gruppo alchil o arilico; Un gruppo metilo, ch3, o una catena gassata corta o lunga.
Se i tre gruppi R sono diversi, il carbonio centrale dell'alcool terziario sarà chirale; Cioè, l'alcol presenterà attività ottica. Per questo fatto, gli alcoli quirali terziari accusano l'interesse all'interno dell'industria farmaceutica, poiché dai chetoni con attività biologica questi alcoli sono sintetizzati con strutture più complesse.
[TOC]
Struttura di un alcol terziario
 Tre alcoli terziari e le loro strutture. Fonte: Gabriel Bolívar.
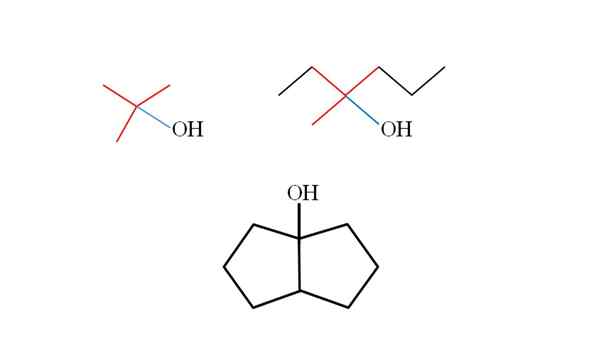
Tre alcoli terziari e le loro strutture. Fonte: Gabriel Bolívar. Considera le strutture degli alcoli terziari superiori per imparare a riconoscerli indipendentemente dal composto. Il carbonio collegato a OH deve anche essere collegato ad altri tre carboni. Se viene osservato in dettaglio, i tre alcoli sono conformi a questo.
Il primo alcol (a sinistra) è composto da tre gruppi CH3 Centro di carbonio centrale collegato, la cui formula sarebbe (Cho3)3COH. Il gruppo di noleggio (scegli3)3C- È noto come tertbutil.
Può servirti: potenziometro (fameter)Il secondo alcol (a destra), ha il carbonio centrale Lin3, Cap3Cap2 e ch2Cap2Cap3. Poiché i tre gruppi sono diversi, l'alcol è chirale e quindi mostra un'attività ottica. Una T non è osservata qui, ma una x vicina a OH (rosso e blu).
E nel terzo alcol (sotto e senza colori), l'OH è collegato a uno dei due carboni che si uniscono a due ciclopentani. Questo alcol non presenta attività ottica perché due dei gruppi collegati al carbonio centrale sono identici. Come il secondo alcol, se viene attentamente osservato, verrà anche trovata una X (piuttosto un tetraedro).
Ostacolo sterico
I tre alcoli superiori hanno qualcosa di più in comune di una X: il carbonio centrale è stericamente prevenuto; Cioè, ci sono molti atomi che lo circondano nello spazio. Una conseguenza immediata di ciò è che i nucleofili, desiderosi di cariche positive, hanno difficoltà ad affrontare questo carbonio.
D'altra parte, avendo tre carbonio legati al carbonio centrale, donano parte della densità elettronica che l'atomo elettronegativo dell'ossigeno lo sottrae, stabilizzandolo ancora di più davanti a questi attacchi nucleofili. Tuttavia, l'alcol terziario può subire una sostituzione formando carbocalizzazione.
Proprietà
Fisico
I terzo alcoli presentano generalmente strutture altamente ramificate. Una prima conseguenza di ciò è che il gruppo OH è prevenuto, e quindi il suo momento di dipolo esercita un effetto minore sulle molecole vicine.
Ciò si traduce in interazioni molecolari più deboli rispetto a quelle degli alcoli primari e secondari.
Può servirti: principio di Le ChâtelierAd esempio, considera gli isomeri strutturali del butanolo:
Cap3Cap2Cap2OH (N-Butanolo, peb = 117ºC)
(Ch3)2Cap2OH (alcol isobutilico, PEB = 107ºC)
Cap3Cap2Ch (oh) ch3 (Alcol secutilico, PEB = 98ºC)
(Ch3)3COH (alcool tertbutilico, PEB = 82ºC)
Nota come scendono i punti di ebollizione man mano che l'isomero diventa più ramificato.
Inizialmente è stato menzionato che nelle strutture degli alcoli si osservano 3 an x, che di per sé indica un ramo elevato. Ecco perché questi alcoli tendono ad avere punti di fusione e/o di ebollizione più bassi.
Leggermente simile è il caso della tua miscibilità con l'acqua. Più impedito, meno miscibile oh sarà l'alcool 3 con acqua. Tuttavia, questa miscibilità riduce più a lungo la catena del carbonio; Pertanto, l'alcol termico è più solubile e miscibile con l'acqua che il N-Butanolo.
Acidità
Gli alcoli terziari tendono ad essere i minimi acidi di tutti. Le ragioni sono numerose e si riferiscono tra loro. Nei conti di riepilogo, il carico negativo del suo alcossido derivato, rosso-, Sentirai una forte repulsione per i tre gruppi alcali legati al carbonio centrale, indebolendo l'anione.
Più è instabile l'anione, meno l'acidità dell'alcol sarà.
Reattività
Il terzo alcol non possono subire ossidazioni ai chetoni (R2C = O) o aldeide (RCHO) o acidi carbossilici (Rcooh). Da un lato, dovrei perdere uno o due carboni (sotto forma di CO2) per ossidare, che diminuisce la sua reattività contro l'ossidazione; E dall'altro, manca di idrogeno che può perdere per formare un altro legame con l'ossigeno.
Può servirti: piridina: struttura, proprietà, usi, tossicità, sintesiTuttavia, possono subire sostituzione ed eliminazione (formazione di un doppio legame, un alchene o olefina).
Nomenclatura
La nomenclatura per questi alcoli non è diversa da quella degli altri. Ci sono nomi comuni o tradizionali e i nomi sistematici governati dall'IUPAC.
Se la catena principale e le sue ramificazioni sono costituite da un gruppo di noleggio riconosciuto, viene utilizzata per il suo nome tradizionale; Quando non è possibile farlo, viene utilizzata la nomenclatura IUPAC.
Ad esempio, considera il seguente alcol terziario:
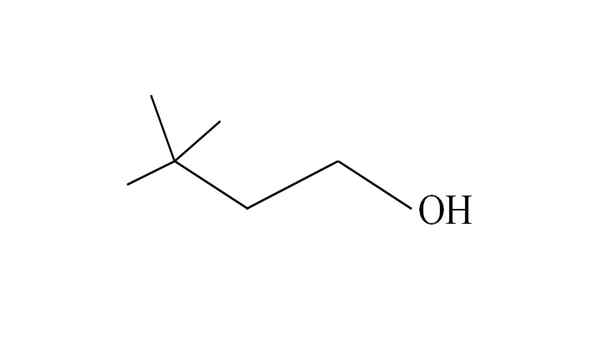 3.3-dimetil-1-butanolo. Fonte: Gabriel Bolívar.
3.3-dimetil-1-butanolo. Fonte: Gabriel Bolívar. Comincia a elencare i carboni da destra a sinistra. Nel C-3 ci sono due gruppi CH3 di sostituenti, e quindi il nome di questo alcol è 3,3-dimetil-1-butanolo (la catena principale ha quattro carboni).
Allo stesso modo, l'intera catena e le sue ramificazioni sono costituite dal gruppo Neohexilo; Pertanto, il suo nome tradizionale può essere l'alcol neoexil o neoesanolo.
Esempi
Infine, vengono menzionati alcuni esempi di alcoli terziari:
-2-metil-2-propanolo
-3-metil-3-esanolo
-Biciclo [3,3,0] ottan-1-ol
-2-metil-2-butanolo: cap3Cap2COH (Ch3)2
Le formule dei primi tre alcoli sono rappresentate nella prima immagine.
Riferimenti
- Carey f. (2008). Chimica organica. (Sesta edizione). Mc Graw Hill.
- Morrison, r. T. e Boyd, r, n. (1987). Chimica organica. (5a edizione). Editoriale Addison-Wesley Inter-American.
- Graham Solomons t.W., Craig b. Frigorifero. (2011). Chimica organica. Ammine. (10a edizione.). Wiley Plus.
- Gunawardena Gamini. (31 gennaio 2016). Alcool terziario. Chimica librettexts. Recuperato da: Chem.Librettexts.org
- Ashenhurst James. (16 giugno 2010). Alcoli (1) - Nomenclatura e proprietà. Recuperato da: MasterOrganicChemistry.com
- Clark J. (2015). Presentazione di alcoli. Recuperato da: ChemGuide.co.UK
- Chimica organica. (S.F.). Tema 3. Alcoli. [PDF]. Recuperato da: Sinorg.Uji.È
- Nilanjana Majumdar. (3 marzo 2019). Sintesi di alcol terziario chirale: sviluppi significativi. Recuperato da: 2.Chimica.MSU.Edu
- « Periodo formativo dell'origine, caratteristiche, prodotti
- Com'è stata la società europea nella prima metà del diciannovesimo secolo »

