Struttura, proprietà e usi dell'ossido di etilene
- 2182
- 515
- Baldassarre Ross
Lui ossido di etilene È un composto organico della famiglia di epossidi. A temperatura ambiente è gassoso, incolore e, sebbene sia quasi igienico, ha un dolce odore dolce, simile a quello degli eteri.
È un blocco di costruzione chimico molto versatile, poiché viene utilizzato in un'ampia varietà di applicazioni industriali per la produzione di altri composti chimici con usi multipli. Ciò è dovuto alla sua alta reattività, cioè con suo facilità reagire con altre sostanze.
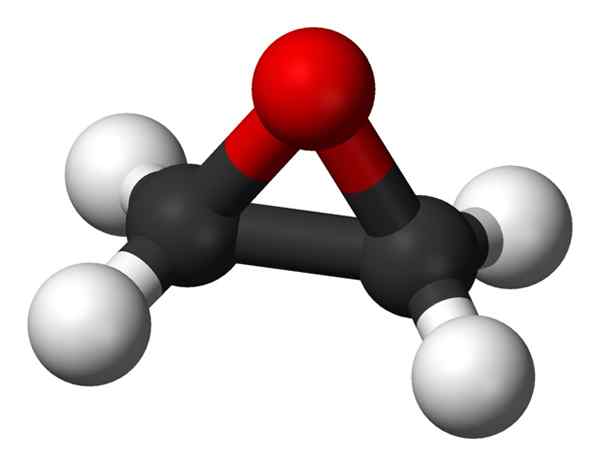
 Struttura spaziale dell'ossido di etilene. Pallie nere: atomi di carbonio; Pare bianche: atomi di idrogeno; Palla rossa: atomo di ossigeno. Benjah-BMM27 [dominio pubblico]. Fonte: Wikimedia Commons.
Struttura spaziale dell'ossido di etilene. Pallie nere: atomi di carbonio; Pare bianche: atomi di idrogeno; Palla rossa: atomo di ossigeno. Benjah-BMM27 [dominio pubblico]. Fonte: Wikimedia Commons. Una delle sue applicazioni principali è come materia prima nella produzione dei componenti dell'antigelo per i radiatori del veicolo. I suoi derivati sono impiegati come ingredienti di detergenti industriali o domestici, prodotti cosmetici e shampoo, plastificazione, preparati farmaceutici o unguenti.
È un disinfettante ampiamente usato, ad esempio nella sterilizzazione di attrezzature mediche e dentali, poiché è in grado di distruggere virus, batteri, funghi e spore, specialmente in condizioni a secco. Inoltre, è stato utilizzato per fumigare prodotti alimentari per i tuoi imballati, sebbene questo utilizzo sia messo in discussione.
Nonostante la sua utilità, deve essere manipolato con alta cautela, in quanto può causare irritazione degli occhi e della pelle. L'inalazione di ossido di etilene per lunghi periodi può influire sul sistema nervoso. Pertanto, le persone che sono esposte ai loro vapori o soluzioni devono utilizzare attrezzature e vestiti protettivi.
[TOC]
Struttura
La sua formula molecolare è C2H4O. Appartiene al gruppo di epossidi, essendo il più semplice e importante di questi. Ha la forma di un anello di tre membri.
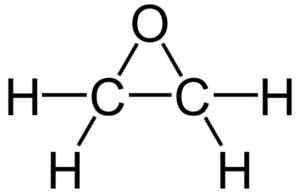 Struttura dell'ossido di etilene. Fonte: Wikimedia Commons
Struttura dell'ossido di etilene. Fonte: Wikimedia Commons A causa della sua struttura di anello triangolare, l'ossido di etilene è molto reattivo, il che è dovuto alla facilità con cui si apre l'anello. In media, gli angoli di collegamento sono 60º, il che rende deboli i loro collegamenti. La molecola è meno stabile di quella di un etere lineare e tende a reagire facilmente con altri composti chimici.
Può servirti: nitrito di sodio (nano2): struttura, proprietà, usi, rischiProprietà
Altri nomi
- Oxyran.
- Epoxietano.
Stato fisico
A temperatura ambiente e sotto pressione atmosferica, è un gas. Sotto 10,6 ºC e sotto pressione atmosferica, è un liquido. Sotto -111 ºC è solido.
Peso molecolare
44,05 g/mol.
Punto d'infiammabilità
Meno di 0 ºF (-17,8 ºC).
Densità
La sua densità è inferiore a quella dell'acqua, essendo da 0,882 a 10 ºC. A loro volta, i loro vapori sono più pesanti dell'aria.
Solubilità
È solubile in acqua, benzene, acetone, etanolo ed etere. È miscibile con tetracloruro di carbonio.
Temperatura di autorezione
428,9 ºC.
Altre proprietà
- Se subisce riscaldamento o contaminazione, può polimerizzare esotermicamente (producendo una grande quantità di calore). Se la polimerizzazione si verifica all'interno di un contenitore, può essere violentemente rotta.
- Può reagire con materiali ossidanti.
- È estremamente tossico, cancerogeno e buone mutazioni generatore nei batteri e nelle cellule di mammifero.
Produzione
Su una scala industriale è preparato mediante ossidazione di etilene con ossigeno (o2) dall'aria. La velocità di questa reazione è aumentata con la presenza di metallo argento (AG) e azione di temperatura. Successivamente, la reazione viene mostrata:
AG, 250 ° C
2 c2H4 + O2 -> 2c2H4O
Ossido di etilene etilene
Rischi
Alla salute
- È stato riferito che produce disturbi neurologici e che la morte può causare. La concentrazione inferiore che può generare effetti tossici per inalazione è 12.500 ppm/10 secondi (ppm mezzi: parti per milione).
- È una pelle forte, gli occhi e il tratto respiratorio.
Può servirti: samario: caratteristiche, struttura, ottenimento, usi- L'esposizione al vapore con alta concentrazione di ossido di etilene può causare irritazione agli occhi, infiammazione della membrana oculare e danni da cornea.
- Lo sviluppo della cataratta è stato associato all'esposizione ai loro vapori e spruzzi. Con soluzioni concentrate ci sono gravi danni agli occhi.
- Il contatto di soluzioni acquose di ossido di etilene con la pelle produce irritazione e può portare a una grave dermatite con ampoule e ustioni.
- La sua inalazione può influire sul sistema nervoso, causando mal di testa e nausea, tra gli altri sintomi.
Fuoco
- Se esposto a una fiamma o calore c'è il pericolo di esplosione. Quando riscaldati generano vapori pericolosi.
- Vapore forma miscele esplosive con aria in una vasta gamma di concentrazioni.
- Dovrebbe essere evitato di manipolarlo con attrezzature contenenti metalli come rame, argento, mercurio, magnesio, alluminio o ossidi di ferro, oltre a evitare agenti come ammoniaca, agenti ossidanti, acidi o basi organiche. Tutti questi materiali possono accelerare la loro polimerizzazione e/o esplosione.
Applicazioni
Applicazioni industriali
È usato come intermediario nella produzione di altri prodotti chimici, che a loro volta vengono utilizzati nella produzione di fibre di poliestere per abbigliamento, tappezzeria, tappeti e cuscini.
Con ossido di etilene, il glicole etilenico viene utilizzato nell'antigelo per i motori del veicolo. Il glicole etilenico è anche utilizzato nella produzione in fibra di vetro e nei film di plastica per l'imballaggio.
Altre sostanze chimiche prodotte dall'ossido di etilene includono tensioattivi non ionici usati in detergenti e formule per lavare i piatti.
Può servirti: isobutil: nomenclatura, formazione, struttura e caratteristicheApplicazioni mediche
Viene usato come agente sterilizzante di attrezzature mediche, come strumenti chirurgici, aghi ipodermici e iniettori o protesi.
Viene anche utilizzato per sterilizzare le macchine per emodialisi, attrezzature da laboratorio, strumenti dentali, strumenti veterinari, termometri, abbigliamento chirurgico o attrezzatura di pronto soccorso, tra gli altri.
 Sala di sterilizzazione. Fonte: Pixabay.com
Sala di sterilizzazione. Fonte: Pixabay.com Sebbene ci siano diversi metodi disponibili per la sterilizzazione delle attrezzature mediche, in alcuni usi nessun trattamento disponibile può sostituire l'ossido di etilene.
Questo è il caso della sterilizzazione di alcuni materiali e radiazioni sensibili al calore, nonché alcuni strumenti e artefatti che richiedono sterilizzazione nel sito degli ospedali stessi.
Biblioteche e musei
In questi luoghi, l'ossido di etilene viene utilizzato per controllare i parassiti come funghi e insetti. Tuttavia, questo uso non è così comune e viene utilizzato quando altre alternative non sono efficaci.
Agricoltura e cibo
È stato usato come pesticida, fungicida, fumigante, erbicida, insetticida, rodenticidi, tra le altre varianti. Riduce in modo significativo la popolazione di batteri e funghi delle spezie.
Tuttavia, a causa della sicurezza e delle preoccupazioni ambientali, l'uso dell'ossido di etilene per la fumigazione alimentare è stato proibito nell'Unione Europea e negli Stati Uniti.
Riferimenti
- O.S. Biblioteca nazionale di medicina. (2019). Ossido di ethilene. Recuperato da Pubchem.NCBI.Nlm.NIH.Gov
- Fatti sulla sicurezza chimica. (2019). Ossido di ethilene. Recuperato da prodotti di sicurezza chimici.org
- Morrison, Robert Thornton; e Boyd, Robert Neilson. 1992. Chimica organica. Prentice-Hall.
- Moerman, f. e Mager, K. (2016). Pulizia e dissinfezione negli impianti di trasformazione degli alimenti secchi. Nel manuale di controllo dell'igiene nell'industria alimentare (seconda edizione). Recuperato da Scienturect.com.
- Eastmond, David a. e Balakrishnan, Sharada. (2010). Genotossia dei pesticidi. Nel manuale di tossicologia dei pesticidi di Hayes (terza edizione). Recuperato da ScienceDirect.com
- Atungulu, g.G. e pane, z. (2012). Decontaminazione microbica di noci e spezie. Nella decontaminazione microbica nel settore alimentare. Recuperato da ScienceDirect.com
- « Struttura di ossido di ferro (II), nomenclatura, proprietà, usi
- Semplici caratteristiche, funzioni e tipi di epitelio piatto »

