Struttura chimica del solfato di calcio (CASE4), Proprietà, Usi
- 3244
- 85
- Rufo Longo
Cos'è il solfato di calcio?
Lui solfato di calcio È un sale ternario di calcio, alcalino di metallo (MR. Scholambara), zolfo e ossigeno. La sua formula chimica è un caso4, Il che significa che per ogni cation ca2+ C'è un anione così42- interagendo con questo. Costituisce un composto con ampia distribuzione in natura.
Le sue forme più abbondanti sono il caso4· 2h2O (l'intonaco) e il caso di forma anidro4 (L'anidrite). Esiste anche una terza forma: l'intonaco o l'intonaco di Parigi, prodotto dal riscaldamento del gesso (l'emidrato, custodia4· 1/2h2O).
Il solfato di calcio è un composto molto utile nel lavoro dell'essere umano, poiché viene utilizzato in numerose funzioni che includono la costruzione di strade, abbellimento domestico e persino riparazione ossea.
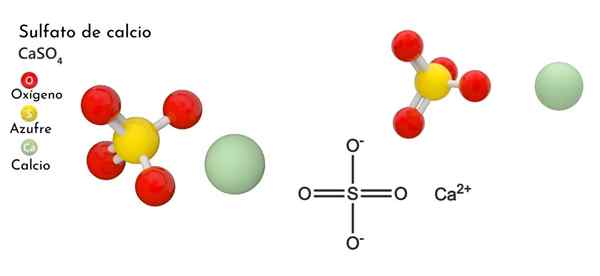
Struttura chimica del solfato di calcio

Nell'immagine superiore la cellula unitaria ortorrombica è mostrata per il caso4. Qui si presume che le interazioni siano puramente elettrostatiche; Cioè, che Cations2+ Attirano così così gli anioni tetraedrici42-.
Tuttavia, il CA2+ È altamente incline a coordinarsi, formando strutture poliedriche attorno ad esso. Per quello che è questo? Alla disponibilità elettronica del calcio per accettare elettroni di specie di base o negativa (come gli atomi di O SO42-).
Considerando il punto precedente, ora gli ioni CA2+ Accettano collegamenti dativi (forniti da O) e la cella unitaria viene trasformata, come indicato dall'immagine inferiore:
Di conseguenza, si forma poliedro cao8 (La sfera verde di Ca2+ circondato da otto sfere rosse di o tetraedra così4 vicino). Poliedros di calcio e tetraedri solfato; Questa è la struttura cristallina del caso4 anidro.
Può servirti: Bipe Beraral: a cosa serve, caratteristiche, a cosa serveInoltre, quando i cristalli sono idratati, forma il sale di -idratato o l'emidrato (caso4· 1/2 h2O)- La struttura è ritardata per incorporare molecole d'acqua.
Queste molecole possono essere intervallate e coordinate con il calcio; cioè, sostituiscono uno o due gruppi di solfato.
D'altra parte, non tutta l'acqua continua a integrare il poliedro CAO8. Alcuni, d'altra parte, formano ponti idrogeno con solfati. Questi fungono da unione per due sezioni in zigzag, prodotti della disposizione degli ioni nel vetro.
Proprietà solfato di calcio
 Aspetto del solfato di calcio
Aspetto del solfato di calcio Formula molecolare
CASE4 · NH2O.
Peso molecolare anidro
136.134 g/mol.
Odore
È un bagno.
Aspetto
Nel caso dell'anidrite, sembra una polvere bianca ortorrombica o solida monoclinica. I cristalli sono di colore variabile: possono essere bianchi o con una tintura bluastra, grigiastra o rossastra; Può anche essere rosso mattone.
Densità
2,96 gr/cm3 (forma anidra). 2,32 GR/cm3 (forma diidrata).
Punto di fusione
1450 ºC (2840 ºF). Caratteristico delle forti interazioni elettrostatiche tra gli ioni bivalenti Ca2+ E così42-.
Solubilità
0,2-0,3 % in acqua a 25 ° C. È poco solubile in acqua e insolubile in etanolo.
Stabilità
Stabile a temperatura ambiente.
Usi di solfato di calcio
In costruzione e arte
È usato nell'elaborazione dello stucco per frisar le pareti delle case e altre costruzioni che contribuiscono alla sua abbellimento. Inoltre, gli stampi multimediali sono realizzati sui tetti e sui telai delle finestre. L'intonaco è anche nei cieli di punta.
Il solfato di calcio viene utilizzato per aiutare a risolvere il problema che si verifica nell'idratazione del calcestruzzo, collaborando così nella costruzione di strade, percorsi, ecc.
Può servirti: elettrofilo: reazioni, esempi, elettrofilibilitàCon l'intonaco, le sculture sono elaborate, in particolare figure religiose, e nei cimiteri sono usate nelle pietre tombali.
Terapie
Veterinario
Sperimentalmente, i pezzi sterili del solfato di calcio sono stati usati in veterinario per riparare difetti o cavità ossei, come quelli lasciati da ferite o tumori.
L'intonaco o l'intonaco di Parigi possono essere utilizzati per riparare i difetti ossei per la loro capacità unica di stimolare l'osteogenesi. Studi a raggi X e tecnici (TC99M) MEDRONATE.
Una rigenerazione ossea è stata dimostrata in sei cani in un periodo da 4 a 6 mesi. Il solfato di calcio iniziò ad essere usato in questo campo nel 1957, a forma di compresse di gesso di Parigi, essendo in grado di riempire le ossa per cani.
La sostituzione ossea del solfato di calcio è paragonabile a quella osservata nell'osso autogenico.
Ruhaimi (2001) ha applicato il solfato di calcio in un osso mascella di coniglio appena distrutto, osservando un aumento dell'osteogenesi e della calcificazione delle ossa.
Medicinale
Il solfato di calcio viene utilizzato in medicina per immobilizzare le articolazioni che hanno subito dislocazioni e in ossa fratturate, oltre ad essere usata come eccipiente nell'elaborazione delle compresse.
odontoiatria
In odontoiatria viene utilizzato come base per elaborare le protesi dentali, nei restauri e nelle impressioni dei denti.
In elaborazione alimentare
È usato come coagulante nell'elaborazione del tofu, un cibo fatto con soia e di grande consumo nei paesi orientali come sostituto della carne. Inoltre, è stato usato come ribadicazione degli alimenti e nel trattamento delle farine.
Può servirti: alotropiaCome fertilizzante e balsamo di terreni coltivati
L'intonaco (custodia4· 2h2O) è stato usato come fertilizzante in Europa dal 18.
Il calcio deve essere disponibile per le radici delle piante per l'approvvigionamento adeguato. Quindi, l'aggiunta di calcio migliora le colture orticole e di arachidi (arachidi).
Il marciume delle radici di arachidi prodotte da agenti patogeni biologici, nonché il marciume apicale di anguria e pomodoro, sono parzialmente controllati con le applicazioni di gesso agricola.
L'intonaco aiuta a ridurre la dispersione dell'argilla, causando la formazione di croste sul terreno. Riducendo le croste formate a terra, l'intonaco facilita l'uscita delle piantine. Aumenta anche l'ingresso di aria e acqua a terra.
L'intonaco aiuta a migliorare il terreno mitigando l'acidità e la tossicità dell'alluminio, adattando così il raccolto per i terreni di sodio.
Nella produzione di altri composti
Il solfato di calcio reagisce con il bicarbonato di ammonio per formare solfato di ammonio. È stato anche utilizzato nel processo di produzione di acido solforico.
Il solfato di calcio Ashidro viene miscelato con scisto o magro e, quando la miscela viene riscaldata, viene rilasciata il triossido di zolfo. L'ossido di zolfo è un precursore dell'acido solforico.