Soluzioni chimiche
- 2430
- 623
- Dott. Rodolfo Gatti
Spieghiamo quali soluzioni chimiche, le loro caratteristiche, i tipi che esistono e danno diversi esempi
 Una sostanza chimica è una miscela omogenea tra due sostanze
Una sostanza chimica è una miscela omogenea tra due sostanze Cosa sono le soluzioni chimiche?
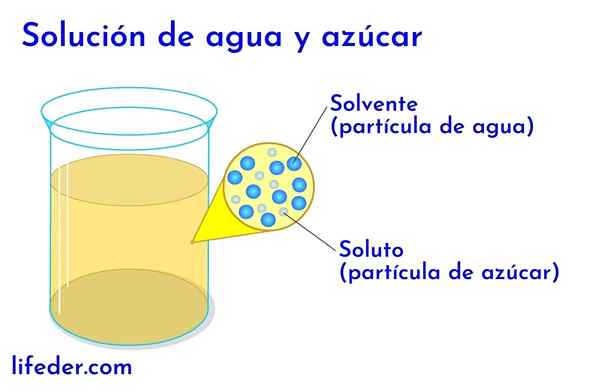
IL Soluzioni chimiche Sono miscele omogenee tra un solvente e uno o più soluti. Le soluzioni più semplici sono formate da un singolo soluto e da un solvente, ad esempio quando dissoliamo lo zucchero in acqua, ma ci sono soluzioni che possono diventare molto complesse con centinaia di soluti.
Le soluzioni più comuni sono in uno stato liquido e nella maggior parte dei casi il solvente è l'acqua. Per questo motivo, l'acqua viene solitamente chiamata "il solvente universale". Ma le soluzioni non si limitano ai liquidi, poiché ci sono soluzioni in uno stato gassoso e solido.
Il soluto può anche essere trovato in diversi stati. Ad esempio, soluzioni liquide con soluti solidi (come sale), fluidi (come alcol) o gassosi (come il gas carbonico nelle bevande analcoliche) possono avere soluzioni solide).
Come riconoscere il soluto e il solvente?
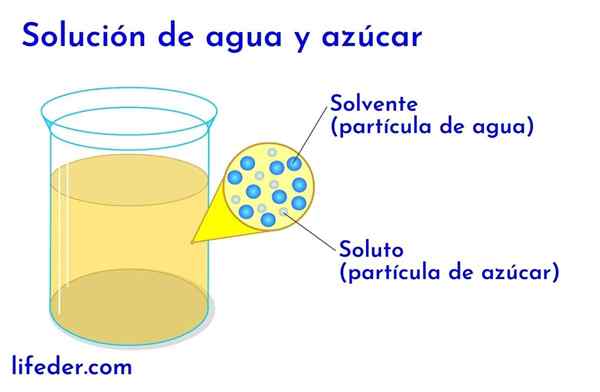 Soluto e solvente in acqua con zucchero
Soluto e solvente in acqua con zucchero In qualsiasi soluzione in cui c'è acqua, questo è considerato il solvente. In tutti gli altri casi, il solvente corrisponde al componente che è in quantità maggiore o in proporzione maggiore ed è quasi sempre un liquido. Gli altri componenti presenti nella soluzione sono considerati soluti.
Diamo un'occhiata a due esempi:
- In una soluzione di acqua e zucchero, l'acqua è il solvente e lo zucchero il soluto.
- L'alcool isopropilico che acquistiamo in farmacia è una soluzione formata da acqua e alcol. In questa soluzione il solvente è l'acqua nonostante sia in una proporzione minore rispetto all'alcol.
Caratteristiche e proprietà delle soluzioni chimiche
Sono miscele omogenee
Le soluzioni sono miscele in cui il soluto solvente non può essere distinto, né ad occhio nudo né con l'uso di un vetro d'ingrandimento o di un microscopio.
Hanno una composizione uniforme
Ciò significa che qualsiasi parte di una soluzione avrà sempre gli stessi componenti (soluto e solvente) alla stessa concentrazione.
Può servirti: cadmio (cd): storia, proprietà, struttura, usiSono caratterizzati dalla loro concentrazione
La concentrazione è una delle caratteristiche più importanti di una soluzione, poiché determina molte delle sue proprietà.
Sono traslucidi (trasparenti)
Le soluzioni liquide devono essere traslucide, cioè la luce deve essere in grado di attraversarle senza disperdersi.
Sono stabili
Una soluzione in cui il soluto e il solvente non reagiscono tra loro sarà stabile indefinitamente. Ciò significa che non subirà alcun cambiamento nel tempo, purché la sua composizione rimane costante (il solvente non evapora, per esempio).
Le sue proprietà fisiche e chimiche sono diverse da quelle del solvente
Le proprietà fisiche e chimiche del solvente cambiano durante la miscelazione con il soluto. Ad esempio, le soluzioni hanno un punto di ebollizione maggiore, un punto di fusione inferiore e hanno anche un'alta pressione osmotica rispetto al solvente puro.
Possono essere separati attraverso alcuni processi fisici e chimici
Le soluzioni non possono essere separate mediante filtrazione, centrifugazione o decantazione. Possono essere separati solo da metodi fisici o chimici come cristallizzazione, distillazione, evaporazione, osmosi inversa e cromatografia, tra gli altri.
 Strumenti di distillazione
Strumenti di distillazione Tipi di soluzioni chimiche
Le soluzioni chimiche possono essere classificate in base alla loro concentrazione, secondo la loro condizione fisica e secondo la natura del solvente:
Secondo la tua concentrazione
- Soluzioni insature: Sono quelli in cui il soluto non ha ancora raggiunto la massima concentrazione nel solvente. Per questo motivo, può essere sciolto più soluto per preparare una soluzione più concentrata.
- Soluzioni sature: Sono soluzioni in cui il solvente non può più dissolvere più soluto. In questi casi c'è sempre una parte del soluto senza dissolvere. Ad esempio, se aggiungiamo molto sale a un bicchiere con acqua, parte di questo sale non si dissolverà e rimarrà sul fondo del vetro.
- Soluzioni superaturate: Queste sono soluzioni in cui c'è più soluto disciolto di quanto il solvente ammetta. Ciò può essere ottenuto riscaldando una soluzione satura per dissolvere ancora più soluto e quindi lasciando lentamente raffreddamento fino alla temperatura iniziale. Queste soluzioni sono instabili, poiché qualsiasi disturbo come la vibrazione o una piccola particella di polvere sulla superficie può causare la separazione del soluto in eccesso.
Secondo la tua condizione fisica
- Soluzioni liquide: Sono i più comuni. In questo tipo di soluzioni il solvente è un liquido (come acqua, alcol, olio, ecc.) Ma il soluto può essere trovato in qualsiasi stato (solido, liquido o gas). Alcuni esempi di soluzioni liquide sono acqua salata, vino e bevande analcoliche.
- Soluzioni solide: In questi casi, sia il solvente che il soluto sono allo stato solido. Gli esempi più comuni di questo tipo di soluzioni sono leghe metalliche come bronzo, acciaio e ottone, ma ci sono anche altri esempi come il vetro.
- Soluzioni gassose: Come suggerisce il nome, sono miscele omogenee in cui tutti i componenti sono in uno stato gassoso.
Secondo il solvente
- Soluzione acquosa: Se in una soluzione il solvente è acqua, allora si dice che sia una soluzione acquosa. Queste sono le soluzioni più comuni che possono essere trovate nella vita quotidiana.
- Soluzioni alcoliche: Il solvente più comune, dopo l'acqua, è l'alcol. Tra gli alcoli più comuni ci sono metanolo, etanolo e alcol isopropilico.
- Soluzioni in altri solventi organici: Ci sono molti altri composti organici che vengono utilizzati come solventi. Questi includono alcuni alcani, la maggior parte degli eteri, dei chetoni liquidi e altri.
Esempi di soluzioni chimiche
Limonata
È una soluzione acquosa formata dall'acqua come succo di solvente e limone e zucchero come soluti.
Acqua di mare
L'acqua di mare o l'acqua salata è una soluzione acquosa composta da acqua e una miscela di sali. Tra questi sali, quello che è più proporzionale è il cloruro di sodio (NaCl) noto come sale da tavola comune.
Può servirti: ossido di mercurio (HG2O)Sciroppo concentrato
Questa è una soluzione acquosa quasi satura di acqua di zucchero.
Acqua gassata
L'acqua carbonificata, nota anche come soda, è una soluzione acquosa di anidride carbonica gassosa (CO2) In acqua.
Aria
L'aria è una soluzione gassosa in cui l'azoto può essere considerato come solvente e ossigeno e altri gas come soluti.
Burro chiarificato
Mischiando il burro e rimuovi tutta la schiuma, si ottiene una soluzione gialla trasparente chiamata burro chiarificata. Questa è una soluzione in cui sia il solvente che i soluti sono grassi.
Vetro colorato
Il vetro a colori sono soluzioni a stato solido, in cui il solvente è fuso silice e i soluti sono altri minerali che forniscono il vetro il suo colore caratteristico.
Caffè
Questa è una soluzione acquosa complessa che contiene molti soluti (tra cui la caffeina) che danno alla bevanda il suo aroma e il sapore caratteristici.
L'acciaio
L'acciaio è una soluzione in lega o solida formata da ferro metallico e carbonio di grafite.
Plasma del sangue
Il plasma sanguigno è una soluzione ottenuta dopo aver centrifugato il sangue per rimuovere tutte le cellule e altri solidi sospesi. Questa è una soluzione acquosa abbastanza concentrata che contiene centinaia di soluti tra cui carboidrati, aminoacidi, proteine solubili ed elettroliti, tra gli altri.
Riferimenti
- Chang, R. e Goldsby, K. (2014). Chimica. 11 ° ed. New York: McGraw-Hill Education.
- Soluzione (25 gennaio 2021). In Wikipedia.org.
- Brown, t. L., Lemay, e. (2018). Chimica: la scienza centrale. 14a edizione. Pearson.
- Krestonosich, s., e altri. (1992). Soluzioni. Editoriale Miró.
- Vidal, J. A. (Editor) (1997). Mentore interattivo - Enciclopedia tematica studentesca. Editoriale oceanico. Barcellona.

