Saponificazione

- 3765
- 633
- Baldassarre Ross
Spieghiamo cosa è la sponificazione, la sua reazione, perché è importante e diamo diversi esempi
 Saponi artigianali preparati attraverso saponificazione
Saponi artigianali preparati attraverso saponificazione Cos'è la saponificazione?
IL saponificazione È il processo chimico attraverso il quale viene fatto il sapone. In effetti, saponificazione significa letteralmente produzione di sapone. Questo processo è costituito dall'idrolisi alcalina, o in un mezzo fortemente di base, degli esteri di acidi grassi come quelli ottenuti in grassi e oli commestibili.
La saponificazione è conosciuta da secoli. Inizialmente è stato usato per determinare la composizione di alcuni trigliceridi comuni, come Stearin.
Il chimico che ha scoperto la reazione per la prima volta, la usò per dimostrare che Stearin non era davvero altro che l'unione tra un alcol, in questo caso glicerina o glicerolo, con tre molecole di un acido grasso chiamato acido steartico.
Reazione di saponificazione
La saponificazione È una reazione di idrolisi di un estere di acido grasso. Ciò significa che il collegamento estere è rotto (lisi - rompere) per mezzo di azione idrica (Hydro - acqua). Per questo, è richiesto l'uso di una base forte come idrossido di sodio o idrossido di potassio.
Come prodotti, si ottiene un sale acido (che è il sapone stesso) e un alcol, come mostrato di seguito:

Meccanismo di reazione della saponificazione
Il meccanismo di questa reazione è un processo a tre fasi, che inizia con un attacco di ione idrossido, quindi l'eliminazione dell'alcool e infine la formazione di sale.
-
Passaggio 1: attacco di ioni idrossido
Il primo passo e il motivo per cui è necessario aggiungere idrossido di sodio o qualche altra base forte è l'attacco dell'idrossido all'estere:
Può servirti: chitosano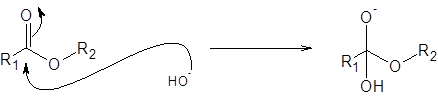
-
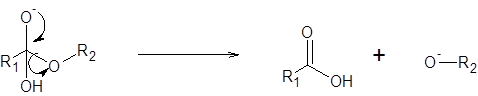
Passaggio 2: eliminazione dell'alcool sotto forma di uno ione alcossido
In questa fase, la coppia di elettroni di ossigeno spinge l'alcol e lo separa dall'estere sotto forma di uno ione alcossido. Questo ione è una base molto forte. Oltre all'alcossido, si forma anche una molecola di acido carbossilico (che è un acido grasso).
-
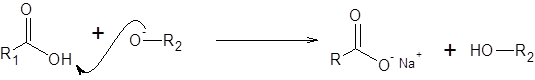
Passaggio 3: Formazione di sale
Lo ione alcossido che si forma nella fase precedente è una base molto forte e rimuove facilmente il protone in acido carbossilico. In tal modo, fa acido.
Trigliceridi
In generale, la reazione di saponificazione viene effettuata con grassi o oli verdure o animali.
 Gli oli vegetali, come l'olio d'oliva, vengono generalmente usati per preparare saponi di saponificazione
Gli oli vegetali, come l'olio d'oliva, vengono generalmente usati per preparare saponi di saponificazione Gli esteri presenti in questi grassi e oli sono quasi sempre trigliceridi o esteri di acidi grassi con un alcol speciale chiamato glicerolo o glicerina.
In questi casi, la reazione di saponificazione è vista come:
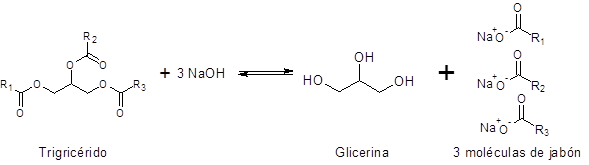
R1, R2 e r3 Rappresentano le catene di acidi grassi. Dato che ci sono molti diversi acidi grassi, la saponificazione può fornire saponi diversi con diversi saponi.
Prodotti di saponificazione
A seconda dell'olio iniziale o del grasso e quale base viene utilizzata, verranno ottenuti saponi con proprietà diverse.
- Per esempio, L'uso di idrossido di sodio o di potassio darà come prodotto un sale di sodio o un sale di potassio (sodio o sapone di potassio). In generale, i saponi di potassio hanno meno punto di fusione del sodio e alcuni sono persino liquidi a temperatura ambiente.
Allo stesso modo, le caratteristiche dell'acido grasso che fa parte dell'estere influenzeranno anche le proprietà del sapone risultante. Più lungo è la catena, maggiore è il suo punto di fusione.
Per questo motivo, quando si desidera preparare i saponi liquidi, ad esempio, gli acidi grassi vengono selezionati con catene più corte e idrolizzati con idrossido di potassio anziché sodio.
Importanza della saponificazione
La saponificazione è una reazione molto importante.
- A livello industriale, è la reazione che viene utilizzata per la produzione di tutti i saponi di pasta, come saponi per manuali o saponi per lavare a barre.
- D'altra parte, viene anche spesso usato come primo passo per ottenere acidi grassi, che vengono quindi utilizzati in un'ampia varietà di settori come la produzione di cosmetici.
- In altri casi, gli acidi grassi sono spesso usati come solventi o agenti sparsi nella produzione di dipinti, sebbene in questi casi sia più comune ottenere oli minerali.
- Inoltre, questa reazione viene utilizzata anche per pulire qualsiasi superficie grassa come l'interno dei forni o la superficie delle cucine.
In quei casi in cui i grassi sono molto vicini alla superficie o sono grassi carbonizzati. In questo modo, il grasso diventa sapone, il sapone si dissolve in acqua e la superficie è pulita.
Può servirti: carbocalizzazione: formazione, caratteristiche, tipi, stabilitàEsempi di reazioni di saponificazione
-
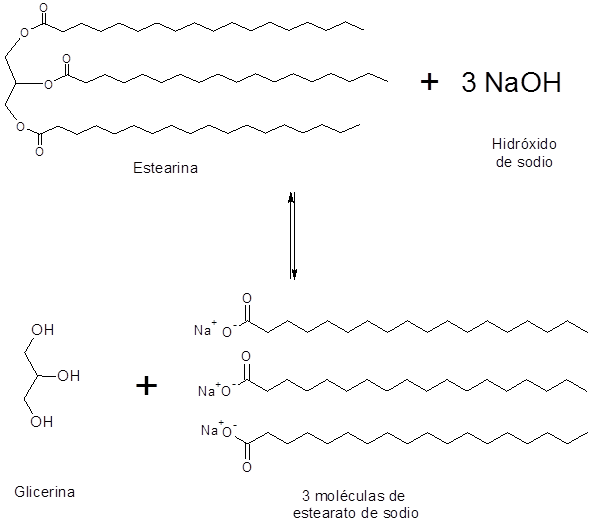
Saponificazione di Stearin
La stearina è un trigliceride che contiene tre molecole di acido stearico legate alla glicerina. La sua saponificazione produce tre molecole di sapone, in questo caso sodio o potassio stearato.
-
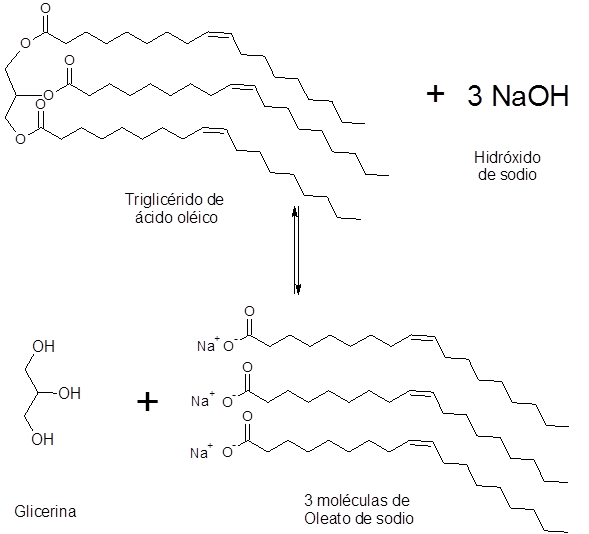
Saponificazione dell'acido oleico
Gli oli di oliva e girasole contengono più dell'80% di acido oleico. Questo è un grasso insaturo che ha 18 catene di carbonio. La saponificazione di questi oli produce, tra le altre cose, olio di sodio.
-
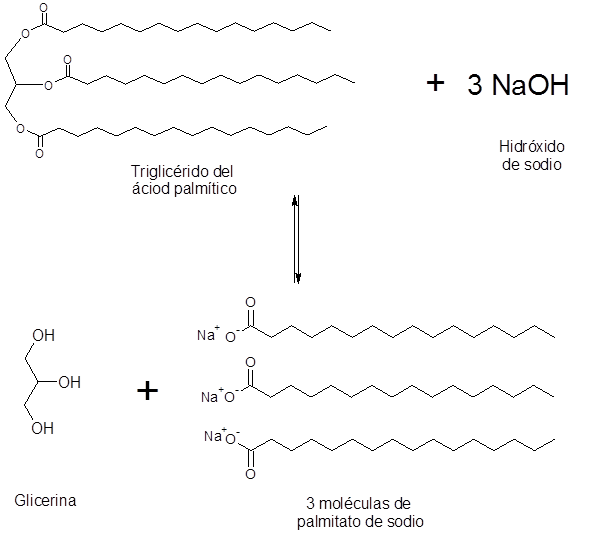
Saponificazione dell'acido palmitico
L'acido palmitico è un acido grasso saturo a lungo termine contenente 16 atomi di carbonio. Questo è l'acido grasso più importante della dieta per essere umani. È il principale acido grasso saturo nel nostro corpo.
Nel cibo, l'acido palmitico è uno dei componenti principali del grasso animale, quindi i saponi preparati da grassi come il burro di bovini, contengono principalmente sodio o potassio palmitato.
Inoltre, l'acido palmitico forma oltre il 40% dell'olio di palma (da cui il suo nome). In effetti, la saponificazione dell'olio di palma è la principale fonte industriale di acido palmitico in tutto il mondo.