Precipitazione chimica

- 3306
- 772
- Rufo Longo
 Serbatoio di sedimentazione per il trattamento dell'acqua
Serbatoio di sedimentazione per il trattamento dell'acqua Qual è la precipitazione chimica?
IL Precipitazione chimica È un processo di trattamento delle acque reflue in cui vengono aggiunte sostanze chimiche per trasformare gli ioni inquinanti disciolti in particelle solide. In altre parole, consiste nel generare particelle sedimentabili nelle acque reflue mediante l'aggiunta di sostanze chimiche.
L'obiettivo principale della pioggia chimica.
Sebbene la maggior parte degli inquinanti che si cercano di eliminare siano metalli come cobalto, cesio o mercurio che formano cationi (ioni con carico positivo), viene anche usato per eliminare gli anioni (ioni con carico negativo) come fluoruro, cianuro e fosfato.
Una volta che i solidi precipitano, è necessario eseguire una serie di passaggi per poterlo separarlo dal resto dell'acqua. Questi passaggi includono flocculazione, sedimentazione e separazione solida-liquido.
L'equilibrio della solubilità e delle precipitazioni chimiche
La tecnica di precipitazione chimica si basa sull'equilibrio di solubilità dei composti ionici e sulla costante del prodotto di solubilità. Nella maggior parte dei casi, i solidi che precipitano sono piccoli idrossidi solubili, sebbene anche altri tipi di ioni siano precipitati.
In tutti i casi di precipitazione chimica, il solido che si forma è un piccolo composto ionico solubile che è in equilibrio con gli ioni in soluzione secondo la reazione generale:
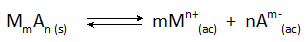
La concentrazione finale del metallo, M, che rimane nella soluzione è determinata dalla costante di equilibrio di questa reazione, nonché dalla concentrazione dell'anione, a, che viene aggiunta.
Per esempio, Se si tratta di un idrossido, la concentrazione finale del metallo dipenderà dalla concentrazione di ioni idrossido nella soluzione e, quindi, del pH.
Processo di precipitazione chimica passo per passo
Il processo di precipitazione chimica è costituito da quattro passaggi di base:
Passaggio 1: aggiunta dell'agente precipitante e regolazione del pH.
Questa è la fase iniziale in cui viene aggiunto l'agente precipitante selezionato (nella maggior parte dei casi è idrossido di calcio). Il pH si regola per massimizzare le precipitazioni e ottimizzare la purezza finale dell'acqua.
Può servirti: acrilonitrilo: struttura, proprietà, produzione, usiDurante questo passaggio, la miscela viene normalmente battuta o agitata per garantire una concentrazione di precipitazione uniforme.
Passaggio 2: floculazione.
Questa fase consente ai piccoli solidi che si formano nella prima fase delle precipitazioni per unirsi a formare particelle o "floc" (da qui il loro nome).
Questi sedimentano più rapidamente nel prossimo passaggio. Per favorire la formazione di queste particelle senza romperle, l'agitazione diventa più lentamente.
Passaggio 3: sedimentazione.
Si consiste nel lasciare che la miscela di acqua appena trattata si alzi in un serbatoio per far andare tutte le particelle solide sullo sfondo (Sedimenta).
Passaggio 4: separazione solida-liquido.
Nella maggior parte dei casi, la separazione solida-liquido consiste in una semplice decantazione dell'acqua che rimane il sedimento. In altri casi, la separazione si ottiene filtrando o persino centrifugare l'acqua trattata, a seconda di quanto siano pericolosi gli inquinanti.
Tipi di precipitazioni chimiche
Precipitazione idrossido
Questo è il tipo più comune di precipitazioni chimiche e consiste nell'aumentare il pH aggiungendo un composto alcalino che è quasi sempre idrossido di calcio (CA (OH)2).
La reazione chimica che si verifica è:

Nella reazione precedente, M rappresenta qualsiasi catione del metallo che si desidera per eliminare. Il solido che si forma in questo caso è un idrossido molto piccolo solubile.
Nel caso della precipitazione dell'idrossido, la regola generale è che maggiore è la concentrazione di OH- (Maggiore è il pH), minore è la concentrazione del metallo che rimane nell'acqua, dopo il trattamento. In altre parole, a maggiore pH, maggiore purezza finale dell'acqua.
Precipitazione con solfuri
Questo tipo di precipitazione chimica viene utilizzato principalmente per l'eliminazione di metalli pesanti, come il piombo o il mercurio, sotto forma di solfuri solubili molto ridotti. Per raggiungere questo obiettivo, può essere aggiunto all'acqua per trattare sia solfuri solubili che insolubili.
I solfuri più comunemente usati sono solubili che includono idrogeno solforato (H2S) e solfuro di sodio (NA2S). La reazione di precipitazione generale è:
Può servirti: lega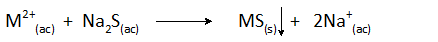
Il solfuro ferroso può anche essere aggiunto che è insolubile, ma fornisce abbastanza ioni solfuri alla soluzione per precipitare la maggior parte dei metalli pesanti.
Precipitazione carbonatica
I carbonati di molti metalli sono meno solubili anche degli idrossidi e possono precipitare dalle acque reflue aggiungendo carbonato di calcio o trasformando idrossidi che gorgogliano l'anidride carbonica nella miscela alcalinizzata nella miscela alcalizzata.
Precipitazione di cianuro
A differenza dei casi precedenti, qui cerchiamo di precipitare il cianuro, che è un anione, anziché un metallo. Il cianuro è un contaminante velenoso molto pericoloso e può essere rimosso dalle acque reflue aggiungendo solfato di zinco o solfato ferroso, poiché si forma complessa con questi metalli che precipitano.
Coprecipitazione
La coprecipitazione si verifica quando un soluto precipita insieme a un altro. In questi casi, il primo soluto viene catturato nel solido quando si forma un precipitato di un altro composto.
È come se il solido quando si forma lasciasse il primo soluto e lo trascinasse fuori dalla soluzione. Questo fenomeno viene usato per eliminare alcuni inquinanti che sono difficili da precipitare.
Applicazioni
Le precipitazioni chimiche vengono utilizzate in settori infiniti al fine di soddisfare i requisiti ambientali della qualità delle acque reflue.
Precipitazione idrossido È usato nelle industrie di:
- Finiture metalliche
- Produzione composta inorganica
- Fondazioni
- Produzione di fuochi d'artificio ed esplosivi
- Smalto in porcellana
- Estrazione del carbone
- L'industria farmaceutica, tra gli altri.
D'altra parte, Precipitazione con solfuri È usato nel settore per eliminare i contaminanti come mercurio, piombo e argento. Questo ha applicazione nei seguenti settori:
- Industria tessile
- Estrazione
- Attrezzatura fotografica e forniture
- Produzione di metalli non ferrosi, tra gli altri
Oltre a queste industrie, le precipitazioni sono la tecnica più importante per Purificazione dell'acqua di raffreddamento dei reattori nucleari. In questo settore, viene utilizzato per eliminare i cationi radioattivi come Plutonio, Américo, Cesio e altri.
Esempi di precipitazione chimica
Precipitazione dello stronzio con carbonato di calcio
La reazione di precipitazione in questo caso è:
Può servirti: ossidi di azoto (NOX)
La reazione viene effettuata a un pH ottimale di 10,5 e raggiunge le concentrazioni di questo metallo fino a 100 volte inferiore rispetto al iniziale.
Precipitazione di idrossido di antimonio
Per eliminare l'antimonio dalle acque reflue, l'idrossido di titanio può essere usato come reagente precipitante. La reazione è:

Questo viene effettuato in un intervallo di pH che va da 5 a 8,5 e riduce anche la concentrazione a un valore 100 volte inferiore al iniziale.
Precipitazione di cesio con tetrafenilborate
Questo è un caso speciale che consente le precipitazioni di cessium, un metallo alcalino difficile da precipitare. La reazione è:

L'uso del tetrafenilborarato offre due grandi benefici: in primo luogo, che funziona praticamente a qualsiasi pH (da pH 1 a 13) e in secondo.
Precipitazione in rame con solfuro di sodio
La reazione di precipitazione in questo caso è:
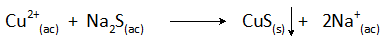
La rimozione del rame delle acque reflue con questo metodo viene eseguita a valori di pH superiori a 8 e la sua concentrazione è ridotta di oltre il 99%.
Coprecipitazione di cromo, piombo e zinco con idrossido ferrico e idrossido di alluminio
In questo caso, l'idrossido di sodio viene aggiunto all'acqua per precipitare ferro e alluminio presenti sotto forma di idrossido ferrico (fede (OH)3) e idrossido di alluminio (al (OH)3). Quando questi due idrossidi precipitano, trascinano parte di ioni cromati, piombo e zinco. Il trattamento posteriore con idrogeno solforato rimuove quasi tutti questi tre metalli.
Riferimenti
- Wang, l. K., Vaccari, d. A., Li, e., & Shammas, n. K. (2005). Precipitazione chimica. Processi di trattamento fisichemico, 141-197. Doi: 10.1385/1-59259-820-X: 141
- Striebig, b.A. (2005). Precipitazione chimica. In Water Enciclopedia (eds. J.H. Lehr e J. Keeley). https: // doi.org/10.1002/047147844X.PC101
- Britannica, t. EDITRI DE ENCYCLOPAEDIA (2018, 8 febbraio). Precipitazione chimica. Britannica Enciclopedia. https: // www.Britannica.com/scienza/pre-precipitazione
- D. Bhattacharyya, a. B. JUMAWAN JR. & R. B. Grieves (1979) Separazione di metalli pesanti tossici da parte del solfuro, scienza della separazione e tecnologia, 14: 5, 441-452, doi: 10.1080/01496397908058096
- Marina Maya Marchioretto, Harry Bruning & Wim Rulkens (2005) Precisione dei metalli pesanti nei fanghi di depurazione, Scienze di separazione e tecnologia, 40:16, 3393-3405, doi: 10: 10.1080/01496390500423748

