Struttura, Proprietà, Ottenimento, Ottenimento, Ottenimento, Ottenimento
- 4740
- 260
- Zelida Gatti
Lui Nitruro di boro È un solido inorganico formato dall'unione di un atomo di boro (B) con un atomo di azoto (N). La sua formula chimica è BN. È un solido bianco molto resistente alle alte temperature ed è un buon conducente di calore. Viene utilizzato ad esempio per produrre crosol di laboratorio.
Boro nitruro (bn) è resistente a molti acidi, tuttavia ha un po 'di debolezza per gli attacchi di acido fluoruro e le basi fuse. È un buon isolante per elettricità.
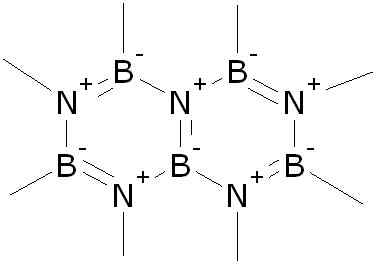
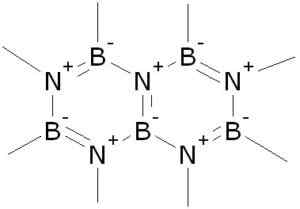 Struttura a nitruro di boro (BN). Akeramop [dominio pubblico]. Fonte: Wikimedia Commons.
Struttura a nitruro di boro (BN). Akeramop [dominio pubblico]. Fonte: Wikimedia Commons. È ottenuto in varie strutture cristalline, di cui le più importanti sono esagonali e cubiche. La struttura esagonale ricorda la grafite ed è scivolosa, quindi è usata come lubrificante.
La struttura cubica è quasi dura quanto il diamante e viene utilizzata per produrre utensili da taglio e per migliorare la durezza di altri materiali.
Con nitruro di boro è possibile produrre tubi microscopici (estremamente sottili) chiamati nanotubi, che hanno applicazioni mediche, come per il trasporto all'interno del corpo e rilasciare medicinali contro i tumori del cancro.
[TOC]
Struttura
Boro nitruro (BN) è un composto in cui gli atomi di boro e azoto sono collegati in modo covalente con un triplo collegamento.
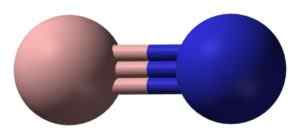 Una molecola di nitruro di boro isolato ha un atomo di azoto azotato unito da un triplo legame. Benjah-BMM27 [dominio pubblico]. Fonte: Wikimedia Commons.
Una molecola di nitruro di boro isolato ha un atomo di azoto azotato unito da un triplo legame. Benjah-BMM27 [dominio pubblico]. Fonte: Wikimedia Commons. In fase solida il BN è formato da un numero uguale di atomi di boro e azoto sotto forma di 6 membri.
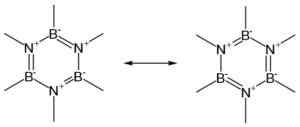 Strutture di risonanza di un anello BN. Autore: Teacher. Fonte: Wikimedia Commons.
Strutture di risonanza di un anello BN. Autore: Teacher. Fonte: Wikimedia Commons. BN esiste in quattro forme cristalline: esagonale (H-BN) simile alla grafite, cubica (C-BN) simile a Diamond, Rhomboédica (R-BN) e Wurtzita (W-BN).
La struttura dell'H-BN è simile a quella della grafite, cioè ha piani di anelli esagonali che hanno atomi di boro e azoto che si alternano.
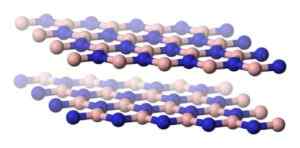 Struttura sotto forma di piani separati di nitruro di boro esagonale. Benjah-BMM27 [dominio pubblico]. Fonte: Wikimedia Commons.
Struttura sotto forma di piani separati di nitruro di boro esagonale. Benjah-BMM27 [dominio pubblico]. Fonte: Wikimedia Commons. Tra gli aerei H-BN c'è una grande distanza che suggerisce di essere uniti solo attraverso le forze di van der Waals, che sono forze di attrazione molto deboli e i piani possono facilmente scivolare l'uno sull'altro.
Può servirti: solePer questo motivo, l'H-BN non è valido al tatto.
La struttura del Bn C-BN cubico è simile al diamante.
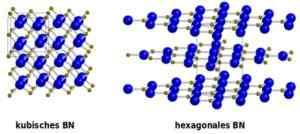 Confronto tra nitruro cubico (a sinistra) ed esagonale (a destra). Da: Benutzer: Oddball, versione vettoriale di Chris 論 [dominio pubblico]. Fonte: Wikimedia Commons.
Confronto tra nitruro cubico (a sinistra) ed esagonale (a destra). Da: Benutzer: Oddball, versione vettoriale di Chris 論 [dominio pubblico]. Fonte: Wikimedia Commons. Nomenclatura
Nitruro di boro
Proprietà
Stato fisico
Solido bianco grasso o scivoloso da toccare.
Peso molecolare
24,82 g/mol
Punto di fusione
Sublima a circa 3000 ° C.
Densità
Esagonale BN = 2,25 g/cm3
BN cubico = 3,47 g/cm3
Solubilità
Leggermente solubile in alcol caldo.
Proprietà chimiche
A causa del forte legame tra azoto e boro (triplo legame) il nitruro di boro ha un'alta resistenza all'attacco chimico ed è molto stabile.
È insolubile in acidi come l'acido cloridrico HCl, l'acido nitrico HNO3 e acido solforico H2SW4. Ma è solubile in basi fusa come idrossido di litio Lioh, idrossido di potassio KOH e idrossido di naoh sodio.
Non reagisce con la maggior parte dei metalli, vetro o sali. A volte reagisce con l'acido fosforico H3Po4. Puoi resistere all'ossidazione ad alte temperature. BN è stabile in aria ma l'acqua si idrolizza lentamente.
BN viene attaccato dal gas fluoro F2 e dall'acido fluorhorico HF.
Altre proprietà fisiche
Ha un'elevata conduttività termica, un'elevata stabilità termica e un'elevata resistività elettrica, cioè è un buon isolatore di elettricità. Ha una superficie alta.
H-BN (BN esagonale) è un solido untutuoso touch, simile alla grafite.
Quando si riscuote l'H-BN ad alta temperatura e la pressione diventa la forma cubica C-BN che è estremamente dura. Secondo alcune fonti, è in grado di graffiare il diamante.
I materiali a base di BN hanno una capacità di assorbimento di inquinanti inorganici (come ioni di metalli pesanti) e inquinanti organici (come coloranti e molecole).
Sorción significa che interagisce con loro e può assorbirli o assorbirli.
Ottenimento
La polvere di H-BN viene preparata per reazione tra bioxido di boro B2O3 o acido borico h3Bo3 Con Ammonia NH3 o con urea NH2(CO) NH2 sotto l'atmosfera di azoto n2.
Può servirti: Monte Olympus (Marte)BN può anche essere ottenuto reagendo il boro con ammoniaca a una temperatura molto elevata.
Un altro modo per prepararlo è da Diborano B2H6 e ammoniaca NH3 Usando un gas inerte e temperature elevate (600-1080 ° C):
B2H6 + 2 NH3 → 2 bn + 6 h2
Applicazioni
L'H-BN (boro esagonale Nituro) ha una varietà di applicazioni importanti basate sulle sue proprietà:
-Come lubrificante solido
-Come additivo per i cosmetici
-In isolanti elettrici ad alta temperatura
-Nei crogioli e nei vasi di reazione
-In stampi e contenitori di evaporazione
-Per la conservazione dell'idrogeno
-Sulla catalisi
-Per adsorb inquinanti delle acque reflue
Nitruro di boro cubico (C-BN) per la sua durezza quasi uguale a quello del diamante viene utilizzato:
-Negli utensili da taglio per la lavorazione di materiali ferrosi duri, come leghe in acciaio duro, ghisa e acciai per utensili
-Per migliorare la durezza e la resistenza all'usura di altri materiali duri come alcune ceramiche per gli utensili da taglio.
 Alcuni utensili da taglio possono contenere nitruro di boro per mostrare una maggiore durezza. Autore: Michael Schwarzenberger. Fonte: Pixabay.
Alcuni utensili da taglio possono contenere nitruro di boro per mostrare una maggiore durezza. Autore: Michael Schwarzenberger. Fonte: Pixabay. - Usi di film sottili di BN
Sono molto utili nella tecnologia dei dispositivi a semiconduttore, che sono componenti di apparecchiature elettroniche. Servono per esempio:
-Produrre diodi piatti; I diodi sono dispositivi che consentono la circolazione dell'elettricità in un certo senso
-Nei diodi di memoria da metallo a semiconduttore, come al-bn-sio2-Sì
-Nei circuiti integrati come limitatore di tensione
-Per aumentare la durezza di determinati materiali
-Per proteggere alcuni materiali di ossidazione
-Per aumentare la stabilità chimica e l'isolamento elettrico di molti tipi di dispositivi
-In condensatore a film sottile
 Alcuni diodi e condensatori possono contenere nitruro di boro. Autore: Sinisa Maric. Fonte: Pixabay.
Alcuni diodi e condensatori possono contenere nitruro di boro. Autore: Sinisa Maric. Fonte: Pixabay. - Usi dei nanotubi BN
I nanotubi sono strutture che a livello molecolare sono a forma di tubi. Sono tubi così piccoli da poter essere visti solo con microscopi speciali.
Di seguito sono riportate alcune delle caratteristiche dei nanotubi BN:
-Hanno un'alta idrofobicità, cioè respingono l'acqua
-Hanno un'alta resistenza all'ossidazione e al calore (l'ossidazione può resistere a 1000 ° C)
-Mostrano un'alta capacità di stoccaggio dell'idrogeno
-Assorbono le radiazioni
-Sono ottimi isolanti di elettricità
Può servirti: termometro di resistenza: caratteristiche, funzionamento, usi-Hanno un'alta conduttività termica
-La sua eccellente resistenza alle alte temperature l'ossidazione significa che possono essere utilizzate per aumentare la stabilità all'ossidazione della superficie.
-A causa della loro idrofobicità possono essere usati per preparare superfici super idrofobiche, cioè non hanno affinità per l'acqua e l'acqua non le penetra.
-I nanotubi BN migliorano le proprietà di alcuni materiali, ad esempio, è stato utilizzato per aumentare la durezza e la resistenza alla frattura del vetro.
 Nibos di nitruro di boro osservato con un microscopio. Keun il suo Kim et al. [CC per 4.0 (https: // creativeCommons.Org/licenze/by/4.0)]. Fonte: Wikimedia Commons.
Nibos di nitruro di boro osservato con un microscopio. Keun il suo Kim et al. [CC per 4.0 (https: // creativeCommons.Org/licenze/by/4.0)]. Fonte: Wikimedia Commons. In applicazioni mediche
I nanotubi di BN sono stati testati come portatori di medicina per il cancro come la doxorubicina. Alcune composizioni con questi materiali hanno aumentato l'efficienza della chemioterapia con detto farmaco.
In diverse esperienze è stato dimostrato che i nanotubi BN hanno il potenziale per trasportare nuovi farmaci e rilasciarli correttamente.
L'uso di nanotubi BN nei biomateriali polimerici è stato studiato per aumentare la loro durezza, degradazione e velocità di durata. Questi sono materiali che vengono utilizzati ad esempio negli impianti ortopedici.
Come sensori
I nanotubi BN sono stati usati per costruire nuovi dispositivi per rilevare l'umidità, l'anidride carbonica2 e per le diagnosi cliniche. Questi sensori hanno dimostrato una risposta rapida e un breve periodo di recupero.
Possibile tossicità dei materiali BN
C'è qualche preoccupazione per i possibili effetti tossici dei nanotubi BN. Non esiste un chiaro consenso sulla sua citotossicità, perché alcuni studi indicano che sono tossici per le cellule, mentre altri indicano il contrario.
Ciò è dovuto alla sua idrofobicità o insolubilità in acqua, poiché rende difficile condurre studi sui materiali biologici.
Alcuni ricercatori hanno coperto la superficie dei nanotubi BN con altri composti che favoriscono la loro solubilità in acqua, ma ciò ha aggiunto una maggiore incertezza nelle esperienze.
Sebbene la maggior parte degli studi indichi che il loro livello di tossicità è basso, si stima che debbano essere condotte ricerche più precise.
Riferimenti
- Xiong, J. et al. (2020). Nitruro di boro esagonale adsorbente: sintesi, sartoria e applicazioni. Journal of Energy Chemistry 40 (2020) 99-111. Recuperato dal lettore.Elsevier.com.
- Mukasyan, a.S. (2017). Nitruro di boro. In un'enciclopedia concisa della sintesi ad alta temperatura autopropagata. Recuperato da ScienceDirect.com.
- Kalay, s. et al. (2015). Sintesi di nanotubi di nitruro di boro e loro applicazioni. Beilstein J. Nanotechnol. 2015, 6, 84-102. NCBI recuperato.Nlm.NIH.Gov.
- Arya, s.P.S. (1988). Preparazione, proprietà e applicazioni dei film sottili di nitruro di boro. Films solido sottile, 157 (1988) 267-282. Recuperato da ScienceDirect.com.
- Zhang, j. et al. (2014). Compositi a matrice ceramica contenente nitruro di boro cubico compositi per utensili da taglio. In progressi nei compositi a matrice ceramica. Recuperato da ScienceDirect.com.
- Cotone, f. Albert e Wilkinson, Geoffrey. (1980). Chimica inorganica avanzata. Quarta edizione. John Wiley & Sons.
- Suanarsan, v. (2017). Materiali per ambiente chimico ostile. Nei materiali in condizioni estreme. Recuperato da ScienceDirect.com
- Dean, J.A. (Editor) (1973). Manuale di chimica di Lange. McGraw-Hill Company.
- Mahan, b.H. (1968). Chimica universitaria. Inter -American Educational Fund, s.A.

