Broglie Atomic Model
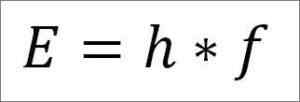
- 2934
- 529
- Enzo De Angelis
Lui Broglie Atomic Model Fu proposto dal fisico francese Louis Broglie nel 1924. Nella sua tesi di dottorato, Broglie ha affermato che la dualità di particelle d'onda degli elettroni, gettando le basi della meccanica ondulata. Broglie ha pubblicato importanti risultati teorici sulla natura delle onde-corpusculus.
Successivamente le dichiarazioni di Broglie sono state dimostrate sperimentalmente dagli scienziati Clinton Davisson e Lester Germer, nel 1927. La teoria delle onde degli elettroni Broglie si basa sulla proposta di Einstein sulle proprietà ondulatori della luce in lunghezze d'onda corte.
 Louis Broglie
Louis Broglie Broglie ha annunciato la possibilità che la materia avesse un comportamento simile a quello della luce e ha suggerito proprietà simili in particelle subatomiche come gli elettroni.
I carichi elettrici e di orbita limitano l'ampiezza, la lunghezza e la frequenza dell'onda descritta dagli elettroni. Broglie ha spiegato il movimento di elettroni attorno al nucleo atomico.
[TOC]
Caratteristiche del modello atomico di Broglie
Per sviluppare la loro proposta, Broglie ha iniziato dal principio secondo cui gli elettroni avevano una doppia natura tra onda e particelle, simile alla luce.
In questo senso, Broglie fece una similitudine tra i due fenomeni e basata sulle equazioni sviluppate da Einstein per lo studio della natura ondulata della luce, disse quanto segue:
- L'energia totale del fotone e, di conseguenza, l'energia totale dell'elettrone, deriva dal prodotto della frequenza d'onda e dalla costante della tavola (6.62606957 (29) × 10 -3. 4 Jules x secondi), come dettagliato nella seguente espressione:
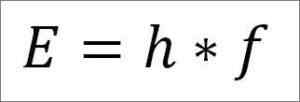
In questa espressione:
E = energia elettronica.
H = costante della tavola.
F = frequenza d'onda.
- Il momento lineare del fotone, e quindi, dell'elettrone, è inversamente proporzionale alla lunghezza dell'onda, ed entrambe le magnitudini sono correlate attraverso la costante della tavola:
Può servirti: osmosi inversa: come funziona, a cosa serve, esempi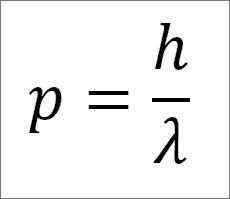
In questa espressione:
P = momento lineare dell'elettrone.
H = costante della tavola.
λ = lunghezza d'onda.
- Il momento lineare è il prodotto della massa della particella a causa della velocità che ha detto la particella durante il suo spostamento.
Se la precedente espressione matematica viene ristrutturata a seconda della lunghezza d'onda, quanto segue è:
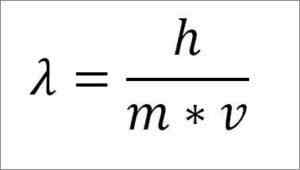
In quella espressione:
λ = lunghezza d'onda.
H = costante della tavola.
M = massa elettronica.
V = velocità elettronica.
Poiché H, la costante della tavola, ha un piccolo valore, la lunghezza d'onda λ è anche. Di conseguenza, è possibile affermare che le proprietà d'onda dell'elettrone sono presentate solo a livello atomico e subatomico.
- Broglie si basa anche sui postulati del modello atomico Bohr. Secondo quest'ultimo, le orbite degli elettroni sono limitate e possono essere solo multipli di numeri interi. COSÌ:
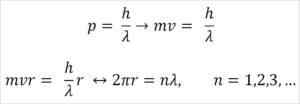
Dove:
λ = lunghezza d'onda.
H = costante della tavola.
M = massa elettronica.
V = velocità elettronica.
R = raggio dell'orbita.
N = numero intero.
Secondo il modello atomico di Bohr, a cui Broglie ha adottato come base, se gli elettroni si comportano come onde stazionarie, le uniche orbite consentite sono quelle il cui raggio è uguale a un intero multiplo della lunghezza d'onda λ.
Pertanto, non tutte le orbite sono conformi ai parametri necessari per un elettrone da mobilitare attraverso questi. Ecco perché gli elettroni possono muoversi solo in orbite specifiche.
La teoria delle onde degli elettroni di Broglie ha giustificato il successo del modello atomico di Bohr per spiegare il comportamento un unico elettronico dell'atomo di idrogeno.
Può servirti: batteria a seccoAllo stesso modo, ha anche dato le luci sul perché questo modello non si è adattato a sistemi più complessi, cioè atomi con più di un elettrone.
Esperimento di Davisson e Germer
Il controllo sperimentale del modello atomico di Broglie ebbe luogo 3 anni dopo la sua pubblicazione, nel 1927.
I principali fisici statunitensi Clinton J. Davisson e Lester Germer hanno confermato sperimentalmente la teoria della meccanica ondulata.
Davisson e Germer hanno eseguito test di dispersione di un raggio di elettroni attraverso un cristallo di nichel e hanno osservato il fenomeno della diffrazione attraverso l'ambiente metallico.
L'esperimento effettuato consisteva nell'esecuzione della seguente procedura:
- In primo luogo, è stato posizionato un gruppo con fascio di elettroni che aveva un'energia iniziale nota.
- È stata installata una fonte di tensione per accelerare il movimento dell'elettrone incitando una differenza potenziale.
- È stato diretto il flusso del raggio di elettroni su un vetro metallico; In questo caso, nichel.
- È stato misurato il numero di elettroni che colpiscono il vetro di nichel.
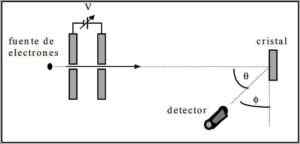
Alla fine della sperimentazione, Davisson e Germer hanno rilevato che gli elettroni si sono dispersi in diverse direzioni.
Quando si ripete l'esperimento usando cristalli di metallo con orientamenti diversi, gli scienziati hanno rilevato quanto segue:
- La dispersione del fascio di elettroni attraverso il vetro metallico era paragonabile al fenomeno dell'interferenza e alla diffrazione dei raggi di luce.
- Il riflesso degli elettroni sull'impatto del vetro ha descritto la traiettoria che, teoricamente, dovrebbe descrivere secondo la teoria delle onde di elettroni di Broglie.
In breve, l'esperimento di Davisson e Germer ha dimostrato sperimentalmente la natura a doppia particella d'onda degli elettroni.
Può servirti: collegamento covalente polare: caratteristiche ed esempiLimitazioni
Il modello atomico di Broglie non prevede la posizione esatta dell'elettrone sull'orbita in cui si muove.
In questo modello, gli elettroni sono percepiti come onde mobilitate in tutta l'orbita senza una posizione specifica, che introduce il concetto di orbitale elettronico.

Inoltre, il modello atomico di Broglie, analogo al modello di Schrödinger, non considera la rotazione degli elettroni sullo stesso asse (rotazione).
Ignorando il momento angolare intrinseco degli elettroni, le variazioni spaziali di queste particelle subatomiche vengono lasciate da parte.
Nello stesso ordine di idee, questo modello non tiene conto dei cambiamenti nel comportamento degli elettroni veloci a seguito degli effetti relativistici.
Articoli di interesse
Modello atomico di Schrödinger.
Modello atomico di Chadwick.
Modello atomico Heisenberg.
Modello atomico Perrin.
Modello atomico Thomson.
Modello atomico Dalton.
Modello atomico di Dirac Jordan.
Modello atomico di Democrito.
Modello atomico Leucipo.
Modello atomico Bohr.
Modello atomico attuale.
Riferimenti
- La teoria quantistica di Bohr e le onde (s Broglie.F.). Recuperato da: NE.Phys.Kyushu-u.AC.J
- Louis de Broglie - Biographical (1929). © The Nobel Foundation. Recuperato da: Nobelprize.org
- Louis-Victor de Broglie (s.F.). Estratto da: Cheded.Chimica.Purdue.Edu
- Lovett, b. (1998). Louis de Broglie. Encyclopædia Britannica, Inc. Recuperato da: Britannica.com
- Modello atomico de broglie. National University of Distance Education. Spagna. Recuperato da: OCW.Innova.Und.È
- Louis de Broglie.F.). Recuperato da: Hiru.EUS
- Von Pamel, o., E Marchisio, s. (S.F.). Meccanica quantistica. Università nazionale di Rosario. Recuperato da: fceia.a r.Edu.ar

