Struttura metossietanica, proprietà, ottenimento, usi, rischi
- 1408
- 56
- Lidia Valentini
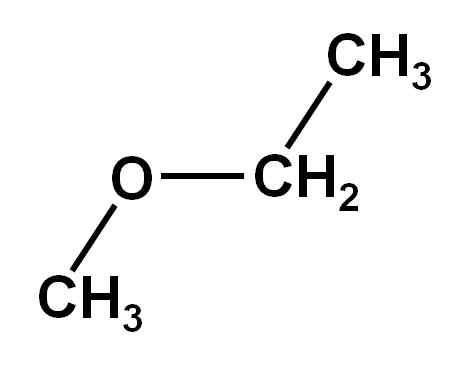
Lui Metossyetan È un composto organico della famiglia di eteri o alcossidi. La sua formula chimica è Cho3Och2Cap3. È anche chiamato metil etil etere o etil metil etere. È un composto gassoso a temperatura ambiente e la sua molecola presenta due gruppi metil -CH3, uno attaccato direttamente all'ossigeno e l'altro appartenente a etil -ch2Cap3.
Metoxietano è un gas incolore, solubile in acqua e miscibile con alcol eterico e alcol. Essere un etere è un piccolo composto reattivo, tuttavia può reagire ad alte temperature con alcuni acidi concentrati.
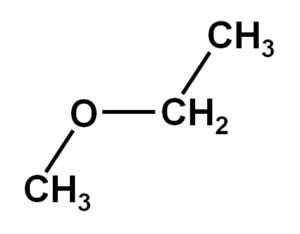 Etere metoxietano o metilico. Autore: Marilú Stea
Etere metoxietano o metilico. Autore: Marilú Stea È generalmente ottenuto dalla sintesi di Williamson così chiamata, che include l'uso di un alcossido di sodio e uno ioduro alchilico. A sua volta, la sua decomposizione è stata studiata in diverse condizioni.
Metoxietano è usato nei laboratori di ricerca con vari obiettivi, ad esempio nello studio dei nanomateriali a semiconduttore o nell'osservazione della materia interstellare nelle costellazioni e nelle grandi nuvole molecolari dell'universo.
In effetti, grazie a telescopi molto sensibili (interferometri) è stato rilevato in alcuni luoghi di spazio interstellare.
[TOC]
Struttura
Il composto metossietano ha un gruppo metilico -CH3 e un gruppo etilico -CH2Cap3 entrambi attaccati a un ossigeno.
Come si può vedere, in questa molecola ci sono due gruppi metilici, uno attaccato all'ossigeno Cho3-O e l'altro appartenente a etil -ch2-Cap3.
Nello stato fondamentale o inferiore dell'energia il gruppo metilico di -CH2-Cap3 è in posizione trans Per quanto riguarda il metile ad attacco di ossigeno, cioè in un luogo diametralmente opposto, prendendo come riferimento al collegamento CHO2-O. Ecco perché a volte viene chiamato trans-Etere etil metil.
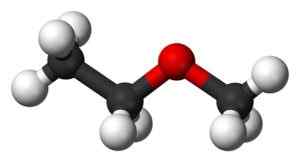 Struttura trans-etil metil etere in 3D. Nero: carbonio. Bianco: idrogeno. Rosso: ossigeno. Il legame tra ossigeno e -ch2- può girare, nel qual caso i due -C3 Sarebbero più vicini l'uno all'altro. Ben Mills e Jynto [dominio pubblico]. Fonte: Wikipedia Commons.
Struttura trans-etil metil etere in 3D. Nero: carbonio. Bianco: idrogeno. Rosso: ossigeno. Il legame tra ossigeno e -ch2- può girare, nel qual caso i due -C3 Sarebbero più vicini l'uno all'altro. Ben Mills e Jynto [dominio pubblico]. Fonte: Wikipedia Commons. Questa molecola può sperimentare torsione nel collegamento CHO2-O, che colloca il metil in una posizione spaziale diversa da trans , Gruppi metil -ch3 Sono molto vicini l'uno all'altro e questa torsione genera una transizione di energia rilevabile da strumenti sensibili.
Può servirti: coulombimetria: fondamentali, tipi, applicazioniNomenclatura
- Metossyetan.
- Ether di metil ether.
- trans-Ethel Ether (principalmente nella letteratura di lingua inglese, traduzione inglese trans-Etere etil metil).
Proprietà fisiche
Stato fisico
Gas incolore
Peso molecolare
60.096 g/mol
Punto di fusione
-113,0 ºC
Punto di ebollizione
7,4 ºC
Punto d'infiammabilità
1,7 ºC (metodo di coppa chiusa).
Temperatura di auto-direzione
190 ºC
Peso specifico
0,7251 a 0 ºC/0 ºC (è meno denso dell'acqua ma più pesante dell'aria).
Indice di rifrazione
1.3420 a 4 ° C
Solubilità
Solubile in acqua: 0,83 moli/l
Solubile in acetone. Miscible di alcol etilico ed etere etilico.
Proprietà chimiche
Metoxietano è un etere, quindi è relativamente piccolo reattivo. L'Unione carbonio-ossigeno-carbonio C-O-C è molto stabile di fronte alle basi, agenti ossidanti e riduttori. Produce solo il suo degrado acido, ma procede solo in condizioni vigorose, cioè con acidi concentrati e alte temperature.
Tuttavia, tende a ossidarsi in presenza di aria che forma perossidi instabili. Se i contenitori che lo contengono per calore o fuoco sono esposti, i contenitori sfruttano violentemente.
Decomposizione del calore
Quando il metossietan viene sottoposto al riscaldamento tra 450 e 550 ° C viene suddiviso in acetaldeide, etano e metano. Questa reazione è catalizzata dalla presenza di ioduro di etil, che è generalmente presente nei campioni di metossietano di laboratorio perché viene utilizzato nell'ottenimento.
Decomposizione fotosensibilizzata
Il metoxietano irradiato con una lampada a vapore di mercurio (lunghezza d'onda di 2537 Å) si decompone generando un'ampia varietà di composti tra cui si distinguono: idrogeno, 2.3-dimetoxibtano, 1-etossi-2-metaxipropano e metil vinile etere etere etere etere.
I prodotti finali dipendono dal tempo di irradiazione del campione, poiché continuando l'irradiazione che inizialmente formano nuovi composti.
Prolungando il tempo di irradiazione, possono anche formare: propano, metanolo, etanolo, acetone, 2-butanone, monossido di carbonio, etil-n-pro-propil etere e etere metil-sec-bitile.
Ottenimento
Poiché è un etere non simmetrico, il metossietano può essere ottenuto dalla reazione tra metossido di sodio CH3Ona e lo Yoduro de Etilo ch3Cap2Yo. Questo tipo di reazioni si chiama sintesi di Williamson.
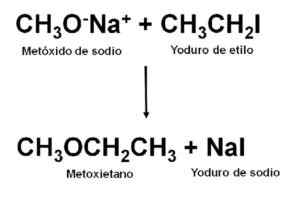 Ottenere Metoxietano attraverso la sintesi di Williamson. Autore: Marilú Stea.
Ottenere Metoxietano attraverso la sintesi di Williamson. Autore: Marilú Stea. Una volta effettuata la reazione, la miscela viene distillata per ottenere l'etere.
Può servirti: composti ternari: caratteristiche, formazione, esempiPuò anche essere ottenuto usando il sodio etossido CH3Cap2Ona e metil solfato (CH3)2SW4.
Posizione nell'universo
Lui trans-L'ether etere di etil è stato rilevato nella metà interstellare in regioni come la costellazione di Orion KL e nella gigantesca nuvola molecolare W51E2.
 Costellazione di orione dove si osservano le nuvole molecolari. Rogelio Bernal Andreo [CC BY-SA 3.0 (https: // creativeCommons.Org/licenze/by-sa/3.0)]. Fonte: Wikipedia Commons.
Costellazione di orione dove si osservano le nuvole molecolari. Rogelio Bernal Andreo [CC BY-SA 3.0 (https: // creativeCommons.Org/licenze/by-sa/3.0)]. Fonte: Wikipedia Commons. Il rilevamento di questo composto nello spazio interstellare insieme all'analisi della sua abbondanza è utile per la costruzione di modelli di chimica interstellare.
Uso del metossyetan
L'etere metoxietano o metil etere è utilizzato principalmente nelle esperienze di laboratorio per la ricerca scientifica.
Per studi sulla materia interstellare
Essendo una molecola organica con rotazioni interne, Metoxietano è un composto chimico di interesse per gli studi sulla materia interstellare.
Le rotazioni interne dei loro gruppi metilici producono transizioni energetiche nella regione a microonde.
Pertanto, possono essere rilevati da telescopi altamente sensibili come il grande millimetro/set submilimetrico di Atacama o Soul (acronimo di inglese Atacama Large millimetro/Submillimeter Array).
 Aspetto di una parte del grande osservatorio astronomico di Alma. ESO/José Francisco Salgado (Josefrancisco.org) [cc di 4.0 (https: // creativeCommons.Org/licenze/by/4.0)]. Fonte: Wikipedia Commons.
Aspetto di una parte del grande osservatorio astronomico di Alma. ESO/José Francisco Salgado (Josefrancisco.org) [cc di 4.0 (https: // creativeCommons.Org/licenze/by/4.0)]. Fonte: Wikipedia Commons. Grazie alla sua rotazione interna e ai grandi osservatori spaziali il trans-L'etere di metil ether è stato trovato nella costellazione di Orione e nella nuvola molecolare gigante W51E2.
Per dedurre le trasformazioni chimiche in vari campi di studio
Alcuni ricercatori hanno osservato la formazione di metossietano o metil etil etere quando una miscela di etilene CH è irradiata con elettroni2= Ch2 E Metanolo ch3OH.
Il meccanismo della reazione passa attraverso la formazione del radicale CH3Oppure •, che attacca il doppio legame ricco di elettroni CHO2= Ch2. L'addotto risultante CH3-O-ch2-Cap2• Cattura un idrogeno da un CHO3Oh e forma il metil ether cho3-O-ch2-Cap3.
Lo studio di questo tipo di reazioni di irradiazione elettronica è utile nel campo della biochimica perché è stato determinato che il danno al DNA può causare o nel campo della chimica organometallica perché favorisce la formazione di nanostrutture.
Può servirti: precipitatoInoltre, è noto che vengono prodotte grandi quantità di elettroni secondari quando le radiazioni elettromagnetiche o di particelle interagiscono con la materia condensata nello spazio.
Pertanto, si stima che questi elettroni possano avviare trasformazioni chimiche in materia di polvere interstellare. Da qui l'importanza di studiare l'etere metil etile in queste reazioni.
Potenziale uso nei semiconduttori
Attraverso metodi di calcolo computazionale alcuni scienziati hanno scoperto che il metossietano o il metil etere possono essere adsorbiti dal grafene dopping con gallio (GA) (notare ciò che l'adsorbimento è diverso dall'assorbimento).
Il grafene è un nanomateriale formato da atomi di carbonio disposti formando un modello esagonale.
 Vista microscopica di grafene. Maido Merisalu [CC BY-SA 4.0 (https: // creativeCommons.Org/licenze/by-sa/4.0)]. Fonte: Wikipedia Commons.
Vista microscopica di grafene. Maido Merisalu [CC BY-SA 4.0 (https: // creativeCommons.Org/licenze/by-sa/4.0)]. Fonte: Wikipedia Commons. L'adsorbimento del metossietan sul grafene dopped si verifica dall'interazione tra l'ossigeno dell'etere e l'atomo di gallio che si trova sulla superficie del nanomateriale. A causa di questo adsorbimento c'è un trasferimento di carico netto dall'etere al gallio.
Dopo l'adsorbimento di metil etil etere e a causa di quel trasferimento di carico, il grafene doppicato con gallio presenta proprietà del semiconduttore di tipo-P.
Rischi
Metoxietano è altamente infiammabile.
Rimanendo in contatto con l'aria, ha la tendenza a formare perossidi instabili ed esplosivi.
Riferimenti
- O.S. Biblioteca nazionale di medicina. (2019). Etere etil metil. Recuperato da: pubchem.NCBI.Nlm.NIH.Gov.
- Irvine w.M. (2019) Ethhyl Methyl Ether (C2H5Och3). In: Gargaoud M. et al. (Eds). Enciclopedia dell'astrobiologia. Springer, Berlino, Heidelberg. Link recuperato.Springer.com.
- Terzo b. et al. (2015). Alla ricerca di trans etil metil eter in orione kl. Astronomia e astrofisica. 582, L1 (2015). NCBI recuperato.Nlm.NIH.Gov.
- Filseth, s.V. (1969). Il Mercurio 6 (3P1) Decomposizione fotosensibilizzata dell'etere di metil. Il Journal of Physical Chemistry. Volume 73, numero 4, aprile 1969, 793-797. Recuperato dai pub.sindrome coronarica acuta.org.
- Casanova, J.Jr. (1963). Preparazione e manipolazione degli studenti di gas-metil etere. Journal of Chemical Education. Volume 40, numero 1, gennaio 1963. Recuperato dai pub.sindrome coronarica acuta.org.
- Ure, w. e giovane, j.T. (1933a). Sul meccanismo delle reazioni gassose. Yo. La decomposizione temale dell'etere di metil etilico. The Journal of Physical Chemistry, Vol. XXXVII, n.9: 1169-1182. Recuperato dai pub.sindrome coronarica acuta.org.
- Ure, w. e giovane, j.T. (1933b). Sul meccanismo delle reazioni gassose. Ii. Catalisi omogenea nella decomposizione del metodo Ether Ether. The Journal of Physical Chemistry, 37, 9, 1183-1190. Recuperato dai pub.sindrome coronarica acuta.org.
- Shokuhi rad, a. et al. (2017). Studio DFT sull'adsorbimento di dietil, ethyl metil e dimetil eteri sulla superficie del grafene drogato con gallio. Scienza della superficie applicata. Volume 401, 15 aprile 2017, pagine 156-161. Recuperato da ScienceDirect.com.
- Schmidt, f. et al. (2019). Formazione indotta da elettroni di etil metil etere in miscele condensate di metanolo ed etilene. J. Phys. Chimica. A 2019, 123, 1, 37-47. Recuperato dai pub.sindrome coronarica acuta.org.

