Metalli alcalineter
- 4925
- 707
- Brigitta Ferrari
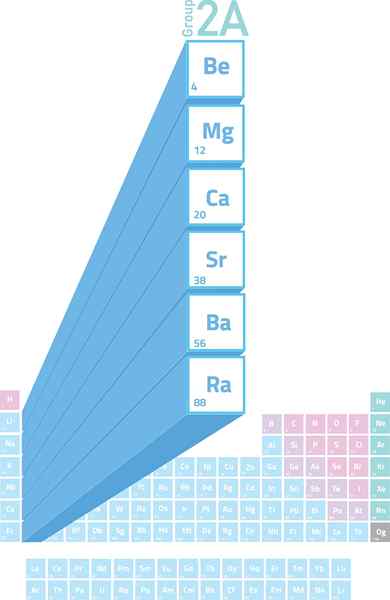
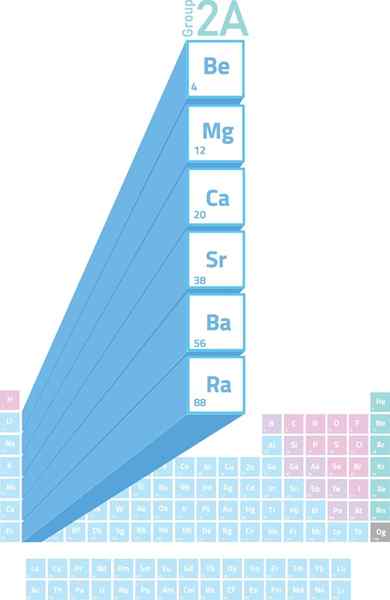 Posizione dei metalli alcalinotherro nella tavola periodica
Posizione dei metalli alcalinotherro nella tavola periodica Cosa sono i metalli alcalinanti?
IL Metalli alcalineter Sono gli elementi del gruppo 2 (precedentemente chiamato gruppo 2A) della tabella periodica. Vale a dire che sono formati dai 6 elementi della seconda colonna della tabella periodica che va dal berillio (BE) alla radio (RA).
Sono un gruppo di elementi metallici abbastanza reattivi e relativamente comuni. Hanno solo due elettroni di valenza situati in una s orbitale. Per questo motivo, appartengono ai blocchi della tavola periodica.
Il nome "Alkalinotrereo" deriva dall'unione di parole "alcaline", che è un altro modo di dire di base, e la terra, che è così che gli venivano raccontati gli ossidi. Quindi i metalli alcalinotherro significa letteralmente metalli che formano ossidi di base.
Questi metalli hanno molte applicazioni che li rendono importanti nella nostra società attuale, in particolare il magnesio. Queste applicazioni sono dovute alle loro proprietà particolari, che sono descritte di seguito.
Proprietà dei metalli alcalinotherro
Hanno un aspetto in metallo
Tutti i metalli alcalinotherro hanno colore argento con luminosità metallica. Il radon è anche radioattivo, quindi brilla nel buio emettendo una caratteristica luce verde.
Sono piccoli metalli densi
Tutti i metalli alcalinori sono più densi dell'acqua, ma sono meno densi della maggior parte degli altri elementi metallici nella tavola periodica.
Le densità in questo gruppo vanno da 1,54 g/cm3 Per calcio fino a 5,5 g/cm3 Per la radio, che è considerevolmente inferiore alle densità di altri metalli come il ferro (7,9 g/cm3), rame (9,0 g/cm3), piombo (11,3 g/cm3) ed El Mercurio (13,5 g/cm3), per dirne alcuni.
Hanno punti di fusione e bollitura relativamente bassi
Essendo metalli, i suoi punti di scioglimento e di ebollizione sono maggiori di quelli della maggior parte dei non metalli. Tuttavia, sono inferiori ai punti di fusione e di ebollizione della maggior parte degli altri metalli, con alcune eccezioni.
Può servirti: equazione di ArrheniusHanno Valencia +2
A causa della loro configurazione elettronica, questi metalli tendono a perdere due elettroni quando reagiscono con altri elementi come i non metalli. Per questo motivo, il suo unico Valencia è +2.
Sono relativamente reattivi
I metalli alcalinori sono molto più reattivi dei metalli come ferro o rame, ma sono meno reattivi dei metalli alcalini (gli elementi del gruppo 1). Più basso è il gruppo, più è reattivo il metallo.
Ad esempio, il berillio (il primo del gruppo) non reagisce con l'acqua mentre i seguenti due possono reagire con acqua calda e le ultime possono persino reagire con acqua fredda.
Reagire con aria per formare ossidi di base
Questi metalli tendono a formare ossidi di base quando reagiscono con l'ossigeno dell'aria. In effetti, questo è il motivo per cui sono chiamati alcaline. Questi ossidi, quando si dissolvono in acqua, diventano idrossidi che producono soluzioni alcaline o di base.
Applicazioni metalliche alkalinotherrous
Nel settore tecnologico
Alcuni dei metalli alcalinotherro sono usati nella produzione di semiconduttori. Questi sono essenziali nella costruzione di circuiti elettronici come quelli che contengono praticamente tutti gli apparecchi elettrici moderni, dai computer e nei telefoni cellulari, alle lavatrici, alle auto e altri.
Nell'industria alimentare
Il calcio è un nutriente essenziale per la vita. Fa parte della struttura delle ossa e ha altre importanti funzioni nel corpo. Per questo motivo, questo elemento viene aggiunto come fortificatore a molti alimenti dai cereali ai prodotti lattiero -caseari. Inoltre, viene utilizzato anche nella produzione di formaggi.
Può servirti: Cironium: storia, proprietà, struttura, rischi, usiNel settore automobilistico
Alcuni dei metalli alcalinotherro hanno proprietà meccaniche molto ottime, il che significa che sono duri e resistenti. Inoltre, sono resistenti alla corrosione, quindi sono spesso utilizzati nella produzione di ruote di lusso per auto e altre parti di esse.
Nell'industria militare
A causa delle loro proprietà meccaniche e della bassa densità, nella costruzione di aerei, satelliti ed elicotteri sono usati metalli come magnesio e berillio.
Inoltre, grazie alle loro proprietà elettriche vengono utilizzati anche nella produzione di diversi tipi di sensori e sistemi ottici ed elettronici che l'industria militare utilizza per creare armi e sistemi di comunicazione.
I sei metalli alcalini
Ci sono solo sei metalli alcalini. Successivamente, c'è una breve descrizione di ciascuno di essi:
Beryllio (be)
È l'elemento numero 4 della tabella periodica e il primo del gruppo di metalli alcalino -otherro. È un metallo molto leggero e forte con proprietà uniche che lo rendono utile nella produzione di semiconduttori.
Magnesio (mg)
Il magnesio è un metallo d'argento relativamente chiaro, con un punto di fusione e di ebollizione bassa (rispetto ad altri metalli). È molto difficile e resistente ed è spesso usato nella produzione di parti dell'auto e come additivo nella preparazione di leghe come alcuni tipi di acciaio.
È il secondo alcalino di metallo e elemento numero 12 della tabella periodica. Come altri elementi di questo gruppo, è un nutriente essenziale per la vita.
Calcio (CA)
Il calcio è il 5 ° elemento più abbondante nella corteccia terrestre. Si trova come carbonato di calcio in molti minerali e rocce ed è anche un elemento essenziale per la vita a causa della sua partecipazione alla formazione di ossa e alla sua importanza nel sistema nervoso.
Può servirti: cloruro di stronzio (SRCL2)Questo metallo è l'elemento numero 20 della tabella periodica, è nel quarto periodo ed è il terzo metallo alcalino.
Stronzio (SR)
L'elemento numero 38 e il quarto metallo alcalino sono stronti. È più pesante del calcio, ma sembra molto in termini di proprietà chimiche e fisiche. In effetti, lo stronzio può sostituire il calcio nelle ossa.
Ciò è particolarmente problematico quando ci esponiamo allo stronzio radioattivo che si verifica dopo una reazione nucleare, poiché, quando si aderiscono alle ossa, è molto difficile eliminare dal corpo e ci sta avvelenando con le radiazioni poco.
Bario (BA)
Questo elemento ha il numero atomico 56 e ha anche proprietà abbastanza simili a quelle di calcio e stronzio. È un metallo piuttosto morbido e molto reattivo che non è di natura elementare. È uno dei metalli alcalino -orizzonti con un carattere metallico maggiore.
Radio (RA)
L'ultimo elemento del gruppo Alcalinotrereos è la radio, un metallo radioattivo (da cui il suo nome) che emette una debole luce verde che è facile da osservare al buio.
Era usato molto nella preparazione di dipinti che brillano al buio, ma dopo che il pericolo di salute era scoperto, il suo uso era proibito.

