Metalli alcalini Proprietà fisiche e chimiche, usi, ottenendo
- 2585
- 616
- Ruth Cattaneo
IL metalli alcalini Questi sono gli elementi che fanno parte del gruppo I della tavola periodica, tranne l'idrogeno: litio (Li), sodio (NA), potassio (k), rubidide. A differenza della maggior parte dei metalli, hanno basse densità e sono molto reattivi. A causa di questa grande reattività chimica, non si trovano mai in natura nella loro forma elementare.
Questi metalli formano composti ionici semplici e stabili che, per la maggior parte, sono solubili in acqua; I metalli alcalini sono generalmente combinati con ioni alogenifro, solfato, carbonato e silicato. Tuttavia, alcuni elementi formano un numero limitato di composti complessi e organometalici.

In generale, le proprietà fisiche e chimiche dei metalli alcalini sono state ben studiate, ad eccezione di Francia a causa della sua natura radioattiva.
[TOC]
Proprietà fisiche
- I metalli alcalini sono argento, tranne il cesio, che è dorato. Conducono elettricità e calore e hanno bassi punti di fusione che diminuiscono anche con l'aumento del numero atomico, poiché il legame tra gli atomi è indebolito dall'aumento del raggio atomico.
- Il fatto di avere un solo elettrone di Valencia da parte di Atom rende debole anche il suo legame metallico. Di conseguenza, i metalli alcalini sono anche abbastanza morbidi da tagliarli con un coltello o una spatola.
- Tutti gli elementi adottano una struttura cubica centrata sul corpo. Poiché questo tipo di struttura cristallina non è confezionato e le radio atomiche dei metalli alcalini sono grandi, hanno basse densità rispetto ad altri metalli. In effetti, litio, sodio e potassio galleggiano in acqua.
- Differenze di energia tra gli orbitali dello strato di Valencia dei metalli alcalini coincidono con le lunghezze d'onda della luce visibile. Per questo motivo, quando si riscuote i composti formati da questi metalli in una fiamma, vengono generati i colori caratteristici.
Può servirti: TrinitrotoLueno (TNT): struttura, proprietà, usi, rischi, esplosione- In ordine discendente, i sali di litio danno un colore cremisi, sali di sodio un colore giallo, potassio un colore viola, rubidio di colore rosso bluastro e cessare un colore blu.
Proprietà chimiche
Tutti i metalli alcalini hanno somiglianze nelle loro proprietà chimiche.
- Hanno una configurazione elettronica di Valencia NS1, che si traduce in uno stato di ossidazione +1. A sua volta, ciò significa che perdono facilmente un elettrone per ottenere una configurazione di gas nobile.
- In generale, i metalli alcalini hanno le energie di ionizzazione più basse di tutti gli elementi, che diminuiscono anche quando il raggio atomico aumenta all'interno del gruppo perché lo strato di Valencia è sempre più distante dal nucleo. Questo spiega la reattività dei metalli alcalini e la formazione di ioni M+ in condizioni acquose facilmente.
- La tendenza termodinamica a formare ioni m+ è confermata dai potenziali standard delle coppie m+/m, che sono tutte grandi e negative. Tale tendenza implica che i metalli alcalini si ossidano facilmente e possono agire come potenti agenti riducenti.
- Questi elementi devono essere conservati in un olio non reattivo per evitare la reazione con ossigeno atmosferico. Sebbene il litio, il sodio e il potassio possano essere manipolati nell'aria per brevi periodi, Rubidio e Cesio devono essere gestiti in un'atmosfera inerte in ogni momento.
Ottenendo metalli alcalini
Sodio

Il modo migliore per ottenere sodio metallico prevede l'elettrolisi del cloruro di sodio fuso. Poiché il punto di fusione del cloruro di sodio è piuttosto elevato (808 ° C) ed è necessaria molta energia per mantenere grandi quantità di sostanza fusa, il cloruro di calcio (Cacl2) viene generalmente aggiunto per ridurre il punto di fusione a circa 600 ° C.
Può servirti: torbidimetriaIl sodio è ottenuto in uno stato liquido nel catodo con una purezza del 99,95% in un'atmosfera inerte.
Litio e potassio
Il litio può anche essere ottenuto dai suoi cloruri lanciati dall'elettrolisi, ma non è il caso del potassio perché è troppo solubile nel cloruro (KCl) e non galleggia sulla superficie della cellula. Inoltre, evapora facilmente alla temperatura operativa, quindi crea condizioni pericolose.
Pertanto, il potassio è ottenuto mediante riduzione del KCl fuso con sodio liquido. Il sodio presente in potassio viene eliminato condensando il vapore a 892 ° C e eseguendo una distillazione frazionaria di metalli liquidi.
Rubido e Cesio
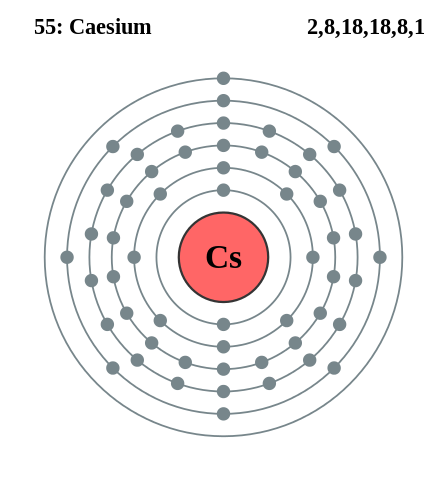 Configurazione elettronica di cesio. Fonte: Pumbaa (lavoro originale di Greg Robson) / CC BY-SA 2.0 UK (https: // creativeCommons.Org/licenze/by-sa/2.0/UK/Atto.In)
Configurazione elettronica di cesio. Fonte: Pumbaa (lavoro originale di Greg Robson) / CC BY-SA 2.0 UK (https: // creativeCommons.Org/licenze/by-sa/2.0/UK/Atto.In) Rubido e cesio possono essere ottenuti in modo simile, ma usando il calcio come agente riducente. Il cessium metallico può anche essere ottenuto mediante elettrolisi del cianuro di cesio fuso (CSCN).
Usi e applicazioni principali
Sodio come agente riducente
Poiché il sodio è molto facilmente ossidato, la sua applicazione più importante è come agente riducente per ottenere metalli come titanio, surround e hafnio. Viene anche usato come scambiatore di calore nei reattori nucleari nel suo stato liquido.
Potassio come fertilizzante
 Cloruro di potassio, fertilizzante. Fonte: Abbas cucaniensis/CC BY-SA (https: // creativeCommons.Org/licenze/by-sa/4.0)
Cloruro di potassio, fertilizzante. Fonte: Abbas cucaniensis/CC BY-SA (https: // creativeCommons.Org/licenze/by-sa/4.0) La maggior parte del potassio che viene elaborato va ai fertilizzanti sotto forma di cloruro di potassio. A sua volta, il cloruro viene utilizzato nella produzione di altri composti e soluzioni come l'idrossido di potassio, che viene utilizzato nella produzione di saponi liquidi.
Il cianuro di potassio viene utilizzato per l'estrazione o il rivestimento dei metalli per facilitare la deposizione di rame, argento e oro. Il potassio può anche essere trovato in alcuni esplosivi e come tintura dei fuochi d'artificio.
Può servirti: radio: struttura, proprietà, usi, ottenimentoLitio come agente in lega
Il litio metallico è usato come agente in lega nella produzione di leghe aeronautiche e aerospaziali in alluminio e magnesio. Ma con il passare del tempo, ha trovato un aumento dell'utilità come anodo della batteria alcalina.
Il litio metallico consente inoltre di ridurre le temperature di fusione e sinterizzazione di alcuni tipi di vetro e ceramica, oltre a diminuire il coefficiente di espansione. Il carbonato di litio è ampiamente utilizzato per trattare le condizioni bipolari, mentre il litio stearato è un lubrificante ampiamente utilizzato nel settore automobilistico.
Rubido e Cesio
Rubido e cesio sono generalmente utilizzati nelle stesse applicazioni, quindi uno di questi elementi può essere sostituito dall'altro. Le applicazioni includono vetro in fibra ottica nel settore delle telecomunicazioni, attrezzature per la visione notturna e cellule fotoelettriche. L'orologio Cesio (orologio atomico) viene utilizzato per la misura del tempo standard internazionale e per la definizione del secondo.
Riferimenti
- Chang, R., & Goldsby, K. A. (2016). Chimica (dodicesimo ed.). New York: Mc-Graw Hill.
- Halka, m., & Nordstrom, B. (2010). Metalli di terra alcali e alcalina. New York: Infobase Publishing.
- Miesler, g. L., Fischer, p. J., & Tarr, D. A. (2014). Chimica inorganica (5a ed.). New York: Pearson.
- Mishra, b., & Majumdar, G. (2017). Produzione di metalli alcali (Li, Na, K). Modulo di riferimento nella scienza dei materiali e ingegneria dei materiali. Elsevier.
- Petrucci, r. H., Harring, f. G., Bissonnette, c., & Maturo, j. D. (2017). Chimica generale: principi e applicazioni moderne (11 ° ed.). New York: Pearson.
- Shriver, d., Weller, m., Overton, t., Rourke, J., & Armstrong, F. (2014). Chimica inorganica (6a ed.). New York: W. H. Freeman.
- « In cui il continente c'è una maggiore concentrazione di popolazione?
- Caratteristiche dell'età del bronzo, periodi, strumenti e invenzioni »

