Metabisolfito di sodio (NA2S2O5) Struttura, proprietà, usi, rischi

- 2796
- 774
- Lino Lombardi
Lui metabisolfito di sodio È un composto inorganico formato da due ioni Na di sodio+ e uno ione metabisolfito o disulfito2O52-. La sua formula chimica è Na2S2O5. È un solido bianco cristallino. È usato come agente antiossidante e antimicrobico in una varietà di prodotti farmaceutici e funzioni come conservante in molte preparazioni alimentari.
Poi un2S2O5 Serve a trattare la farina per preparare biscotti e dolci di pasticceria perché aiuta a rompere le molecole proteiche e semplificare la mola.
 METABISULFITE NA di sodio2S2O5 solido. Nessun autore leggibile dalla macchina fornita. Walkerma assunto (in base alle richieste di copyright). [Dominio pubblico]. Fonte: Wikimedia Commons.
METABISULFITE NA di sodio2S2O5 solido. Nessun autore leggibile dalla macchina fornita. Walkerma assunto (in base alle richieste di copyright). [Dominio pubblico]. Fonte: Wikimedia Commons. È usato in molti alimenti trasformati per impedire loro di essere attaccati da funghi e batteri. Tra questi alimenti ci sono formaggi, succhi di frutta, salse, margarine, ecc.
Tuttavia, poiché sono stati notati alcuni effetti negativi sulla salute delle persone, gli organismi autorizzati controllano la massima quantità di metabisolfito di sodio2S2O5 che devono contenere questi alimenti.
Le altre applicazioni NA2S2O5 Di solito si basano sulle loro proprietà riducenti (l'opposto dell'ossidazione), come per ridurre la quantità di cloro nelle acque trattate, come la candeggina di lana, nelle formule cosmetiche, tra gli altri usi.
[TOC]
Struttura
Il metabisolfito di sodio è formato da due ioni Na di sodio+ e uno ione bisolfito s2O52-. Quest'ultimo ha due atomi di zolfo uniti insieme e cinque atomi di ossigeno distribuiti tra questi.
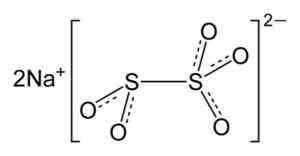 Struttura chimica del metabisolfito di sodio2S2O5. Autore: Benjah-BMM27. Fonte: Wikimedia Commons.
Struttura chimica del metabisolfito di sodio2S2O5. Autore: Benjah-BMM27. Fonte: Wikimedia Commons. Nomenclatura
-Metabisolfito di sodio
-Pyrosulfito di sodio
-Disolfito di sodio
-Disolfito di disodio
Proprietà
Stato fisico
Incolore, bianco o ingialtante cristallino. Cristalli esagonali.
Peso molecolare
190,11 g/mol
Punto di fusione
A temperature superiori a 150 ° C viene scomposto.
Peso specifico
Da 1,4 a 25 ° C/4 ° C
Solubilità
Molto solubile in acqua: 66,7 g/100 g di acqua.
Può servirti: ossigeno molecolare: struttura, proprietà, usiph
Le sue soluzioni acquose sono acide. Una soluzione al 10% ha un pH di 4,0-5,5.
Proprietà chimiche
Quando si dissolve in acqua è un acido corrosivo. Ha proprietà riducenti e antiossidanti.
Se è esposto all'aria, ossida lentamente il solfato di sodio2SW4, anche perdendo parte del suo contenuto così2.
Reagisce con l'acqua per dare bisolfito al sodio3, biossido di zolfo così2 e so di sodio solfito2SW3.
Ha un leggero odore di zolfo. Non è carburante, ma sotto calore può generare gas tossici.
Ottenimento
Il metabisolfito di sodio può essere ottenuto passando un eccesso di biossido di zolfo a gas2 per una soluzione di carbonato di sodio Na2Co3.
Usi nel cibo
Come conservante
Poi un2S2O5 È un antiossidante. Funge da conservante e inibitore di alcuni microrganismi. Il suo effetto antimicrobico è ottimale al di sotto del pH = 4, come nei succhi di frutta.
Permette di prevenire il deterioramento e rendere più lento l'utile di alcuni alimenti. È stato usato per esempio per evitare l'oscuramento delle patate dolci.
Viene usato durante il raccolto di gamberi marini per prevenire la formazione di macchie nere. I gamberi sono immersi in una soluzione di metabisolfito sul ghiaccio.
 A volte i gamberi sono immersi in soluzione acquosa di metabisolfito di sodio per impedire loro di deterioramento. Autore: Aakashkhatu1998. Fonte: Pixabay.
A volte i gamberi sono immersi in soluzione acquosa di metabisolfito di sodio per impedire loro di deterioramento. Autore: Aakashkhatu1998. Fonte: Pixabay. È un antiossidante efficace e migliora la ritenzione dell'acido ascorbico (vitamina C) nei frutti e sui succhi secchi. In questi inibisce alcuni tipi di batteri, funghi e lieviti.
È stato usato in Sudafrica per controllare il deterioramento e inibire l'oscuramento del frutto dei lichi. Tuttavia, sembra che il gusto di detto frutto cambi leggermente.
Altri alimenti usati sono formaggio, vari drink, margarina, salse, dolci e pesce.
Nell'industria del vino e in altre bevande
Nell'uva dopo la raccolta viene utilizzato come fungicida, poiché alcuni funghi possono crescere su questo frutto. Quindi agisci su alcuni microrganismi specifici, il che lo rende utile nell'industria vinicola perché consente di controllare la sua fermentazione.
Può servirti: 10 esempi di collegamenti covalenti non polariIl metabisolfito residuo è efficace dopo la fermentazione del vino per evitare la crescita dei lieviti tolleranti all'alcol.
È stato anche usato nel succo di mela e nel sidro per controllare alcuni microrganismi patogeni come Escherichia coli.
Per curare alcune farine, cereali e amidi
Serve a condizionare la massa di alcuni cibi cotti. Agisce come un agente riducente nella produzione di biscotti, in particolare quei casual nel grasso e nel povero di zucchero e nei dolci di pasticceria.
Il metabisolfito reagisce con i legami S-S delle proteine contenute nella farina di pasta con cui sono preparati i biscotti e i dolci, ammorbidendolo, rendendolo più estensibile e meno elastico.
Uno degli obiettivi è impedire che l'impasto venga respirato, prima o durante la cottura. Tuttavia, il suo uso nella massa dei cookie non è sempre accettato e si preferiscono altre alternative.
 Alcuni formaggi, marmellate e biscotti possono contenere metabisolfito di sodio come conservante. Autore: Steve Buissinne. Fonte: Pixabay.
Alcuni formaggi, marmellate e biscotti possono contenere metabisolfito di sodio come conservante. Autore: Steve Buissinne. Fonte: Pixabay. Serve anche a sbiancare gli amidi commestibili e ammorbidire i granuli di mais durante il processo di macinazione bagnata.
Cibi in cui non dovrebbe essere usato
La Food and Medicine Administration degli Stati Uniti, o FDA (per il suo acronimo per l'inglese Food and Drug Administration) Etichettato metabisulfito di sodio e marcato2S2O5 come sostanza "considerata generalmente sicura".
Tuttavia, è stato riconosciuto da questo corpo come un composto antitiamina o anti -amitamina B1.
Pertanto non dovrebbe essere usato nelle carni, né negli alimenti fonte di vitamina B1. Né dovrebbe essere usato in frutta o verdura che vengono vendute grezze ai consumatori o che sono presentati freschi.
Può servirti: clorito di sodio (NaClo2): struttura, proprietà, usi, rischiSecondo alcune fonti consultate se utilizzate in concentrazioni superiori a 10 mg/kg di cibo, deve essere segnalato sull'etichetta di questo.
Altri usi
Altre applicazioni NA2S2O5 sotto.
-Come agente riducente nelle formule cosmetiche e come antiossidante, ad esempio nei prodotti per la cura dei capelli.
-Come antiossidante nei preparati farmaceutici, come sciroppi o fluidi iniettabili. È usato in preparati acidi. Ha una certa attività antimicrobica, in particolare il pH acido.
-Come reagente di laboratorio, ad esempio per preservare l'istamina quando viene eseguita la sua analisi.
 Alcuni farmaci liquidi possono contenere Na2S2O5 Come conservante. Autore: Steve Buissinne. Fonte: Pixabay.
Alcuni farmaci liquidi possono contenere Na2S2O5 Come conservante. Autore: Steve Buissinne. Fonte: Pixabay. -Come agente riducente nello sviluppo di fotografie.
-Per ridurre il cloro nei processi industriali per il trattamento dell'acqua e delle acque reflue.
-Nel settore tessile: come candeggina di lana, come agente anticloro dopo il riciclaggio di denaro, per ridurre alcuni coloranti e solubilizzare altri.
-Per produrre biossido di zolfo2 Nel sito di utilizzo. Ad esempio in silos di erba fresca, il SO2 Prodotto dal metabisulfite di sodio sviluppa l'acidità rapidamente e consente la conservazione del materiale, poiché la fermentazione richiederebbe troppo tempo.
 La lana può essere sbiancante con metabisolfito di sodio. Autore: Jaclou DL. Fonte: Pixabay.
La lana può essere sbiancante con metabisolfito di sodio. Autore: Jaclou DL. Fonte: Pixabay. Rischi
-Se la Na è inalata2S2O5 Il solido è tossico. Il contatto diretto irrita fortemente la pelle, le mucose e i tessuti. È occhi irritanti e sistema respiratorio.
-Se ingerito direttamente, puoi produrre dolore addominale, diarrea, nausea e vomito.
-È corrosivo.
-Si dice che alcuni asmatici siano pericolosamente sensibili alle minuscole quantità di metabisolfito nei pasti.
-È dannoso per gli organismi acquatici.
Riferimenti
- Cauvain, s.P. (2017). MATERIE PRIME. In problemi di cottura risolti (seconda edizione). Recuperato da ScienceDirect.com.
- O.S. Biblioteca nazionale di medicina. (2019). Sodio metabisolfito. Centro nazionale per le informazioni sulla biotecnologia. Recuperato da Pubchem.NCBI.Nlm.NIH.Gov.
- Sivakumar, d. e Korsten, L. (2011). Litchi (Lush Chinensis Sonn.). In biologia e tecnologia posthavest dei frutti tropicali e subtropicali: Cocona al mango. Recuperato da ScienceDirect.com.
- DANYLUK, m.D. et al. (2012). Decontaminazione microbica dei succhi. Nella decontaminazione microbica nel settore alimentare. Recuperato da ScienceDirect.com.
- Wieer, h. (2012). L'uso di agenti redox in Bretadmaking. In Bretamaking (seconda edizione). Recuperato da ScienceDirect.com.
- Ercan, s. et al. (2015). Induzione del percorso infiammatorio omega 6 da parte del metabisolfito di sodio nel fegato di ratto e la sua attenuazione da parte della grelina. Lipidi in salute e malattia (2015) 14: 7. NCBI recuperato.Nlm.NIH.Gov.
- « Formule di calore e unità, caratteristiche, come vengono misurate, esempi
- Soluzione riscaldare come calcolati, applicazioni ed esercizi »

