Berillio idrossido (BE (OH) 2)
- 4325
- 1100
- Brigitta Ferrari
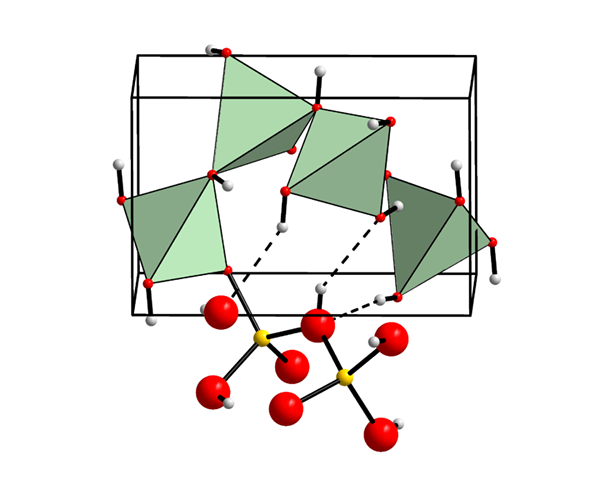
 Struttura chimica dell'idrossido di beryl. Fonte: Wikimedia Commons
Struttura chimica dell'idrossido di beryl. Fonte: Wikimedia Commons Cos'è l'idrossido di beryl?
Lui idrossido di berillio È un composto chimico formato da due molecole di idrossido (OH) e una molecola di berillio (BE). La sua formula chimica è (oh)2 Ed è caratterizzato dall'essere una specie di anfotato. In generale, può essere ottenuto dalla reazione tra berillio e monossido d'acqua, secondo la seguente reazione chimica:
Beeo + H2O → essere (oh)2
D'altra parte, questa sostanza anfotata presenta una configurazione molecolare di tipo lineare. Tuttavia, è possibile ottenere varie strutture di idrossido di beryl: forma alfa e beta, come una fase minerale e vapore, a seconda del metodo utilizzato.
Struttura chimica dell'idrossido di beryl
Questo composto chimico può essere trovato in quattro modi diversi:
Beryl alpha idrossido
Aggiungendo qualsiasi reagente di base come l'idrossido di sodio (NaOH) a una soluzione di sale di birra, si ottiene la forma alfa (α) dell'idrossido di beryl. Un esempio è mostrato di seguito:
2Naoh (diluito) + becl2 → essere (oh)2↓ + 2NACL
2Naoh (diluito) + bacio4 → essere (oh)2↓ + Na2SW4
Beryl Beeta Idroxide
La degenerazione di questo prodotto alfa forma una struttura cristallina tetragonale meta-stabile, che dopo un periodo di tempo prolungato è trasformato in una struttura rombica chiamata berillio beta idrossido (β).
Questa forma beta è anche ottenuta come precipitato da una soluzione di sodio berillio mediante idrolisi in condizioni vicine al punto di fusione.
Berilio idrossido in minerali
Sebbene non sia normale, l'idrossido di beryl si trova come un minerale cristallino noto come Behoite (chiamato in questo modo in riferimento alla sua composizione chimica).
Può servirti: acido non decilénico: struttura, proprietà, sintesi, usiSi verifica in pegmatita di granito formate dall'alterazione di gadolinita (minerali del gruppo silicati) nei fumaroli vulcanici.
Questo minerale - riflettente nuovo - è stato scoperto per la prima volta nel 1964 e attualmente è stato trovato solo in pegmatitas di granito situato negli stati del Texas e dello Utah, negli Stati Uniti.
Vapore di idrossido di berillio
A temperature superiori a 1.200 ° C (2.190 ° C), l'idrossido di beryl esiste in una fase a vapore. Si ottiene dalla reazione tra vapore acqueo e ossido di beryl (Beeo).
Allo stesso modo, il vapore risultante ha una pressione parziale di 73 pa, misurata a una temperatura di 1.500 ° C.
Proprietà di idrossido di ficcrossido
L'idrossido di beryl ha un peso molecolare molecolare o un peso molecolare approssimativo di 43.0268 g/mol e una densità di 1,92 g/cm3. Il suo punto di fusione è a una temperatura di 1.000 ° C, in cui inizia la sua decomposizione.
Come minerale, BE (OH)2 (Beoita) ha una durezza di 4 e la sua densità varia tra 1,91 g/cm3 e 1,93 g/cm3.
Aspetto
L'idrossido di berillio è un solido bianco, che nella sua forma alfa ha un aspetto gelatina e amorfo. D'altra parte, la forma beta di questo composto è costituita da una struttura cristallina ben definita, ortorrombica e stabile.
Si può dire che la morfologia del minerale di BE (OH)2 È vario, perché può essere trovato come cristalli reticolari, aggregati arborescenti o sferici. Allo stesso modo, è presentato in colori bianchi, rosa, bluastri e persino incolori e con una lucentezza vitrea grassa.
Proprietà termochimiche
Entalpia di allenamento: -902,5 kJ/mol
Gibbs Energy: -815,0 kJ/mol
Può servirti: cloro gassoso: formula, effetti, usi e rischiEntropia di addestramento: 45,5 J/mol
Capacità termica: 62,1 J/mol
Capacità termica specifica: 1.443 J/K
Entalpia di formazione standard: -20,98 kJ/g
Solubilità
L'idrossido di berillio è amfotilizzato, quindi è in grado di donare o accettare protoni e dissolvere sia in acidi che in media di base in una reazione a base di acido, producendo sale e acqua.
In questo senso, la solubilità di BE (OH)2 In acqua è limitato dal prodotto di solubilità KPS(H2O), che è uguale a 6,92 × 10-22.
Rischi di esposizione
L'esposizione umana ammissibile legale (PEL o OSHA) di una sostanza idrossido di beryl definita per una concentrazione massima tra 0,002 mg/m3 e 0,005 mg/m3 Sono 8 ore e per una concentrazione di 0,0225 mg/m3 Al massimo 30 minuti.
Queste limitazioni sono dovute al fatto che il berillio è catalogato come agente cancerogeno di tipo A1 (agente cancerogeno nell'uomo, basato sulla quantità di evidenza di studi epidemiologici).
Usi di idrossido di crediti
È molto limitato (e insolito) l'uso di idrossido di beryl come materia prima per la lavorazione di un prodotto. Tuttavia, è un composto usato come reagente principale per la sintesi di altri composti e ottenere berillio metallico.
Ottenimento
L'ossido di berillio (Beeo) è il composto chimico dell'alta purezza del berillio più utilizzato nell'industria. È caratterizzato come un solido incolore con proprietà isolante elettrica e alta conducibilità termica.
In questo senso, il processo per la sua sintesi (in qualità tecnica) nel settore primario viene eseguito come segue:
- L'idrossido di beryl viene sciolto in acido solforico (H2SW4).
- Eseguita la reazione, la soluzione viene filtrata, in modo che le impurità insolubili di ossido o solfato vengano eliminate.
- Il filtraggio è sottoposto a evaporazione per concentrare il prodotto, che viene raffreddato per ottenere cristalli di solfato di berillio4.
- Il bacio4 È calcinato a una temperatura specifica tra 1.100 ° C e 1.400 ° C.
Il prodotto finale (Beeo) viene utilizzato per la produzione di parti speciali in ceramica per uso industriale.
Ottenere berillio metallico
Durante l'estrazione e la lavorazione dei minerali di berillio, vengono generate impurità, come ossido di idrossido di beryl e beryl. Quest'ultimo è soggetto a una serie di trasformazioni fino al berillio metallico.
Essere (oh) reagisce2 Con una soluzione bifluoro di ammonio:
Essere (oh)2 + 2 (NH4) HF2 → (NH4)2Bef4 + 2 h2O
Il (NH4)2Bef4 È soggetto all'aumento della temperatura, che soffre una decomposizione termica:
(NH4)2Bef4 → 2nh3 + 2hf + bef2
Infine, la riduzione del fluoruro di berillio a una temperatura di 1.300 ° C con magnesio (mg) risulta in berillio metallico:
Bef2 + Mg → BE + MGF2
Il berillio viene utilizzato in leghe in metallo, produzione di componenti elettronici, produzione di schermi e finestre di radiazione utilizzate in dispositivi a raggi X.
Riferimenti
- Wikipedia (s.F.). Idrossido di berillio. Recuperato da.Wikipedia.org
- Holleman, a. F.; Wiberg, e. E Wiberg, n. (2001). Idrossido di berillio. Ottenuto dai libri.Google.co.andare
- Publishing, m. D. (S.F.). Behoite. Recuperato da manuale della mineralogia.org
- Tutte le reazioni (s.F.). Berillio idrossido essere (OH)2. Ottenuto da tutte le reactions.com
- PUBCHEM (S.F.). Idrossido di berillio. Recuperato da Pubchem.NCBI.Nlm.NIH.Gov
- Walsh, k. A. e vidal, e. E. (2009). Chimica e lavorazione del berillio. Ottenuto dai libri.Google.co.andare

