Fermio (FM)
- 4630
- 782
- Dott. Rodolfo Gatti
Cos'è Fermio?
Lui Fermio (FM) è un elemento chimico radioattivo che si ottiene indotto dalla trasmutazione nucleare, in cui le reazioni di tipo nucleare sono in grado di alterare artificialmente il nucleo di un elemento considerato stabile, e quindi causare un isotopo di natura radioattiva o un elemento che non fa esistono naturalmente.
Questo elemento fu scoperto nel 1952, durante il primo saggio nucleare di successo "IVI Mike", realizzato da un gruppo di scienziati dell'Università della California sotto la direzione di Albert Ghiriorso. Il Fermio è stato scoperto come un prodotto della prima esplosione di una pompa di idrogeno nell'Oceano Pacifico.
Anni dopo, il Fermio fu ottenuto sinteticamente in un reattore nucleare, bombardando il plutonio con neutroni; E in un ciclotrone, bombardamento di uranio-238 con ioni di azoto.
Attualmente il Fermio si verifica attraverso una lunga catena di reazioni nucleari, che prevede il bombardamento di ogni isotopo a catena con neutroni e quindi permettendo all'isotopo risultante di sperimentare una decomposizione beta.
Struttura chimica del fermio
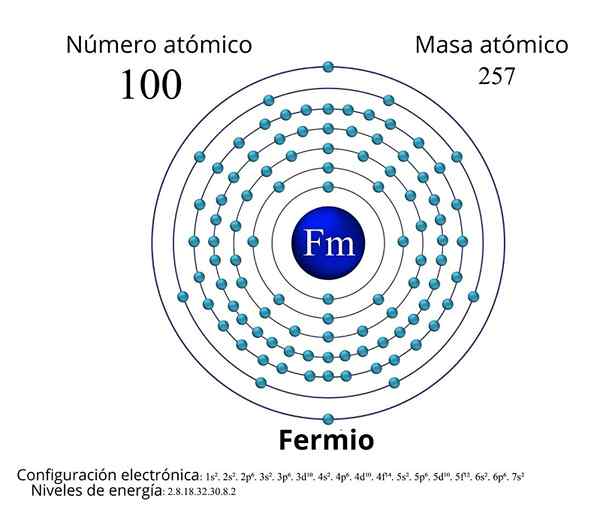
Il numero atomico del fermio (FM) è 100 e la sua configurazione elettronica è [RN] 5F12 7S2. Inoltre, si trova all'interno del gruppo di actinidi che fanno parte del periodo 7 della tavola periodica e, poiché il suo numero atomico è maggiore di 92, si chiama elemento transurico.
In questo senso, il fermio è un elemento sintetico e, quindi, non ha isotopi stabili. Per questo motivo non ha una massa atomica standard.
Inoltre, gli atomi - che sono isotopi tra loro - hanno lo stesso numero atomico, ma una massa atomica diversa, considerando che ci sono 19 isotopi noti dell'elemento, che vanno dalla massa atomica 242 a 260.
Può servirti: carbossimetilcellulosaTuttavia, l'isotopo che può verificarsi in grandi quantità in una base atomica è FM-257, con un'emivita di 100,5 giorni. Questo isotopo è anche il più grande numero atomico e di massa mai isolato da qualsiasi reattore o materiale prodotto da un'installazione termonucleare.
Sebbene Fermio-257 sia prodotto in quantità maggiori, il Fermio-255 è stato più regolarmente disponibile e viene utilizzato più frequentemente per studi chimici a livello di tracciante.
Proprietà Fermio
Le proprietà chimiche del fermio sono state studiate solo con quantità minime, in modo che tutte le informazioni chimiche disponibili che sono state ottenute provengano da esperimenti condotti con tracce dell'elemento. In effetti, in molti casi questi studi vengono condotti con solo pochi atomi, o anche un atomo allo stesso tempo.
Secondo la Royal Society of Chemistry, il Fermio ha un punto di fusione di 1527 ° C (2781 ° F o 1800 K), il suo raggio atomico è 2,45 Å, il suo raggio covalente è 1,67 Å e una temperatura di 20 ° C è in stato solido (metallo radioattivo).
Allo stesso modo, la maggior parte delle sue proprietà come lo stato di ossidazione, l'elettronegatività, la densità, il punto di ebollizione, tra gli altri, sono sconosciuti.
Fino ad oggi, nessuno è riuscito a produrre un campione sufficientemente ampio di Fermio per vederlo, sebbene l'aspettativa è che, come altri elementi simili, è un metallo grigio argento.
Comportamento nelle soluzioni
Il Fermio si comporta in condizioni di riduzione non forte in una soluzione acquosa come previsto per uno ione Actinid trivalente.
Può servirti: idrossido di nichel (ii): struttura, proprietà, usi, rischiIn acido cloridrico concentrato, soluzioni tiocianato di acido nitrico e ammonio, il fermio si forma anionico con questi ligandi (una molecola o uno ione che unisce un catione metallico per formare un complesso), che può essere adsorbito e quindi eliminare dalle colonne di scambio anionico.
In condizioni normali, il Fermio esiste in soluzione come ione FM3+, che ha un indice di idratazione di 16,9 e una costante di dissociazione acida di 1,6 × 10-4 (PKA = 3.8); Quindi si ritiene che l'unione nei successivi complessi di actinidi sia principalmente ionico.
Allo stesso modo, è previsto lo ione FM3+ essere più piccolo di uno ioni3+ (Plutonio, Americo o Curio), a causa della maggiore carico nucleare efficace di Fermio; Pertanto, ci si aspetterebbe che i Fermio formino i collegamenti in metallo più corti e forti.
D'altra parte, Fermio (III) può essere ridotto abbastanza facilmente a Fermio (II); Ad esempio, con cloruro di samarium (II), con il quale Coprecipita El Fermio (II).
Potenziale di elettrodo normale
È stato stimato che il potenziale dell'elettrodo sia di circa -1,15 V rispetto all'elettrodo di idrogeno standard.
Inoltre, l'FM2+/ Fm0 Ha un potenziale elettrodo di -2,37 (10) V, basato su misurazioni polarografiche; cioè, voltamperometria.
Decadimento radioattivo
Come tutti gli elementi artificiali, il Fermio sperimenta un decadimento radioattivo causato principalmente dall'instabilità che li caratterizza.
Ciò è dovuto alle combinazioni di protoni e neutroni che non consentono di mantenere l'equilibrio e cambiano spontaneamente o decadono fino a raggiungere una forma più stabile, rilasciando determinate particelle.
Può servirti: elettronegativitàQuesto decadimento radioattivo è dato dalla fissione spontanea attraverso una decomposizione alfa (perché è un elemento pesante) in California-253.
Usi e rischi
La formazione di Fermio non si verifica naturalmente e non è stata trovata nella crosta terrestre, quindi non c'è motivo di considerare i suoi effetti ambientali.
A causa delle piccole quantità di Fermio prodotte e della sua breve e mezza vita, attualmente non ci sono usi per questo dalla ricerca scientifica di base.
In questo senso, come tutti gli elementi sintetici, gli isotopi di Fermio sono estremamente radioattivi e sono considerati altamente tossici.
Sebbene poche persone entrano in contatto con il Fermio, la Commissione internazionale di protezione radiologica ha stabilito limiti di esposizione annuali per i due isotopi più stabili.
Per il Fermio-253, il limite di ingestione è stato stabilito in 107 Bequerel (1 BQ è equivalente a una decomposizione al secondo) e il limite di inalazione in 105 BQ; Per Fermio-257, i valori sono rispettivamente 105 BQ e 4000 BQ.

