Struttura stagno, proprietà, ottenimento, usi

- 1308
- 222
- Rosolino Santoro
Lui lattina È un metallo appartenente al blocco P della tavola periodica, il cui simbolo chimico è SN e che si trova nel gruppo 14, il carbonio. Nonostante sia un metallo ampiamente usato in tutta l'umanità sin dai tempi antichi, la verità è che è un metallo scarso nella crosta terrestre (2.3 ppm).
È un metallo argento, morbido, duttile e malleabile. Ha un numero atomico di 50 e i suoi stati predominanti o numeri di ossidazione sono +2 (SN2+) e +4 (Sn4+), Essendo i composti di stagno (ii), come lo Sncl2, Buoni agenti riducenti.
 Alotropi di stagno. Fonte: Zinn_9.Jpg: da: utente: tomihahndorf.Lavoro derivato: MaterialScientist/CC BY-S (https: // creativeCommons.Org/licenze/by-sa/2.0)
Alotropi di stagno. Fonte: Zinn_9.Jpg: da: utente: tomihahndorf.Lavoro derivato: MaterialScientist/CC BY-S (https: // creativeCommons.Org/licenze/by-sa/2.0) La scatola ha come simbolo SN, che è un'abbreviazione della parola latina "Stannum". La stagno è un metallo resistente all'attacco d'acqua e all'aria a temperatura ambiente; Ma nell'aria calda forma il biossido di stagno, snam2.
La proprietà di essere resistenti alla corrosione e avere un basso punto di fusione, ha servito ad avere numerose applicazioni; come il rivestimento di superfici metalliche e saldatura.
La scatola ha due forme altotropiche principali: la forma β bianca e solida; e i contesti α, grigi e normalmente polverosi (più fragili). Pertanto, la forma β è la più utilizzata nelle applicazioni di stagno.
Un'altra importante proprietà della stagno è la sua capacità di far parte di leghe con diversi metalli, il più antico è il bronzo, una lega di rame e stagno.
[TOC]
Scoperta
 Granuli di latta. Fonte: Nephronus, CC0, via Wikimedia Commons
Granuli di latta. Fonte: Nephronus, CC0, via Wikimedia Commons La stagno è un metallo che è noto dai tempi antichi. Pertanto, non si sa chi fosse il suo scopritore; E molto meno, l'anno e il luogo della sua scoperta.
Il bronzo è una lega di rame con stagno e arsenico. È possibile che l'elaborazione di questa lega sia una conseguenza di un fatto fortuito e non intenzionale, poiché i primi oggetti in bronzo - nell'era del bronzo - erano formati da rame e solo tracce di arsenico.
Questi oggetti sono apparsi nel Vicino Oriente dove l'arsenico è associato al rame. Ma dall'inizio è stata evidenziata la tossicità dell'arsenico, raggiungendo la sua sostituzione2).
Gli antichi greci ottennero latta dal commercio marittimo e si riferivano alla fonte della loro stagno come "i cassiteridi" che significa "isole di stagno". È possibile che queste isole fossero situate a cornuelles, britanniche o Spagna, dove ci sono grandi depositi di stagno.
Può servirti: subsalicilato di bismuto: struttura, proprietà, usi, effettiStruttura di stagno chimico
Quando ci sono due alotropi: la stagno bianco o β-SN e la stagno grigio o α-SN, avremo due strutture cristalline. Il β-sn è centrato tetragonale sul corpo (BCT), che caratterizza la malleabilità della stagno bianco.
Nel frattempo, la struttura dell'α-SN è diamante; Cioè, gli atomi SN sono collegati formando reti di tetraedra, senza l'esistenza di un legame metallico.
La stagno presenta anche altri due alotropi in diverse condizioni di pressione (nell'ordine del GPA) e la temperatura (sopra 161 ºC): σ-SN e γ-SN.
Configurazione elettronica
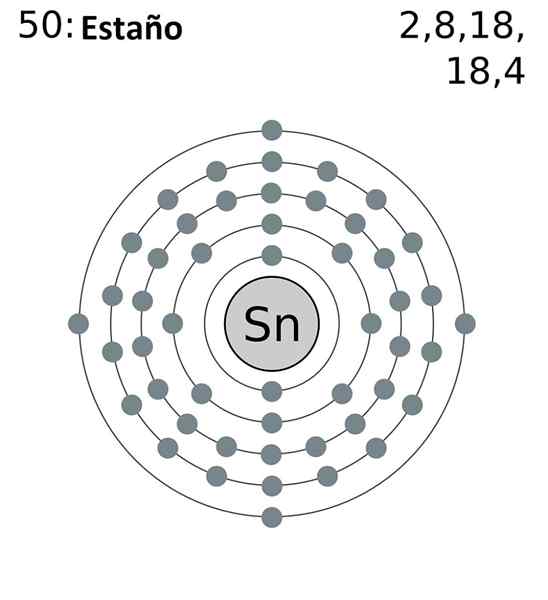
La configurazione elettronica abbreviata in latta è la seguente:
[Kr] 4D10 5s2 5 p2
Aggiunta di tutti gli elettroni avremo un totale di 14, lo stesso numero che corrisponde al tuo gruppo. Tuttavia, solo gli elettroni degli orbitali 5S e 5p sono quelli che partecipano alle reazioni chimiche della stagno, poiché quelli del 4D non sono energicamente disponibili.
Proprietà di stagno
Aspetto e caratteristiche fisiche
La stagno è un metallo morbido, duttile e malleabile, che può essere freddo e rotante. Il suo basso punto di fusione consente di aderire alle superfici di metalli o leghe come acciaio, rame e le sue leghe, proteggendoli dall'ossidazione.
Quando un pezzo di stagno è piegato, taglia, emettendo un suono caratteristico noto come "GHOUT TIN", una conseguenza della schiacciamento dei cristalli.
Tin ha due forme altropi: β e α. La forma β corrisponde a un solido bianco ed è responsabile delle applicazioni di stagno; Mentre la forma α è una polvere grigiastra.
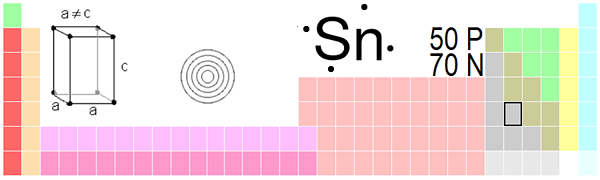 Posizione della latta nella tavola periodica. Fonte: Immagine di Daniel Mayer o Greatpatton e rilasciata in termini di GNU FDL
Posizione della latta nella tavola periodica. Fonte: Immagine di Daniel Mayer o Greatpatton e rilasciata in termini di GNU FDL La forma β è presentata a temperature superiori a 13.2 ºC. Quando la temperatura scende 13.2 ºC, la stagno cambia dalla forma β alla forma α. Questo fenomeno è indesiderabile ed è evitato aggiungendo altri metalli alla stagno, come l'antimonio o il bismuto, che bloccano questo cambiamento e prolungano la sua vita utile.
Tin è il primo superconduttore noto a temperature inferiori a 3.72 k.
Numero atomico
cinquanta
Massa molare
118.71 g/mol
Punto di fusione
231.93 ºC
Punto di ebollizione
2602 ºC
Densità
Alotropo β: 7.265 g/cm3
Alotropo α: 5.769 g/cm3
Stati di ossidazione
La stagno ha più stati di ossidazione: -4, -3, -2, -1, 0, +1, +2, +3, +4. Tuttavia, la maggior parte dei loro composti ha la scatola con stati di ossidazione +2 (SN2+) e +4 (Sn4+).
Può servirti: composti organiciEnergie di ionizzazione
Primo: 708.6 kj/mol
Secondo: 1411.8 kj/mol
Terzo: 2943.0 kj/mol
Elettronegatività
1.96 sulla scala Pauling
Reattività
La stagno è un metallo resistente all'azione dell'aria e dell'acqua a temperatura ambiente, ma quando viene riscaldato nell'aria forma ossido di stagno (IV), snam2, che è debolmente acido. Viene attaccato da acidi e alcali e in presenza di ossigeno può agire in alcuni casi come catalizzatore.
Ottenimento
 Il minerale di Casiterite è la principale fonte mineralogica di stagno. Fonte: Rob Lavinsky, Irocks.Com-CC-BY-SA-3.0/cc BY-SA (https: // creativeCommons.Org/licenze/by-sa/3.0)
Il minerale di Casiterite è la principale fonte mineralogica di stagno. Fonte: Rob Lavinsky, Irocks.Com-CC-BY-SA-3.0/cc BY-SA (https: // creativeCommons.Org/licenze/by-sa/3.0) La stagno, dal punto di vista della sua occorrenza, è un metallo raro, poiché ha un'abbondanza nella corteccia terrestre di soli 2 ppm. Il minerale di castiterite, un minerale di ossido di stagno, è l'unica fonte commerciale di stagno.
Il Casiterite è un minerale nerastro trovato nei terreni fangosi sulle rive dei fiumi. La scatola viene estratta dalla casiterite riscaldando fino a 1370 ºC con carbone o coke per produrre la sua riduzione.
La scatola prodotta è impura, quindi viene trattata con idrossido di sodio o acido cloridrico per solubilizzare la stagno. Quindi, questo è sottoposto a elettrolisi, essendo l'anodo di stagno e il catodo di ferro. La scatola viene depositata sul catodo, con una purezza superiore al 90%.
Usi/applicazioni
Protezione dalla corrosione
La stagno è metallo resistente alla corrosione. La lattina così chiamata o la stagno è un contenitore in acciaio, coperto da uno strato di stagno per evitare l'ossidazione.
Le lattine sono state utilizzate per conservare cibo e altre sostanze, ad esempio: dipinti, lacca, solventi, ecc. Ma sono attualmente sostituiti da contenitori in alluminio o plastica. I tubi e le valvole rivestiti di stagno mantengono acqua e bevande purezza.
Leghe
 I primi usi per le leghe di stagno erano produrre contenitori o utensili come lattine e brocche di questa dispensa. Fonte: Butterfly Voyages - Serge Ouachée/CC di -SA (https: // creativeCommons.Org/licenze/by-sa/3.0)
I primi usi per le leghe di stagno erano produrre contenitori o utensili come lattine e brocche di questa dispensa. Fonte: Butterfly Voyages - Serge Ouachée/CC di -SA (https: // creativeCommons.Org/licenze/by-sa/3.0) L'uomo ha iniziato a usare il bronzo per più di 5000 anni. Il bronzo è una lega di rame e stagno utilizzato nell'elaborazione di strumenti, armi, utensili per la casa.
Allo stesso modo la buccia, una lega inizialmente di stagno e piombo, veniva usata per creare vasi, piastre, ecc. Ma a causa della tossicità del piombo, la buccia è attualmente prodotta con lega di stagno, antimonio e cobalto.
Può servirti: acido ipoyodous (Hio)La lega e il piombo in latta hanno un basso punto di fusione, proprietà che ne ha consentito l'uso nella saldatura, una tecnica che serve a mettere insieme pezzi presenti nei circuiti elettrici ed elettronici. Ci sono automobili in cui la scatola è in lega di ferro, mentre vengono utilizzate nelle leghe di alluminio, stagno e titanio in alluminio aerospaziale.
Le leghe di circonium, chiamate anche zircaloy, sono usate nei reattori nucleari e hanno una piccola quantità di stagno.
 Campioni di stagno. Fonte: Ondřej Mangl, dominio pubblico, via Wikimedia Commons
Campioni di stagno. Fonte: Ondřej Mangl, dominio pubblico, via Wikimedia Commons La lega di argento e stagno è stata usata nelle amalgami dentali.
Una lega cristallina con l'elemento niobio è un superconduttore che funziona a una temperatura di 18 K e mantiene la sua proprietà in un forte campo magnetico.
Bicchiere
La scatola viene utilizzata nella procedura di Pilkington per produrre vetro finestre. Il vetro fuso viene posizionato su una superficie di stagno fuso, acquisendo il vetro una superficie piana e liscia. Questa tecnica è ancora utilizzata con successo.
I sali di stagno vengono spruzzati sul vetro per ottenere una fodera di potenza conduttiva, essendo in grado di utilizzare pannelli di illuminazione e parabrezza senza gelo.
Composti di stagno
Cloruro peccaminoso (sncl2) È usato in stagno zincato e come agente riducente nella produzione di polimeri e coloranti. Fluoruro di stagno (SNF2) È un ingrediente attivo nelle paste dentali.
Nel frattempo, il suo ossido è un utile catalizzatore in alcuni processi industriali. Inoltre, viene usato come polvere per lucidare l'acciaio.
I composti di stagno organico sono usati come biocidi e fungicidi, essendo tossici per l'uomo. Gli stabilizzatori di stagno organico vengono utilizzati per prevenire i cambiamenti nel cloruro di polivinile a causa dell'esposizione alla luce e al calore.
Il cloruro isñico (sncl4) è usato come stabilizzatore di profumo e come materiale di partenza per altri sali di stagno.
Riferimenti
- SHIVER & ATKINS. (2008). Chimica inorganica. (quarta edizione). Mc Graw Hill.
- Wikipedia. (2020). Lattina. Recuperato da: in.Wikipedia.org
- National Center for Biotechnology Information (2020). Lattina. Pubchem Comunund Sommario per CID 23974. Recuperato da: pubchem.NCBI.Nlm.NIH.Gov
- Dottore. Doug Stewart. (2020). Fatti per elementi di stagno. Recuperato da: Chemicool.com
- I redattori di Enyclopedia Britannica. (2020). Lattina. Recuperato da: Britannica.com
- Bell, Terence. (26 agosto 2020). Le proprietà, la produzione e le applicazioni di stagno. Recuperato da: Thoughtco.com
- Lentech b.V. (2020). Lattina. Recuperato da: lentech.com
- Stephanie PUPAS. (28 luglio 2015). Fatti su stagno. Recuperato da: LiveScience.com
- Atti della conferenza AIP. (9 febbraio 2018). Recupero di stagno dalle scorie di stagno usando il metodo di elettrolisi. doi.org/10.1063/1.5024070

